Tópico 5 - Editora Saraiva
Tópico 5 - Editora Saraiva
Tópico 5 - Editora Saraiva
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
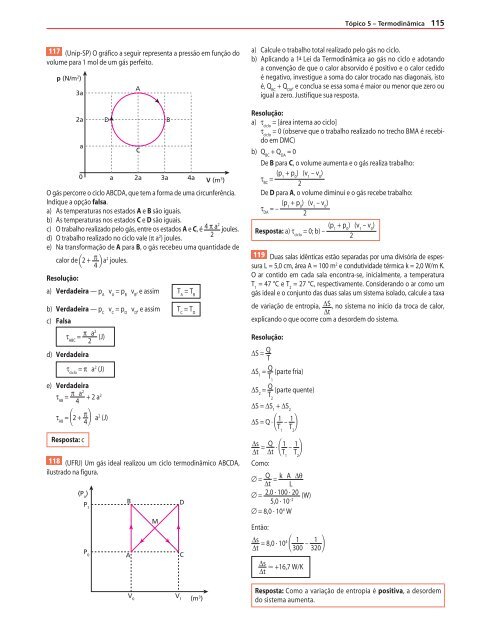
117 (Unip-SP) O gráf ico a seguir representa a pressão em função do<br />
volume para 1 mol de um gás perfeito.<br />
p (N/m 2 )<br />
3a<br />
2a<br />
a<br />
D<br />
A<br />
C<br />
0 a 2a 3a 4a<br />
B<br />
V (m 3 )<br />
O gás percorre o ciclo ABCDA, que tem a forma de uma circunferência.<br />
Indique a opção falsa.<br />
a) As temperaturas nos estados A e B são iguais.<br />
b) As temperaturas nos estados C e D são iguais.<br />
c) O trabalho realizado pelo gás, entre os estados A e C, é 4 π a2<br />
2 joules.<br />
d) O trabalho realizado no ciclo vale (π a2 ) joules.<br />
e) Na transformação de A para B, o gás recebeu uma quantidade de<br />
calor de 2 + π<br />
4 a2 joules.<br />
Resolução:<br />
a) Verdadeira — p v = p v , e assim T = T A A B B A B<br />
b) Verdadeira — p C v C = p D v D , e assim T C = T D<br />
c) Falsa<br />
τ ABC =<br />
d) Verdadeira<br />
π a2<br />
2 (J)<br />
τ ciclo = π a 2 (J)<br />
e) Verdadeira<br />
τ =<br />
π a2<br />
+ 2 a2<br />
AB 4<br />
τ AB = 2 + π 4 a2 (J)<br />
Resposta: c<br />
118 (UFRJ) Um gás ideal realizou um ciclo termodinâmico ABCDA,<br />
ilustrado na f igura.<br />
(P a )<br />
P 1<br />
P 0<br />
B D<br />
A<br />
V 0<br />
M<br />
C<br />
V 1<br />
(m 3 )<br />
<strong>Tópico</strong> 5 – Termodinâmica<br />
115<br />
a) Calcule o trabalho total realizado pelo gás no ciclo.<br />
b) Aplicando a 1 a Lei da Termodinâmica ao gás no ciclo e adotando<br />
a convenção de que o calor absorvido é positivo e o calor cedido<br />
é negativo, investigue a soma do calor trocado nas diagonais, isto<br />
é, Q BC + Q DA , e conclua se essa soma é maior ou menor que zero ou<br />
igual a zero. Justif ique sua resposta.<br />
Resolução:<br />
a) τ = [área interna ao ciclo]<br />
ciclo<br />
τ = 0 (observe que o trabalho realizado no trecho BMA é recebi-<br />
ciclo<br />
do em DMC)<br />
b) Q + Q = 0<br />
BC DA<br />
De B para C, o volume aumenta e o gás realiza trabalho:<br />
τ = BC (p1 + p0 ) (v1 – v0 )<br />
2<br />
De D para A, o volume diminui e o gás recebe trabalho:<br />
τ = – DA (p1 + p0 ) (v1 – v0 )<br />
2<br />
Resposta: a) τ = 0; b) – ciclo (p1 + p0 ) (v1 – v0 )<br />
2<br />
119 Duas salas idênticas estão separadas por uma divisória de espessura<br />
L = 5,0 cm, área A = 100 m2 e condutividade térmica k = 2,0 W/m K.<br />
O ar contido em cada sala encontra-se, inicialmente, a temperatura<br />
T = 47 °C e T = 27 °C, respectivamente. Considerando o ar como um<br />
1 2<br />
gás ideal e o conjunto das duas salas um sistema isolado, calcule a taxa<br />
de variação de entropia, ΔS , no sistema no início da troca de calor,<br />
Δt<br />
explicando o que ocorre com a desordem do sistema.<br />
Resolução:<br />
ΔS = Q<br />
T<br />
ΔS = 1 Q<br />
(parte fria)<br />
T1 ΔS = 2 Q<br />
(parte quente)<br />
T2 ΔS = ΔS + ΔS 1 2<br />
ΔS = Q · 1<br />
–<br />
T1 1<br />
T2 Δs<br />
=<br />
Q<br />
·<br />
1<br />
–<br />
Δt Δt T1 1<br />
T2 Como:<br />
∅ = Q<br />
=<br />
k A Δθ<br />
Δt L<br />
∅ = 2,0 · 100 · 20<br />
5,0 · 10 –2<br />
(W)<br />
∅ = 8,0 · 104 W<br />
Então:<br />
Δs<br />
= 8,0 · 104<br />
Δt<br />
Δs<br />
+16,7 W/K<br />
Δt<br />
1<br />
–<br />
1<br />
300 320<br />
Resposta: Como a variação de entropia é positiva, a desordem<br />
do sistema aumenta.