AÄRI VE AÄRI MEKANÄ°ZMALARINA GÃNCEL BAKIÅ Osman Nuri ...
AÄRI VE AÄRI MEKANÄ°ZMALARINA GÃNCEL BAKIÅ Osman Nuri ...
AÄRI VE AÄRI MEKANÄ°ZMALARINA GÃNCEL BAKIÅ Osman Nuri ...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
ADÜ Týp Fakültesi Dergisi2002; 3(2) : 37 - 48<br />
Derleme<br />
AÐRI <strong>VE</strong> AÐRI MEKANÝZMALARINA GÜNCEL BAKIÞ<br />
<strong>Osman</strong> <strong>Nuri</strong> AYDIN 1<br />
ÖZET<br />
Kimyasal, mekanik veya termal uyarýlar doku yaralanmasýna yol açarak veya damarsal bütünlüðü bozarak<br />
aðrýnýn subjektif etkilerine ilaveten otonomik (kalp hýzý veya kan basýncýnda deðiþiklik) veya hormonal (adrenal<br />
ve hipofizer sekresyonlar) yanýtlara neden olur.Aðrý fizyopatolojisini ve aðrý yolaklarýný bilmek, aðrý tedavisinde<br />
bize yardýmcý olur. Son yýllarda aðrýda rol oynayan fizyolojik ve kimyasal mekanizmalarýn daha iyi<br />
anlaþýlmasýyla aðrý tedavisinde çok önemli geliþmeler saðlanmýþtýr. Bu yazýda aðrý ile ilgili tanýmlamalar,<br />
sýnýflamalar ve aðrýda rol oynayan fizyolojik ve kimyasal mekanizmalar konusundaki güncel bilgiler gözden<br />
geçirilmiþtir.<br />
Anahtar kelimeler: Aðrý yollarý, aðrý algýlanmasý, serebral korteks, nosisepsiyon, nörotransmitter<br />
Current Inspect To Pain And Pain Mechanism<br />
SUMMARY<br />
Chemical, mechanical, or thermal stimuli lead to autonomic (changes in heart rate or blood pressure) or hormonal<br />
(adrenal and pituitary secretion) responses well as causing subjective sensation of pain by tissue destruction and<br />
disruption of vasculature integrity.Abetter understanding of pain physiopathology and pain pathways helps us in<br />
treatment of pain. Recent advances in our understanding of the chemical and physiologic pain mechanisms have<br />
provided us with important developments in pain therapy. In this article, current information about the definition<br />
and classification of pain and its chemical and physiologic mechanisms are reviewed.<br />
Key words: Pain pathways, pain perception, cerebral cortex, nociception, neurotransmitters<br />
Uluslararasý aðrý araþtýrmalarý derneði<br />
(International Association for the Study of<br />
Pain=IASP) aðrýyý, vücudun herhangi bir<br />
yerinden baþlayan, organik bir nedene baðlý olan<br />
veya olmayan, kiþinin geçmiþteki deneyimleri ile<br />
ilgili, sensoryal, emosyonel, hoþ olmayan bir<br />
duygu olarak tarif etmiþtir. Aðrýnýn, doku<br />
hasarýnýn bilinçsiz olarak farkýna varýlmasý<br />
1,2<br />
þeklinde de tanýmlanabileceði bildirilmiþtir.<br />
Merskey, aðrýyý; gerçekte mevcut olan veya<br />
potansiyel doku hasarý ile birlikte bulunan, hoþ<br />
olmayan duyusal ve emosyonel tecrübe olarak<br />
3<br />
tanýmlamýþtýr. Esener'e göre aðrý; herhangi bir<br />
dokuda hasar oluþtuðunda ortaya çýkan,<br />
kompleks ve nahoþ bir algýlama olup, hastayý<br />
4<br />
doktora getiren en önemli nedendir. Ertekin ise<br />
aðrýyý, bedenin bir köþesinden köken alan, hoþ<br />
olmayan, kiþiyi panik ve kaçýþ davranýþýna<br />
5<br />
yönelten algýlamadýr diye tariflemiþtir.<br />
Aðrý çeþitli þekillerde sýnýflanabilir;<br />
IASP Taksonomi Alt Komitesi; aðrýyý beþ<br />
eksenli taksonomi þeklinde, eksen bazýnda<br />
6<br />
tanýmlamýþtýr. Bu tanýmlamaya göre; 1. eksen<br />
aðrýnýn yer aldýðý vücut bölgesi ile ilgilidir. Ýkinci<br />
eksen aðrýnýn etkilediði sistemleri, 3. eksen<br />
oluþum süresini ele alýr. Dördüncü eksen,<br />
hastanýn ifadesine göre aðrýnýn þiddeti ve<br />
baþladýðýndan bu yana geçen süreyi, 5. eksen ise<br />
aðrýnýn etyolojisini belirtir.<br />
6<br />
Raj , aðrýyý 4 ana baþlýk altýnda tanýmlamýþtýr:<br />
1. Nörofizyolojik mekanizma: a.Nosiseptif, b.<br />
Somatik, c. Visseral,<br />
d. Nöropatik (nonnosiseptif), e. Psikojenik<br />
2. Süreye baðlý: a.Akut, b. Kronik<br />
3. Etiyolojik: a. Kanser aðrýsý, b. Postherpetik<br />
nevralji, c. Orak hücre anemisine baðlý aðrý,<br />
d.Artrit aðrýsý<br />
4. Bölgesel aðrý: a. Baþ aðrýsý, b. Yüz aðrýsý, c.<br />
Bel aðrýsý, d. Pelvik aðrý.<br />
Aðrý tanýmýnda sýk kullanýlan bir baþka<br />
sýnýflandýrmada, baþlama süresi, mekanizmasý ve<br />
2,4,7-11<br />
kaynaklandýðý bölge dikkate alýnmaktadýr.<br />
I. Aðrýnýn baþlama süresine göre<br />
sýnýflama<br />
1. Akut aðrý: Daima nosiseptif nitelikte<br />
olup, vücuda zarar veren bir olayýn varlýðýný<br />
gösterir. Neden olan lezyon ile aðrý arasýnda yer,<br />
þiddet ve zaman bakýmýndan yakýn iliþki vardýr.<br />
Nedenleri arasýnda, travma, enfeksiyon, doku<br />
hipoksisi ve enflamasyon sayýlabilir. Postoperatif<br />
akut aðrý en iyi örnektir. Akut aðrý, üzerinden 3-6<br />
ay süre geçtiðinde kronik aðrý özellikleri gösterir.<br />
2. Kronik aðrý: Çoðu kez nosiseptif<br />
nitelikte olup uyarýcý iþlevi geçtikten sonra,<br />
kiþinin hayat kalitesini deðiþtiren, kiþileri<br />
anormal davranýþlara yönelten, psikolojik<br />
etkenlerin rol oynadýðý kompleks bir tablodur.<br />
1<br />
Adnan Menderes Üniversitesi Týp Fakültesi Anestezyoloji ve Reanimasyon AD. AYDIN<br />
37
Aðrý ve aðrý mekanizmalarýna...<br />
Akut aðrýdaki kadar otonomik cevaplar yoktur.<br />
Sempatik tonus artýþý, nöroendokrin fonksiyonda<br />
artýþ belirgindir.<br />
II: Mekanizmalarýna göre aðrý<br />
sýnýflamasý<br />
1. Nosiseptif aðrý: Daha sonra etraflýca<br />
incelenecektir.<br />
2. Nöropatik aðrý: Nonnosiseptif aðrý için<br />
en yaygýn kabul gören terimdir. Nosiseptif<br />
aðrýdan en belirgin farký, sürekli bir nosiseptif<br />
6<br />
uyarýnýn bulunmamasýdýr. Santral veya periferik<br />
yaralanmaya sekonder yapýsal veya fonksiyonel<br />
sinir sistemi adaptasyonlarýnýn neden olduðu<br />
aðrýdýr. Önceleri psikojenik olarak<br />
deðerlendirilen aðrý, son zamanlarda daha iyi<br />
tanýmlanmýþ ve santral orijinli nöropatik aðrý<br />
olduðu anlaþýlmýþtýr. IASP santral aðrýyý,<br />
“santral sinir sisteminde fonksiyon bozukluðu<br />
veya primer lezyonun baþlattýðý veya neden<br />
11<br />
olduðu aðrý” olarak tanýmlamýþtýr. Spinal kord<br />
yaralanmasý, multipl sklerozis, epilepsi ve inme<br />
gibi yapýsal deðiþikliklere baðlý aðrýlar örnektir.<br />
Nöropatik ve nörojenik aðrý karýþtýrýlmamalýdýr.<br />
Nörojenik aðrý, herhangi bir nöropati oluþturma<br />
þartý aranmaksýzýn periferal sinir yaralanmasý ile<br />
ortaya çýkan aðrýdýr. Nöropatik aðrý metabolik<br />
hastalýklar sonucu ortaya çýkan aðrýyý da<br />
tanýmlamak için kullanýlýr. Aðrý spontan olarak<br />
ortaya çýkabilir. Aðrý eþiði düþtüðü için normalde<br />
aðrýsýz olan uyarý aðrý yapabilir (allodini).<br />
Uyarýya yanýt hem sürekli hem de amplitüd<br />
bakýmýndan abartýlý olabilir (hiperaljezi).<br />
Nöropatik aðrý opioid ilaçlara ve nörolitik<br />
iþlemlere nosiseptif aðrýdan daha az yanýt verir.<br />
Sinir kompresyonuna veya inflemasyonuna baðlý<br />
mononöropati, þimþek çakar gibi nevraljiler,<br />
diyabetik polinöropatiler ve deafferantasyon<br />
2,6<br />
aðrýsý nöropatik aðrý çeþitleridir.<br />
3. Deafferantasyon aðrýsý: Periferik ve<br />
santral sinir sistemi yaralanmalarý sonucunda<br />
somatosensoryal uyaran iletiminin merkezi sinir<br />
sistemine gidiþinin kesilmesi ile ortaya çýkar.<br />
Talamik aðrýlar, fantom aðrýlarý örnektir.<br />
4. Reaktif aðrý: Motor ya da sempatik<br />
afferentlerin refleks aktivasyonuyla<br />
nosiseptörlerin uyarýlmasý sonucu oluþan<br />
miyofasyal aðrý örnektir.<br />
5. Psikosomatik aðrý ( Psikojenik aðrý):<br />
Anksiyete ve depresyon gibi psikolojik<br />
sorunlarda doku hasarý varmýþ gibi algýlama<br />
olmaktadýr.<br />
38<br />
III: Kaynaklandýðý bölgeye göre aðrý<br />
sýnýflamasý<br />
1. Somatik aðrý: Somatik sinirlerden<br />
kaynaklanan, ani baþlayan, keskin, iyi lokalize<br />
edilen aðrýdýr.<br />
2. Viseral aðrý: Ýç organlardan kalkan aðrýlý<br />
uyaranlar, otonom sisteme ait afferent yollarla<br />
taþýnýrlar. Kolon, rektum ve mesaneden kalkan<br />
uyarýlar sakral parasempatik sinirlerle m.<br />
spinalise taþýnýr. Farenks, trakea ve ösefagusun<br />
üst kýsmýndan kalkan uyarýlar, glossofaringeus ve<br />
vagus sinirleri ile, geri kalan bütün organlardan<br />
kalkan uyarýlar sempatik sinirlerle m. spinalise<br />
taþýnýrlar. Kimyasal irritanlar, organlarýn ani<br />
gerilmesi, aþýrý kasýlmalar ve kan akýmýnýn<br />
azalmasý nedenler arasýnda sayýlabilir. Viseral<br />
aðrý yaygýn, lokalizasyonu güç, yansýyan tipte<br />
olabilir. Kan basýncý ve nabýz sayýsýnda deðiþme,<br />
kas rijiditesi ve hiperestezi ile birliktedir.<br />
3. Sempatik aðrý: Sempatik sinir<br />
sisteminin aktivasyonu ile ortaya çýkan damarsal<br />
kökenli aðrýlar, CRPS (kompleks rejyonal aðrý<br />
sendromu) ve kozaljiler örnektir.<br />
4. Periferal aðrý: Kaslar, tendonlar veya<br />
bizzat periferik sinirlerin kendinden köken<br />
alabilir.<br />
Bir baþka sýnýflandýrma da normal<br />
fonksiyon gösteren sinirler ile patoloji sonrasý<br />
fonksiyonlarý deðiþen sinirler arasýndaki farka<br />
2,4<br />
göredir;<br />
Derin aðrý: Eklem, tendon, kas ve fasyadan<br />
kalkan uyarýlar, cilttekine benzer olarak ince<br />
liflerle taþýnýr ve ayný yollarla iletilir. Genellikle<br />
künt ve zonklayýcý tiptedir. Ýyi lokalize edilemez<br />
ve yayýlma eðilimindedir. Derin aðrý, liflerin<br />
sonlarýnýn kimyasal maddelerle uyarýlmasý, kas<br />
liflerinin gerilmesi gibi mekanik etkiler sonrasý<br />
görülür.<br />
Yüzeyel aðrý: Deri ve mukozadan köken<br />
alan aðrýdýr.<br />
Yansýyan aðrý: Bazý organ ve derin<br />
dokulardan kaynaklanan aðrýlar, uyarý yerinden<br />
farklý bir yerde duyulabilir. Kardiyak aðrýnýn sol<br />
kola, diyagrafmatik aðrýnýn sol omuza yansýmasý<br />
gibi. Birçok dermal ve viseral afferent lifin, aðrý<br />
yolu üzerinde ayný ikinci nöron üzerine<br />
konverjansý ile açýklanmaktadýr.<br />
Tetik noktalarý (Trigger alanlar,<br />
Miyaljezik noktalar): Cilt, kas ve bað<br />
dokusunda küçük, yuvarlak, hipersensitif<br />
alanlardýr. Yansýyan aðrý ile yakýndan ilgilidir. En<br />
sýk olarak miyofasyal yapýlarda görülürler. Akut<br />
yaralanmalarda yaralanma bölgesi dýþýnda da<br />
oluþmaktadýr. Bu noktalar basýnç, iðneleme,
Aydýn<br />
hareket, gerilme, aþýrý sýcak veya soðukla aktive<br />
olur. Kas-iskelet sistemindeki bir çok tetik<br />
noktasýnýn yerleþimi, klasik akupunktur<br />
noktalarýna uymaktadýr. Tedavide, noktanýn<br />
belirlenmesi ve lokal anestezik ile bloke edilmesi<br />
etkili olmaktadýr.<br />
Aðrý tanýmlanmasýnda kullanýlan tanýmlar;<br />
2,4,10<br />
Allodini: Aðrý olmamasý gereken<br />
dokunmayý, aðrý olarak algýlama<br />
Analjezi: Aðrý duyusunun olmamasý<br />
Anestezi: Aðrý da dahil bütün hislerin kaybý<br />
Anestezi dolorosa: Duyu kaybý olan<br />
bölgede aðrý<br />
Dizestezi: Uyarý ile veya uyarýsýz olarak<br />
nahoþ ve anormal duyu<br />
Hipoaljezi: Aðrýlý uyaranlara azalmýþ<br />
reaksiyon<br />
Hiperestezi: Aðrýlý uyaranlara artmýþ<br />
reaksiyon, sensoryal liflerin aþýrý duyarlýlýðý<br />
Hiperpati: Hiperestezi, allodini,<br />
hiperaljezi+artmýþ reaksiyon+uyarý kesildikten<br />
sonra da duyunun devamý<br />
Hipoestezi: Azalmýþ cilt duyarlýlýðý (hafif<br />
dokunma, basý ve ýsýya karþý)<br />
Kozalji: Periferik sinirlerdeki tahribat<br />
sonucu geliþen, yanýcý karakterdeki aðrýdýr. Ýlgili<br />
bölgeye çok hafif dokunma bile aðrý oluþturabilir.<br />
Nöralji: Bir spinal veya kranial sinirin<br />
daðýlým alanýnda görülen, tekrarlayýcý, þiddetli ve<br />
genellikle ilgili cildin uyarýlmasý ile baþlayan bir<br />
aðrýdýr.<br />
Parestezi: Belirli bir bölgede, herhangi bir<br />
uyarý olmadan, spontan olarak iðnelenme,<br />
karýncalanma veya uyuþma hissedilmesidir.<br />
Dorsal kök, periferik sinir veya santral sinir<br />
sistemi irritasyonuna baðlý olabilir.<br />
Radikülopati: Bir veya birden fazla sinir<br />
kökünün anormal fonksiyonu<br />
Hiperaljezi: Zararlý uyarýlara abartýlý<br />
reaksiyondur.<br />
Fizyolojik aðrý: Doku hasarý yapabilecek<br />
þiddete yakýn, ancak belirgin bir enflamasyon ya<br />
da sinir hasarý uyarýlarýnýn neden olduðu duyu<br />
þeklidir. Mekanik, kimyasal veya termal<br />
uyarýlarýn etkileri, basý, yanma, sýcak ve soðuk<br />
þeklinde algýlandýklarý derecenin biraz üstüne<br />
çýktýklarýnda artýk aðrý olarak algýlanmaktadýr.<br />
Patolojik aðrý: Doku enflamasyonu ve sinir<br />
hasarý sonunda ortaya çýkmaktadýr.<br />
Nosisepsiyon<br />
Aðrý, kapsülsüz sýnýr sonlarýnýn aktivasyonu<br />
sonucu doku yaralanmasýyla oluþur. Bedenin bir<br />
bölgesindeki doku yaralanmasýnda uyarýnýn<br />
özelleþmiþ sinir uçlarý ile (nosiseptör) alýnýp,<br />
santral sinir sistemine götürülmesi, belirli bölge<br />
ve nöral yapýlarda integre edilmesi, bu zararlý<br />
tehdidin (noxious uyarý) algýlanmasý, buna karþý<br />
fizyolojik, biyoþimik ve psikolojik önlemlerin<br />
harekete geçirilmesidir. Nosisepsiyon, doku<br />
hasarý ile aðrýnýn algýlanmasý arasýnda oluþan<br />
karmaþýk elektrokimyasal olaylar serisinin<br />
1,4,9<br />
bütünüdür. Aðrý, nosisepsiyon içinde bir<br />
5<br />
algýlama olayýdýr. Latincede Noci,<br />
zarar veya<br />
zedelenme anlamýndadýr. Travmatik veya<br />
noxious stimulasyona nöral cevaptýr. Tüm<br />
nosiseptör uyarýlar aðrý oluþturur, fakat tüm<br />
2<br />
aðrýlar nosisepsiyondan kaynaklanmaz. Aslýnda<br />
nosiseptörler periferik terminalleri aðrýlý<br />
uyaranlara hassas primer afferent ve tüm deri,<br />
deri altý dokularýnda bulunan çýplak ve serbest<br />
4<br />
sinir uçlarýdýr. Miyelinsiz C lifleri ile miyelinli<br />
A-delta ( δ) liflerinin distal uzantýlarýndan<br />
oluþmuþlardýr ve 100-400 µ m uzunluðundaki<br />
aksonal sonlanmalar, küçük kan damarlarý ve<br />
11<br />
mast hücreleri kenarýnda sonlanýrlar. A-delta<br />
liflerinin uçlarý genellikle uyarýldýklarý tipe göre<br />
termal veya mekanik nosiseptörler adýný alýr ve<br />
30 m/sn hýzda ileti oluþtururlar. Dolayýsýyla bu<br />
nosiseptörlerin aktivasyonu keskin, iðneleyici ve<br />
iyi lokalize edilebilen bir aðrý oluþturur. C<br />
liflerinin uçlarý, polimodal nosiseptör adýný alýr<br />
ve þiddetli mekanik, kimyasal, aþýrý sýcak ve<br />
soðuk uyaranlarla aktive olurlar. C lifleri,<br />
enflamasyonda olduðu gibi gecikmiþ, yanýcý ve<br />
inatçý karakterdeki aðrýdan sorumludurlar.<br />
Ýmpulslarý 0.5-2 m/sn gibi çok yavaþ olarak<br />
ilerletirler. Dolayýsýyla daha donuk, daha yaygýn<br />
1,5<br />
aðrý ve hiperestezi oluþtururlar. Sinir liflerinin<br />
özellikleri ve fonksiyonlarý Tablo I'de<br />
özetlenmektedir.<br />
Tablo I:<br />
Sinir liflerinin özellikleri ve fonksiyonlarý<br />
Grup Çap ( µ ) Miyelin Fonksiyon<br />
A 20-12 + Motor (efferent), duyusal<br />
A 12-6 + Motor, afferent<br />
(Proprioseptif, dokunma)<br />
A 8-2 + Sensorial<br />
(aðrý, ýsý, dokunma)<br />
A 5-2 + Otonom<br />
(efferent pregangliyoner)<br />
B 3 + Sensorial<br />
(aðrý, ýsý, dokunma)<br />
C 1.2 - Otonom<br />
(postgangliyoner sempatik)<br />
Normal fizyolojik koþullarda aðrý ve<br />
nosisepsiyon, hoþ olmayan bir algýlama olarak<br />
39
Aðrý ve aðrý mekanizmalarýna...<br />
görülse de amacý organizmayý zararlý bir<br />
saldýrýdan korumak ve ilgili savunma<br />
5<br />
mekanizmalarýný ortaya çýkarmaktýr.<br />
Nosiseptif proçesin periferal<br />
komponentleri<br />
Periferik çýplak sinir uçlarýnýn uyarýlmasý,<br />
12-14<br />
nörotransmitter salýnýmýna yol açar. Substant P<br />
(SP) ve diðer taþikininlerin (Tablo II) lokal<br />
salýnýmý, vazodilatasyon ve plazma<br />
ekstravazasyonuna yeter miktarda iseler ödem<br />
15<br />
oluþur. Vazodilatasyonu takiben histamin ve<br />
bradikinin, kan hücrelerinden lokal olarak salýnýr<br />
ve ikisi de nosiseptörleri sonraki uyarýlar için<br />
sensitize edebilir (hiperaljezi). Doku yaralanmasý<br />
ve SPmast hücrelerini aktive eder.<br />
Tablo II: Periferal duyarlýlýkta oluþan nöroaktif substantlar<br />
Madde Kaynak Sinir sonundaki<br />
etkileri<br />
Substans P Sinir terminalleri Sensitizasyon<br />
Bradikinin Plazma kininojen Aktivasyon<br />
Histamin Trombositler, Aktivasyon<br />
mast hücresi<br />
Protonlar Ýskemi, Aktivasyon<br />
(düþük pH) zedelenmiþ hücreler<br />
Prostoglandinler Araþidonik asit, Sensitizasyon<br />
zedelenmiþ hücreler<br />
Lökotrienler Araþidonik asit, Sensitizasyon<br />
zedelenmiþ hücreler<br />
Interlökinler Mast hücreleri Aktivasyon ve<br />
sensitizasyon<br />
TNF-α<br />
Mast hücreleri Aktivasyon ve<br />
Sensitizasyon<br />
Primer afferent lif transmitterleri; Küçük<br />
liflerin çoðu eksitatör amino asitleri (EAA),<br />
aspartat, glutamat ve nöropeptidleri (substant P,<br />
kalsitonin, gen-related peptid, kolesistokinin,<br />
galanin, somastatin vb.) içerir. Bu maddeler<br />
sýklýkla ayný afferent terminalde<br />
2,15,16<br />
toplanmýþlardýr. Eksitatör amino asitler hem<br />
geniþ hem de küçük çaplý primer afferent liflerde<br />
bulunurlar ve eklem inflamasyonunda kronik<br />
veya akut nosiseptif uyarý sonucu A-beta ( β)<br />
liflerince aktive edilen düþük akýmlý elektrik<br />
17,18<br />
aktivitesi sonucu salýndýklarý gösterilmiþtir.<br />
Eksitatör amino asit reseptörlerinin, N-metil-Daspartat<br />
(NMDA) ve non-NMDA<br />
(AMPA/kainate ve metabotropik) reseptörleri<br />
gibi postsinaptik ve spinal dorsal boynuz<br />
19,20<br />
hücrelerinde bulunan bir çok alt tipi vardýr.<br />
Çeþitli çalýþmalarda, hem NMDA hem de non-<br />
NMDA reseptör agonistlerinin intratekal olarak<br />
uygulanmasýnda nosifensif davranýþ oluþtuðu<br />
21,22<br />
bildirilmiþtir.<br />
Sinirle inerve edilen periferik hedefler,<br />
40<br />
afferent liflerin çapýndan çok peptid içeriði ile<br />
ilgilidir. Aslýnda sinirler yeni periferal dokularý<br />
tekrardan uyardýklarýnda peptid içerikleri<br />
deðiþmiþ gibi gözükür (afferent axonun fenotip<br />
transmitteri deðiþir). Nosiseptif dorsal boynuz<br />
nöronlarýnýn büyük kýsmý, substance P içeren<br />
23<br />
snapslarýn önemli kýsmýyla baðlantýlýdýr.<br />
Periferde salýnan ve noxious uyarý özelliði<br />
taþýyan nörotransmitterler;<br />
Bradikinin: Zararlý mekanik uyarý ile hücre<br />
zarý permeabilitesi bütünlüðü bozulur ve lokal<br />
hücre yýkýmý sonrasý hücre dýþýna öncül maddeler<br />
çýkar. Bradikinin, nosiseptörü direkt olarak<br />
aktive eder ve çevre damarlarda vazodilatasyon<br />
yaratýr. Ayrýca hücre zarlarý üzerine etki yaparak<br />
prostoglandin oluþumuna da katkýda bulunur.<br />
Serotonin: Trombositlerden salýnýr. Direkt<br />
olarak nosiseptörü aktive eder. Hücre zarlarýna<br />
etki ederek prostaglandinlerin salýnmasýna yol<br />
açar.<br />
Direkt doku travmasý ile serotonin ve<br />
bradikinin hücre membranlarýnda fosfolipidler<br />
üzerine etki yapmasý ile prostoglandinler ve<br />
16<br />
lökotrienler serbest hale gelir. Burada anahtar<br />
durumundaki öncü madde araþidonik asittir<br />
(Tablo II). Siklooksijenaz enzimi ile siklik<br />
endoperoksitler ve buradan da prostaglandinler<br />
oluþur. Prostaglandinler, hem nosiseptif<br />
duyarlýlýðý artýrýrlar hem de lokal dolaþýmda<br />
vazodilatasyonu artýrarak daha fazla algojenik<br />
madde birikmesine yol açarlar. Refleks<br />
mekanizma ile duyarlý hale gelen nosiseptör<br />
uçlardan nöropeptidler çevre dokuya salgýlanýr.<br />
Özellikle P maddesi, nörokinin A ve CGRP<br />
(calsitonin- gene related protein) gibi taþikininler<br />
bölgede ödem ve yangýnýn baþlamasýna yol<br />
açarlar. P maddesi mast hücrelerinden histamin<br />
17,18<br />
salýnmasýna neden olur.<br />
AÐRININALGILANMASI<br />
Periferde bulunan aðrýya hassas<br />
nosiseptörlerin aktivasyonu veya hasar görmüþ<br />
dokudan salýnan mediyatörler tarafýndan,<br />
medulla spinalise afferent transmisyon ve dorsal<br />
boynuz üzerinden yüksek merkezlere ileti<br />
1,5,24<br />
aþamalarý ile gerçekleþir.<br />
Aðrý 4 aþamada algýlanýr;<br />
1. Transdüksiyon: Sinirlerin sensoryal<br />
uçlarýnda, stimulusun elektriksel aktiviteye<br />
dönüþtürüldüðü aþamadýr.<br />
2. Transmisyon: Ýmpulslarýn sensoryal<br />
sinir sistemi boyunca yayýldýðý aþamadýr.
Aydýn<br />
a. Primer sensoryal afferent nöronlarýn,<br />
elektriksel aktiviteyi spinal korda iletmesi<br />
b. Uyarýnýn spinal kordda, assendan ileti<br />
sistemi ile beyin sapý ve talamusa iletilmesi<br />
c. Talamokortikal projeksiyon<br />
3. Modülasyon: Nosiseptif transmisyonun<br />
nöral etkenlerle modifiye olmasýdýr.<br />
4. Persepsiyon: Bireyin psikolojisi ile<br />
etkileþimi ve subjektif emosyonel deneyimleri<br />
sonucu geliþen, uyarýnýn algýlandýðý son<br />
aþamadýr.<br />
Spinal veya belirli kranyal sinirlerdeki C<br />
lifleri veya A-delta liflerindeki elektriksel<br />
impulslar olarak spinal kök veya beyin köküne<br />
gider. Bir seri kompleks kimyasal etkileþimler ile<br />
sinaptik bileþkeyi geçtikten sonra sinyal<br />
nosiseptif spesifik yüksek SSS seviyelerine bir<br />
kez daha elektriksel olarak geçer. Ya da aðrýya<br />
daha az spesifik WDR nöronlarýna gider.<br />
Aðrýnýn iletimi ve algýlanmasý konusunda<br />
Ken Casey'in “nosisepsiyon dorsal boynuzda<br />
doðar, beyine ulaþýncaya kadar onu aðrý olarak<br />
25<br />
isimlendiremeyiz” ifadesini unutmamalýyýz.<br />
Aðrý iletimi ile ilgili nöronlar<br />
A-delta ve C lifleri omuriliðe girince hemen<br />
ikiye ayrýlýrlar. Birkaç segment yukarý aþaðýya<br />
devam ederek Lissauer traktusunun bir kesimini<br />
oluþtururlar. Bunlarýn akson kollateralleri de<br />
dorsal boynuz içine girer. Nosiseptif sinir<br />
uçlarýnýn bu santral terminalleri dorsal boynuz gri<br />
cevherinin marjinal zonu (lamina-I) ile subsantia<br />
gelatinosa (lamina-II)'da yer alan nöronlarla<br />
sinaps yaparlar. Bazý A-delta liflerinin uzantýlarý<br />
daha derinde bulunan lamina-V hücrelerine<br />
1,5,26<br />
ulaþýr.<br />
Aðrýlý uyaranlarý taþýyan periferik liflerin<br />
hücre cismi, yani aðrý yolunun 1. nöronu arka<br />
kök ganglionlarýnda yer alýr. Buradan kalkan<br />
lifler spinal korda girer ve substantia<br />
gelatinosa'da (SG) arka boynuz hücreleri ile<br />
sinaps yapar (2. nöron). Yani aðrý iletiminde<br />
ikinci durak spinal korddur. Substantia<br />
gelatinosa'da enkefalinerjik ara nöronlar<br />
bulunmaktadýr. Aðrý yolunun 3. nöronu<br />
1,5,26<br />
talamustadýr.<br />
Arka boynuzdaki nöronlar 3 çeþittir.<br />
a. Projeksiyon nöronlarý (santral geçiþ<br />
hücreleri); oluþan sinyal ve impulslarý<br />
anterolateral afferent sistemden üst merkezlere<br />
iletirler. Projeksiyon nöronlarýný baþlýca iki<br />
grupta incelemek olasýdýr. Lamina I'de yoðun<br />
olarak bulunan ve sadece A-delta ve C-lifleri ile<br />
uyarýlan projeksiyon nöronlarý “nosiseptif<br />
spesifik=NS” dir. Lamina I ve V'de bulunan<br />
ikinci grup projeksiyon nöronlarý, hem<br />
nosiseptörlerden hem de düþük eþikli<br />
mekanoreseptörlerden lif uyarýmý alan “wide<br />
26<br />
dynamic range=WDR” nöronlarýdýr.<br />
b. Eksitatuar nöronlar; aðrýlý uyaranlarý<br />
projeksiyon nöronlarýna ileterek eksite<br />
26<br />
olmalarýný saðlarlar.<br />
c. Ýnhibitör nöronlar; geniþ çaplý liflerle<br />
eksite olduklarýnda projeksiyon nöronlarýnda<br />
inhibisyona neden olurlar. Genellikle C ve A-<br />
delta liflerinden gelen sinyallerle aktive olan bu<br />
ara nöronlar, aðrýlý sinyalleri projeksiyon<br />
nöronuna geçirirler.<br />
Aðrýlý uyarýlarý üst merkezlere geçirmede,<br />
dorsal boynuzda baþlýca iki týp nörotransmitter<br />
rol almaktadýr. Bunlar glutamat ve<br />
1,5,26<br />
nöropeptidlerdir.<br />
Glutamat; A-delta terminal uçlarýndan ve<br />
motor nöronlara sinaps yapan afferentlerden<br />
26,27<br />
salgýlanan eksitatör bir aminoasittir. Dorsal<br />
boynuz projeksiyon hücrelerinde çok kýsa süreli<br />
veya çok uzun süreli depolarizasyon yaratabilir.<br />
Çok kýsa etkisini, “ligand-gated” Na/K iyonlarýný<br />
açmasý ile, uzun süreli depolarizasyon etkisini N-<br />
Metil, D-Aspartat (NMDA) kullanarak<br />
gerçekleþtirir.<br />
Nöropeptidler; Özellikle C lifleri<br />
eksitasyonu ile oluþurlar ve projeksiyon<br />
hücrelerinde çok yavaþ ve çok uzun süreli<br />
depolarizasyona yol açarlar. Bu nöropeptidler<br />
arasýnda; P maddesi, nörokinin-A, kolesistokinin<br />
ve kalsitonin-gene related peptid (CGRP)<br />
sayýlabilir. C lifleri uçlarýndan birden fazla<br />
27,28<br />
nöropeptid salgýlanabilir.<br />
1,2,5,29<br />
Kapý kontrol teorisi<br />
Wall ve Melzack tarafýndan 1965'te ortaya<br />
atýlmýþtýr. Periferden gelen yoðun afferent<br />
nosiseptif impulslarla eksitan ara nöronlar aktive<br />
olmakta ve bu inhibitör ara nöronu inhibe ederek<br />
ve de projeksiyon nöronunu eksite ederek aðrýlý<br />
impulslarýn santral sinir sistemine geçmesine yol<br />
açmaktadýr. Ancak ayný zamanda A ve B grubu<br />
geniþ myelinli liflerin aktivasyonu ile inhibitör<br />
ara nöronlarý aktive ederek projeksiyon ara<br />
nöronlarýný inhibe etmekte ve aðrýlý sinyallerin<br />
geçiþini durdurmaktadýr. Bu mekanizma TENS<br />
(transkutanöz elektriksel sinir uyarýmý) ve spinal<br />
kord stimulasyonu gibi geniþ çaplý lifleri uyartan<br />
41
Aðrý ve aðrý mekanizmalarýna...<br />
saðaltým yöntemine temel olmuþtur.<br />
Dorsal boynuz geçiþi: Dorsal boynuzda<br />
salýnan substant P'ye ilaveten C lifleri diðer<br />
uyarýcý transmitterleri (glutamat, aspartat,<br />
kalsitonin gen related peptid (CGRP) ve nitrik<br />
8<br />
oksit salar. Nitrik oksitin geçek rolü tam olarak<br />
tanýmlanamamýþtýr fakat diðer pek çok yerlere<br />
ilaveten sinapsýn diðer tarafýnda da üretildiði<br />
bilinmektedir.<br />
Nitrik oksit (NO) aðrý iliþkisi: NMDA<br />
reseptörlerinin aktivasyonu nitrik oksit sentetazý<br />
(NOS) aktive eder ve NO oluþur.<br />
Prostoglandinler ve NO medulla spinaliste<br />
2<br />
uyarýcý aminlerin serbestleþmesini saðlar. Nitrik<br />
oksitin nosiseptif olaylardaki rolü tam olarak<br />
açýða çýkmamýþtýr ve akut nosisepsiyonda çok<br />
önemli deðildir. Ancak kronik aðrý durumlarýnda<br />
NO indüksiyonu önem taþýyabilir ve hücre<br />
ölümünde önemli rol oynayabilir. Nitrik oksitin<br />
aðrý üzerinde bir pozitif feedback mekanizmasý<br />
oluþturduðu düþünülmektedir. Nitrik oksitin<br />
blokajý nöropatik hayvan modellerinde aðrýnýn<br />
29<br />
azalmasýna yol açmaktadýr. Enflamasyonda<br />
olduðu gibi NO'nun aðrýda da rol aldýðý ileri<br />
30<br />
sürülmektedir. Tedesco ve ark. poliartritli rat<br />
modelinde NOS inhibitörlerinin aðrý ve<br />
enflamasyon üzerine olan etkilerini araþtýrdýklarý<br />
çalýþmalarýnda; NO'nun mekanik deðil ama<br />
termal duyu yollarýnda etkili olduðunu ve<br />
uyarýlmýþ NOS aktivasyonunun selektif<br />
inhibisyonunun, oluþturulmuþ enflamasyonu<br />
31<br />
arttýrdýðýný bildirmiþlerdir. Dray , pek çok<br />
mediyatör gibi NO'nun da tümöre baðlý<br />
nosisepsiyonda rolü olduðunu vurgulamýþtýr.<br />
Nitrik oksit, NOS'ýn aktivasyonuyla L-<br />
argininden oluþur. Bu mediyatörün düþük<br />
konsantrasyonlarý hemostatik rol oynarken,<br />
büyük konsantrasyonlarý patolojik olur ve yýkýcý<br />
etki taþýr. Nitrik oksit sentetazýýn inhibitörleri<br />
nöronal, endotelyal isoformlar için farklý<br />
selektivite taþýr, ki bu da onun faydalý veya zararlý<br />
özelliklerini gösterir. Bu sahadaki son geliþmeler<br />
ýþýðýnda NO, enflamatuar hastalýklar, aðrý,<br />
nörolojik hastalýklar, þok, ateroskleroz ve kanser<br />
32<br />
tedavisinde alternatif yöntemler sunabilir.<br />
Temporal sumasyon: Eðer bir uyarý dorsal<br />
boynuzdaki sinapsa 3 dakikadan daha sýk<br />
aralýklarla gelirse, post-sinaptik elektrik deþarj<br />
daha fazla uzar. Bu da aðrýnýn þiddetinde artýþla<br />
sonuçlanýr. Temporal sumasyon, wind-up olarak<br />
2,30<br />
isimlendirilir.<br />
Dorsal boynuz patofizyolojisi: Özellikle<br />
aðrý ýsrarlý olduðunda, nöropatik deðiþiklikler<br />
oluþabilir. Bunlarýn doðasý, oluþtuðu koþullar,<br />
ayný zamanda nasýl önleneceði veya geri<br />
çevrileceði sonraki araþtýrmalarýn odaðý<br />
olmalýdýr.<br />
Primer afferent lifler: Aðrý duyarlýlýðý;<br />
uyarýnýn modeline deðil daha çok afferent liflerin<br />
uyarýlmasýna baðlý gibi gözükmektedir. A-δ<br />
nosiseptörlerinin uyarýlmasý kýsa süreli<br />
iðnelenme (karýncalanma), C liflerinin<br />
aktivasyonu ise kötü lokalize yanma duyusunu<br />
16<br />
oluþturur. Aðrýyla ilgili çalýþmalarda, sadece<br />
nosiseptörlerle ilgili liflerin uyarýlmasý anlamlý<br />
33,34<br />
bulunmuþtur. Diðer liflerin ayný ve yüksek<br />
frekanstaki uyarýsý, hiç bir zaman aðrý duyusuyla<br />
35<br />
sonuçlanmaz. Doku yaralanmasý olmadýðýnda,<br />
afferent nosiseptif liflerin aktivitesi ya çok azdýr<br />
ya da hiç görülmez.<br />
Nosiseptif Dorsal Boynuz Hücre Tipleri;<br />
a. Nosiseptif-spesifik nöronlar: Lamina I ile<br />
daha küçük ve daha derindeki lamina V bir çok<br />
nosiseptif spesifik hücreler taþýr. Bunlar yüksek<br />
eþikli, potansiyel olarak dokuya zarar verici<br />
stimulusa selektif yanýt verirler. Bazýlarý türe özel<br />
(termal veya mekanik uyarana yanýcý tarzda<br />
yanýt) olmasýna raðmen bazýlarý kimyasal<br />
uyarýlara yüksek oranda yanýt yanýnda,<br />
diðerlerine de yanýt verebilir. Alýcý bölgeler<br />
genellikle küçüktür ve deri ile kaslardan oluþur.<br />
Uyarýnýn özelliðinden baðýmsýz olarak nosiseptör<br />
spesifik nöronlardaki aktivite, nosiseptörlerin<br />
uyarýlmasýyla oluþan belirli mesajý saðlar.<br />
36,37<br />
Lamina I'deki diðer önemli hücre tipleri;<br />
1. Termoreseptif soðuk hücreler; zararsýz<br />
soðuk ve ýsýtma ile aktive ve inhibe olurlar.<br />
2. Isý, sýkýþma, soðuk hücreleri, geleneksel<br />
nosiseptif spesifik hücrelerine benzerler fakat<br />
zarar verici soðuk tarafýndan uyarýlýrlar.<br />
b. WDRN (Geniþ-Dinamik-Alan<br />
Nöronlarý): Lamina I'de bir miktar bulunmasýna<br />
raðmen, çoðunluðu derin lamina V ve çevresinde,<br />
1,2,5,25<br />
dorsal boynuz boynunda bulunur. Zararsýz ve<br />
nosiseptif uyarýya yanýt vermesi nedeniyle böyle<br />
isimlendirilmiþtir. Zararlý uyarýya yanýtlarý<br />
maksimaldýr. Bir baþka deyiþle, uyarýyý<br />
yoðunluðunun frekansýna göre deðerlendirirler.<br />
Lamina X, WDR nöronlarýn büyük bölümünü<br />
oluþturur ve yüksek oranda viseral uyarýlarý<br />
içerir.<br />
c. Diðer hücreler: Substantia geletinosa<br />
(lamina II)'deki hücrelerin yanýt özellikleri<br />
farklýdýr. Yüksek oranda süren aktiviteleri ve<br />
küçük alýcý bölgeleri vardýr. Yüksek yoðunluklu<br />
uyarý ile inhibe olan ve nosiseptif uyarýnýn rostral<br />
42
Aydýn<br />
yayýlýmýndan sorumlu hücreler vardýr. Derinin<br />
ayný sahasýna hafif dokunuþ, bu hücreleri aktive<br />
38<br />
eder.<br />
Dorsal Boynuz Nöronlarýnýn Yanýt<br />
16<br />
Özellikleri<br />
Önceleri sadece yüksek eþikli küçük<br />
afferentlerden uyarý alan nöron topluluðu olarak<br />
bilinmelerine raðmen daha büyük kýsmý afferent<br />
konverjans özelliðine sahiptirler.<br />
Lif konverjansý (yakýnlaþmasý): WDR<br />
nöronlarý rutin olarak geniþ myelinli (A β, A δ) ve<br />
myelinsiz C liflerinden uyarý alýrlar. Tek hücreye<br />
konverjans, hücrenin büyük uyarý<br />
yoðunluklarýna düzeltilmiþ yanýt vermesine<br />
olanak saðlar.<br />
Modalite konverjansý: Bir WDR hücresi,<br />
termal ve mekanik uyarana cevap verebilir. Bu<br />
özellik onun uyarýyý mekanoreseptörler (Aβ<br />
ve<br />
A δ) (Aδ<br />
ve C) gibi masum ve zararlý<br />
termoreseptörlerden (A ve C) alabileceðinden<br />
kaynaklanýr. Bu özellik WDR hücresinin,<br />
afferent trafiði entegre etme ve uyarýnýn<br />
yoðunluðunu modalitesinden baðýmsýz olarak<br />
düzenlemesine olanak saðlar.<br />
Organ Konverjansý: Wide dynamic range<br />
hücresi viseral organlar yanýnda deri ve kastan da<br />
uyarý alabilir. Bu özellik deðiþik organ veya<br />
bölgelerin birbirleriyle olan planlanmýþ<br />
somatotopikal konverjansýný organize eder.<br />
Böylece sol torasik spinal kord dorsal boynuz<br />
nöronlarýnýn bazýlarý kol ve omuzdan input<br />
alýrlar. Bu hücreler ayný zamanda koroner damar<br />
ve kaslardan kardiyak afferent input alýrlar. Bu<br />
konverjans koroner iskeminin sol kolda aðrýlý<br />
olarak algýlanmasý ile ilgilidir (viseral yansýyan<br />
aðrý).<br />
2,5,26<br />
Nosiseptif geçiþin spinal modulasyonu<br />
Afferent input ve spinal output arasýnda<br />
duyusal algýlamaya yol açan iliþki vardýr. Inputoutput<br />
illiþkisinin koordinasyonu, bir çok<br />
algýlama tipinin fonksiyonu olarak görülür.<br />
Bazýsý hiperaljezi veya allodini gibi oranda artýþ,<br />
bazýsý da çýktýda azalma ve dolayýsýyla analjezi<br />
oluþturur.<br />
Spinal Yardým: WDR nöronlarýnýn bir<br />
özelliði “wind-up” fenomenidir. WDR<br />
hücrelerinin uyarýlmasý C liflerini aktive ediyorsa<br />
ve uyarý >0.33 Hz ise, hücresel yanýt süre ve<br />
büyüklük bakýmýndan artar. “Wind-up”,<br />
hücrenin uzun sürdürülmüþ parsiyel<br />
depolarizasyonu ve geliþmesiyle deðiþir, bu da<br />
membranýn afferent inputa artan þekilde duyarlý<br />
2,5,26<br />
olmasýna yardýmcý olur.<br />
“WIND-UP”ýn özellikleri : Wind-up<br />
santral duyarlýlýðýn spesifik subtipi olarak<br />
görülür. Wide dynamic range ve NS dorsal<br />
boynuz hücrelerinde girdi-çýktý oranlarýnda<br />
jeneralize artýþ gözlenir. Santral duyarlýlýk, artmýþ<br />
reseptif bölgeyle sonuçlanýr. Dermatomal<br />
alanlardan, önceleri nöronlarý aktive etmeyen<br />
afferent inputlar belirgin yanýt oluþturmaya<br />
baþlar. Ayrýca düþük eþikli taktil uyarýlar, artan<br />
2,24<br />
þekilde effektif olmaya baþlar (allodini).<br />
“Wind-up”ýn farmakolojisi: Bu tip yavaþ,<br />
süregiden uyarýnýn nörokininlerin (özellikle<br />
substant P=SP, EAA, NMDA reseptörlerinden)<br />
tekrar salýnýmýndan oluþtuðu<br />
39,40<br />
düþünülmektedir. N-Metil D- Aspartat<br />
antagonistleri ve nörokinin reseptör 1 (NK),<br />
spesifik antagonistleri SP için major baðlanma<br />
noktasýdýr. Psikofiziksel çalýþmalarda, çoðalmýþ<br />
ikincil aðrý (hiç bir zaman birincil aðrý deðil) veya<br />
ikincil aðrýnýn tabaný NMDA antagonistleri ile<br />
41<br />
tedavi edilememiþtir. Bu morfinin oluþturduðu<br />
redüksiyona ters düþer. Prostoglandin ve nitrik<br />
oksit salan moleküllerin intratekal uygulanmasý<br />
42<br />
aðrýya (allodini ve hiperaljeziye) yol açar. Aydýn<br />
ve<br />
43<br />
Erenmemiþoðlu merkezi etkili<br />
benzodiazepinlerin de sistemik (intraperitoneal)<br />
kullanýmlarýnda hiperaljezi oluþtuðunu<br />
saptamýþlardýr. Siklooksigenaz inhibitörler ve<br />
nitrik oksit sentez inhibitörlerinin uygulanmasý<br />
ise hiperaljezi ve allodiniyi azaltýr.<br />
Siklooksigenaz izoenzimini bloke eden<br />
kortikosteroidlerin antihiperaljezik olduðu<br />
44,45<br />
düþünülmektedir.<br />
NOSÝSEPTÝFÇIKICI SÝSTEMLER<br />
Spinotalamik ve spinoretiküler yol uzun<br />
yýllardýr çok iyi bilinmektedir. Diðer yolaklar<br />
yeni tanýmlanmýþtýr veya uzun yýllar önce<br />
tanýmlanmalarýna raðmen, herkesce yeni<br />
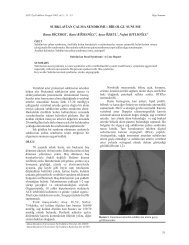
kabullenmiþtir (Þekil 1). Bu yolaklarý þöyle<br />
2,5,6,26<br />
tanýmlayabiliriz.<br />
1. Spino-talamik yol: Nosiseptif uyarý<br />
geldiðinde lamina I, V ve VII. nöronlarýndan kö<br />
ken alýr, orta hattý geçer, anterolateral çýkýcý<br />
sistem içinde ilerler ve spinal kordun karþý<br />
tarafýnda, talamusun VPL (ventral posterolateral)<br />
çekirdeðinde ( 3. nöronda) sonlanýr. Bu nükleus<br />
vücudun özel bölgeleri için bölümlere<br />
ayrýlmýþtýr. Her bölge kendi primer duyusal<br />
korteksinin bölümüne projekte olur. Talamusdan<br />
çýkan uzantýlar da kortekse giderek postsentral<br />
gyrusda sonlanýr. Bu yol aðrýnýn yer, þiddet ve<br />
43
Aðrý ve aðrý mekanizmalarýna...<br />
EK<br />
Þekil 1: Aðrý yollarý ile ilgili bölgeler A: Çýkan aðrý yollarý, B: Ýnen aðrý yollarý (“Aðrý ve Tedavisi” isimli kitaptan alýnmýþtýr)<br />
ARAS: Assendan retiküler aktive edici sistem, ED: Endorfin, EK: Enkefalinerjik,NA: Noradrenalin, 5-HT: 5<br />
Hidroksitriptamin<br />
zaman gibi özellikleri ile birlikte algýlanmasýný<br />
saðlar (arousal). Bu tanýmlayýcý yolak, aðrýnýn<br />
yeri hakkýndaki bilgiyi bilinç düzeyine ulaþtýrýr.<br />
2. Spino-retiküler yol: Anterolateral çýkýcý<br />
sistem içinde ilerler ve çapraz yapmýþ dorsal<br />
boynuz aksonlarýndan oluþur. Bulbus ve ponstaki<br />
retiküler çekirdek gruplarýna uzanýr veya<br />
kollateraller verir. Spinal kordun iki tarafýndaki<br />
sað ve sol talamus intralaminar çekirdeklerine<br />
çýkar. Daha sonra nöronal bilgi singulat gyrusun<br />
ön parçasý (emosyon), amigdal (hafýza ve<br />
emosyon), hipotalamus (emosyon ve emosyona<br />
vasküler yanýt) gibi bir çok beyin bölgesine<br />
ulaþýr. Acý yolaðý olarak isimlendirilir. Korteksi<br />
ve subkortikal yapýlarý (limbik sistem ve<br />
diensefalon) genel bir uyanýklýk içinde tutmak ve<br />
zararlý uyarana karþý genel bir alarm hali<br />
yaratmakla görevlidir.<br />
3. Spino-mezensefalik yol: Dorsal boynuz<br />
lamina I ve V'teki nosiseptif projeksiyon<br />
nöronlarý anterolateral sistem içinde yer alýr ve<br />
44<br />
spino-retiküler yola çok yakýn olarak<br />
mezensefalik periaquaduktal gri cevhere dek<br />
yükselir. Bu beyin kökündeki parabrakial<br />
nükleusa giden yolakla ayný veya ilgili olabilir.<br />
Ön beyindeki parabrakial çekirdek, amigdala,<br />
hipotalamus ve diðer limbik sistem yapýlarýna<br />
projekte olur. Bu yolun periaquaduktaya baðlantý<br />
yapmasý nosisepsiyonda çok önemlidir. Çünkü<br />
burada analjezik etki saðlayan enkefalinerjik<br />
nöronlar vardýr. Periaquaduktal gri cevher<br />
antinosiseptif mekanizmalarýn tetiklendiði en<br />
önemli bölgelerden biridir.<br />
4. Dorsal kolon yolu: Damarsal (visseral)<br />
nosisepsiyonu ve ayný zamanda somatik<br />
dokunma ve pozisyon duyusunu talamusa<br />
46<br />
taþýdýðý sanýlmaktadýr.<br />
5. Spino-hipotalamik yol: Retiküler<br />
formasyonda sinaps yapmayan, yeni<br />
tanýmlanmýþ bir yoldur. Deri, dudak, genital<br />
organlar, gastrointestinal traktus, intrakranial kan<br />
damarý, dil ve korneadan emosyonel önem taþý
Aydýn<br />
16<br />
yan bilgiyi direkt olarak hipotalamusa taþýr.<br />
Santral Duyarlýlýk: Santral duyarlýlýk<br />
kronik aðrýnýn karakteristiðidir. Uzun, devamlý<br />
uyarý ile fizyolojik deðiþiklikler olur. Genlerin<br />
ifadesindeki deðiþiklikler (ör: c-fos ve c-jun),<br />
dorsal boynuzdan kalkan sekonder nöronlar<br />
(spinotalamik ve spinoretiküler yollar) ile oluþur.<br />
Bu gen deðiþikliklerini, enzimlerin volüm ve<br />
tipini oluþan nöropeptidler etkiler. Bunlar<br />
postsinaptik hücrelerde uzun süreçli<br />
deðiþiklikleri indüklerler. Spinal kordun dorsal<br />
boynuzundaki yapýsal reorganizasyon, aðrýnýn<br />
anormal yayýlýmýný açýklayabilir. Spinal kordun<br />
deðiþik seviyelerini içeren, uzak bölgelerden<br />
belirli bir alandan gelen lifler, bilinçlenme<br />
8<br />
yapýlacak nöronlara girer. Volüm iletimi,<br />
nöroaktif moleküllerin hedef bölgelerinden<br />
uzaða ekstrasinaptik yayýlýmýdýr. Bu maddeler<br />
primer afferent nörotransmisyonun uzun süreli<br />
potensiyelizasyonuna ve hem nöronal<br />
uyarýlabilirlik hem de gen ifadesinde kalýcý<br />
deðiþikliklere yol açar. Bu mekanizma yaralanma<br />
sahasýnýn ilerisindeki aðrý algýlanmasýnýn<br />
yayýlýmýný içerebilir. Bir çok supraspinal aðrý<br />
düzenleyici nokta vardýr. Bu noktalar aðrýnýn<br />
47,48<br />
miktarýný artýrabilir veya azaltabilir.<br />
SEREBRALKORTEKS <strong>VE</strong>AÐRI<br />
Son 30 yýldýr supraspinal aðrý<br />
mekanizmalarý hakkýnda Melzac ve Casey'in<br />
teorileri kabul görmektedir. Bu yazarlar, aðrýnýn<br />
duyusal diskriminatif (ayrýmlaþma) ve affektif<br />
(hissi) motivasyonal komponentlerinin uzak<br />
nöral sistemlerle paralel olarak daðýldýðýný<br />
49<br />
bildirmiþlerdir. Özellikle lateral spinotalamik<br />
traktusun, talamusun lateral çekirdeðinin ve<br />
somatosensoryal korteksin, aðrýnýn duyusal<br />
diskriminatif özellikleriyle ilgili olduðunu, buna<br />
ilaveten medial spinotalamik traktusun,<br />
talamusun medial çekirdeðinin ve limbik<br />
sistemle ilgili beyin bölgelerinin aðrýnýn afektifmotivasyonel<br />
bölgeleri olduðunu belirtmiþlerdir.<br />
Deðiþik beyin sahalarýnýn aðrýlý uyaranlarla<br />
aktive olduðu düþünülmektedir. Bu bölgeler;<br />
talamus, putamen ve serebellum gibi subkortikal<br />
bölgeler ve suplementer motor korteks, anterior<br />
singulate korteks, anterior insular korteks gibi<br />
serebral kortikal bölgelerdir.<br />
Bir yüzyýldan fazla zamandýr yapýlan<br />
çalýþmalarda, harap edildiðinde aðrý deneyimi<br />
ortadan kalkan bir beyin bölgesi bulunamamýþtýr.<br />
Fokal beyin harabiyeti, aðrýnýn belli<br />
görünümlerini bozarken, aðrýnýn diðer<br />
komponentleri saklý kalabilir. Beyinde lokalize<br />
aðrý merkezi yoktur. Aðrý, birçok beyin<br />
bölgesince iþleme tabi tutulur.<br />
Talamustan serebral kortekse nosisepsiyon<br />
bilgisini ileten multipl parelel yollar<br />
tanýmlanmýþtýr. Ventroposterolateral (VPL)<br />
nukleus, ventroposterior inferior nükleus (VPI),<br />
posterior ventromedial nükleus (VMPo),<br />
posterior kompleks (Po), sentrolateral nükleus<br />
(CL), parafasiküler nükleus (Pf) ve medial dorsal<br />
nükleus (MD) nosiseptif nöronlarý içeren spinal<br />
50,51<br />
kord bölgelerinden direkt input alýr.<br />
Tek taraflý aðrýlý uyaran hakkýndaki bilgi<br />
talamustan her iki serebral hemisfere direkt<br />
olarak transfer edilmektedir. Alýþýlagelmiþ<br />
bilgilerin aksine, tek taraflý aðrýlý uyarý hem<br />
kontralateral hem de ipsilateral talamusu aktive<br />
52-55<br />
eder. Fonksiyonel görüntüleme çalýþmalarýnda<br />
56<br />
nöronlarýn bilateral aktivasyonu gösterilmiþtir.<br />
Aðrý olayýnda serebral korteksin görevi tam<br />
olarak anlaþýlamamýþtýr. Aðrýyla ilgili olaylarýn<br />
kompleksliði ve beyin alanlarý arasýndaki<br />
baðlantýlara raðmen, nadiren özel beyin<br />
alanlarýnýn birebir aktivasyonunun aðrý<br />
57<br />
deneyimiyle iliþkisi vardýr. Serebrumda aðrý ile<br />
ilgili bölümler; I. ve II. duyusal alanlar, frontal<br />
lob, 9 ve 12. alanlar, posterolateral bölgelerle<br />
beyinin çeþitli bölümlerini birbirine bað<br />
layan assosiyasyon lifleridir. Aðrý olayýndaki<br />
karmaþýk iliþkilerin kýsmen kortikal<br />
mekanizmalarla ortaya çýktýðý ve özellikle frontal<br />
lobun bu üst düzeydeki iþlevlerde rol aldýðý<br />
düþünülmektedir.<br />
KortikalAðrý Merkezi Var mý?<br />
Ne yazýk ki aðrý düþünüldüðünde belirli bir<br />
merkez yoktur.Aðrý yaþam için o kadar önemlidir<br />
ki, yaklaþýk tüm beyin onunla ilgilidir. Aðrýnýn;<br />
bilinç, emosyon ve davranýþla ilgisi vardýr.<br />
Aþaðýdaki kortikal sahalarýn aðrýlý uyaran<br />
sýrasýnda PET (positron emission tomography)<br />
scan ile incelenmesinde aktivite saptanmýþtýr.<br />
Brodmann'ýn doku klasifikasyonu parentez<br />
57<br />
içindeki sahalardýr; duyusal ve motor korteks<br />
alanlarý (1-4), premotor korteks (aðrýnýn<br />
algýlanmasý için) (6), pariyetal korteksin diðer<br />
parçalarý (7, 37-40), frontal korteksin diðer<br />
parçalarý (8-10, 43-47), cingulate korteks (24,<br />
32), insula (14), oksipital korteks (19).<br />
Aðrý; talamus, putamen, kaudate nükleus,<br />
hipotalamus, amigdala, periaquaduktal gri mater,<br />
hipokampus, kýrmýzý nükleus, pulvinar,<br />
45
Aðrý ve aðrý mekanizmalarýna...<br />
serebellumun vermisi gibi subkortikal yapýlara<br />
55<br />
da geçer. Bunlarýn hepsi Dennis Turk'un<br />
“aðrýnýn merkezi temel olarak beyindedir” fikrini<br />
destekler. Aðrý kontrolünde bir baþka merkez<br />
58<br />
yoktur.<br />
ANTÝNOSÝSEPTÝFÝNÝCÝ SÝSTEMLER<br />
Özellikle endojen opioid peptidlerin keþfi<br />
ile aðrýlý uyaranlara karþý spinal ve supraspinal<br />
düzeyde enkefalinerjik ve monoaminerjik bir<br />
inhibisyon varlýðý gösterilmiþtir. Bunlar 3 gruba<br />
ayrýlýrlar (Þekil 1).<br />
1. Mezensefalik periaquaduktal gri<br />
cevherde yer alan enkefalinerjik nöronlardýr.<br />
Bunlar serebral korteks ve hipotalamus ile<br />
baðlantý içindedirler. Muhtemelen hipotalamus<br />
kökenli nöronlar endorfin taþýmaktadýr.<br />
Mezonsefalonda, Sylvius kanalýnýn çevresine<br />
yerleþmiþ nöronlarýn oluþturduðu periaquaduktal<br />
gri cevherden baþlayan yol, bulbustaki retiküler<br />
formasyona giderek nükleus rafe magnus ve<br />
nükleus retikülaris gigantosellularisteki<br />
serotoninerjik nöronlarla sinaps yaparlar.<br />
Böylece diensefalik endorfin ve mezonsefalik<br />
enkefalin nöronlarý bulbustaki serotonin<br />
nöronlarýný uyarýrlar. Buradan kalkan uyarýlar da<br />
m. spinalis arka boynuzu ve trigeminal sinirin<br />
sensoriyal çekirdeðine giderek presinaptik ve<br />
postsinaptik baðlantýlarla inhibisyon<br />
2,5,11<br />
oluþturur. Supraspinal inhibisyondan<br />
2<br />
sorumludurlar.<br />
2. Retiküler formasyonun bazý<br />
çekirdeklerinden baþlayýp, m. spinalis arka<br />
boynuzunda sonlanan noradrenerjik nitelikteki<br />
lifler. Bunlarýn temel nörotransmitteri<br />
noradrenalindir. Bu yollarýn baþlangýcýndaki<br />
opioid reseptörlerin aktivasyonu ile supraspinal<br />
2,5<br />
analjezi elde edilir.<br />
3. Antinosiseptif spinal segmental<br />
mekanizmada özellikle spinal yerleþimli<br />
enkefalinerjik nöronlar rol oynar. Dinorfin<br />
taþýyan nöronlar bu bölgede yoðundur.<br />
Tüm bu monoaminerjik ve enkefalinerjik<br />
antinosiseptif etkiler; hücresel düzeyde, lamina I<br />
ve II'de bulunan nosiseptif projeksiyon nöronlarý<br />
üzerinde<br />
+<br />
K iyonu membran iletkenliðini<br />
arttýrarak ve hiperpolarizasyon oluþturarak<br />
ortaya çýkar. Ayrýca genel bir inhibitör madde<br />
olarak gama amino butirik asit (GABA)'nýn da<br />
antinosiseptif mekanizmalara katýldýðý<br />
düþünülmektedir. Projeksiyon nöronlarý üzerinde<br />
hýzlý ve kýsa süreli inhibisyon, en çok<br />
monoaminerjik transmitterler GABA ve kýsmen<br />
46<br />
de enkefalin ile olmaktadýr. Daha uzun süreli<br />
inhibisyon endorfin, kýsmen enkefalin ve<br />
somatostatin ile oluþmaktadýr. Glisin ve<br />
GABA'nýn medulla spinaldeki segmental aðrý<br />
2<br />
inhibisyonunda önemli rolleri vardýr. Bunlar<br />
dýþýnda somatostatin ve bombesin gibi<br />
5<br />
nöropeptidler de inhibitör etki yapar.<br />
DiðerAðrý Düzenleyen ÝniciYolaklar;<br />
· Korteksten nükleus gracilis ve kuneatusa,<br />
retikülar formasyona, talamusa inenler,<br />
· Periaquaduktal gri cevherden kalkan ve direkt<br />
olarak dorsal boynuza, medullanýn raphe<br />
çekirdeðini geçip ve ardýndan dorsal boynuza<br />
geçenler,<br />
· Lokus seruleus'tan kalkan ve spinal kordun<br />
dorsal boynuzuna geçenler.<br />
Sonuçta çok karmaþýk olan aðrý ve aðrý<br />
fizyolojisine güncel bilgiler ýþýðýnda<br />
yaklaþýlmaya çalýþýldý. Toplumun çok büyük bir<br />
kesimini ilgilendiren aðrý ile baþ edebilmek için<br />
aðrý mekanizmalarýnýn iyi bilinmesi gerekir. Son<br />
yýllarda epeyce yol alýnmasýna karþýn, aðrý ve<br />
fizyopatolojisi konusunda bilinmeyenler<br />
bilinenlerden daha fazladýr. Bu nedenle aðrý<br />
konusunda yapýlan çalýþmalar artarak devam<br />
etmektedir.<br />
KAYNAKLAR<br />
1. Yücel A. Akut aðrý nörofizyolojisi. Hasta kontrollü<br />
analjezi (PCA). Ýstanbul: MER Matbaacýlýk&<br />
Yayýncýlýk, 1997: 5-19.<br />
2. Morgan GE, Mikhail MG. Pain Management. In:<br />
nd<br />
Clinical Anesthesiology, 2 ed. New Jersey: Prenttice-<br />
Hall Interntional, Inc., 1996: 274-316.<br />
3. Merskey HM, Pain terms. Pain 1986; suppl. 3: 215-21.<br />
4. Kayhan Z. Klinik Anestezi. 2. Baský Ýstanbul: Logos<br />
Yayýncýlýk, 1997: 759-87.<br />
5. Ertekin C. Aðrýnýn nöroanatomisi ve nörofizyolojisi.<br />
Aðrý ve tedavisi. Ýbrahim Yegül (ed). Ýzmir:Yapým<br />
Matbaacýlýk, 1993: 1-18.<br />
6. Raj PP. Aðrý taksonomisi. Erdine S (ed). Aðrý, Birinci<br />
baský, Ýstanbul;Alemdar Ofset, 2000: 12-20.<br />
7. Türkoðlu M. Aðrýnýn tanýmlanmasý ve ölçümü. Aðrý ve<br />
tedavisi. Ýbrahim Yegül (ed). Ýzmir:Yapým Matbaacýlýk,<br />
1993: 19-99.<br />
8. Bonica JJ. The Management of Pain,<br />
nd<br />
2 ed.<br />
Philadelphia: Lea & Febriger 1990.<br />
9. Benjamin WJ. Pain Mechanisms: Anatomy,<br />
Physiology and Neurochemistry. In: Raj PP (ed).<br />
th<br />
Practical Management of Pain, 3 ed., Missouri: Mosby<br />
Inc., 2000: 117-45.<br />
10. Aldemir T. Aðrý sendromlarý. Erdine S (ed). Aðrý,<br />
birinci baský, Ýstanbul;Alemdar Ofset, 2000: 714-63.<br />
11. Merskey HM, Bogduk N, Classification of Chronic<br />
nd<br />
Pain, 2 ed., Seattle: IASPPress, 1994: 211-8.<br />
12. Mense S. Nociception from skeletal muscle in relation<br />
to clinical muscle pain. Pain 1993; 54: 241-89.
Aydýn<br />
13. Ness TJ and Gebhart GF. Visceral pain: a review of<br />
experimental studies. Pain 1990; 41: 167-234.<br />
14. Cervero F. Sensory innervation of the viscera:<br />
peripherals basis of visceral pain. Physiol Rev. 1994;<br />
74: 95-138.<br />
15. Dray A and Perkins MN. Bradykinin and inflammatory<br />
pain, trends. Pharmacol Sci 1993; 16: 99-104.<br />
16. Sorkin LS. Basic pharmacology and physiology of<br />
acute pain proccessing. In: Wallace MS, Dunn JS,<br />
Yaksh TL (eds). Anesthesiology Clinics of North<br />
America. Philadelphia: W.B. Saunders Company,<br />
1997: 235-50.<br />
17. Schouenborg J, Sjolund B. First-order nociceptive<br />
synapses in rat are blocked by an amino acid antagonist.<br />
Brain Res 1986; 376: 394-8.<br />
18. Sorkin L, McAdoo DJ. Amino acids and serotonin are<br />
released into the lumbar spinal cord of the anesthesized<br />
cat following intradermal capsaicin injections. Brain<br />
Res 1993; 607: 89-98.<br />
19. Childs A, Evans R, Watkins J: The pharmacological<br />
selectivity of three NMDA antagonists. Eur J<br />
Pharmacol 1988; 145: 81-6.<br />
20. Salt T, Hilkl R. Pharmacological differentiation<br />
between responsesif rat medullary dorsal horn neurons<br />
to noxious mechanical and noxious thermal cutaneous<br />
stimulation. Brain Res 1983; 262: 167-71.<br />
21. Aanonsen L, Wilcox GL. Nociceptive action of<br />
exicitatory amino acids in the mouse: effects of spinally<br />
administered opioids, phencycladine and sigma<br />
agonists. J Pharmacol Exp Ther 1987; 243: 9-19.<br />
22. Raigorodsky G, Urca G. Intrathecal N-methyl-Daspartate(NMDA)<br />
activates both nociceptive and<br />
antinociceptive pathways. Brain Res 1987; 422: 158-<br />
62.<br />
23. O'Brien C, Woolf C, F,tzgerald M, et al. Differences in<br />
the chemical expression of rat primary afferent neurons<br />
which innervate skin, muscle or joint. Neuroscience<br />
1989; 493-502.<br />
24. Casey KL. Pain and central nervous system disease:<br />
The central pain sendroms. Raven press, Newyork<br />
1991.<br />
25. Yaksh TL, Aimone LD. The Central pharmacology of<br />
pain transmission. In: Wall PD, Melzack R (eds).<br />
nd<br />
Textbook of Pain, 2 ed. Edinburg: Churchill<br />
Livingstone, 1989, 181-205.<br />
26. Heavner JE, Willis WD. Pain pathways: Anatomy and<br />
physiology. In: Raj PP (ed). Practical Management of<br />
th<br />
Pain, 3 ed. St Louis: Mosby Inc., 2000; 107-45.<br />
27. Dickenson AH. NMDA receptor antagonits as<br />
analgesics. In: Fields HL, Liebeskind (eds),<br />
Pharmocolgical approaches to the treatment of pain.<br />
Seattle: IASPPress, 1994: 173-87.<br />
28. Price DD, Mao J, Mayer DJ. Central neural<br />
mechanisms of normal and abnormal pain states. In<br />
Fields HL, Liebeskind (eds). Pharmocological<br />
approaches to the Treatment of Pain. Seattle: IASP<br />
Press, 1994: 61-84.<br />
29. Erdine S. Aðrý mekanizmalarý. Erdine S (ed). Aðrý,<br />
Birinci baský, Ýstanbul;Alemdar Ofset, 2000: 20<br />
30. Tedesco LS, Fuseler J, Grisham M, Wolf R, Roerig SC.<br />
Therapeutic administration of nitric oxide synthase<br />
inhibitors reverses hyperalgesia but not inflammation<br />
in a rat model of polyarthritis. Pain 2002; 95: 215-23.<br />
31. DrayA. Neurogenic mechanisms and neuropeptides in<br />
chronic pain. Prog Brain Res 1996; 110: 85-94.<br />
32. Alcaraz MJ, Guillen MI. The nitric oxide related<br />
therapeutic phenomenon: a challenging task. Curr<br />
Pharm Des 2002; 8: 215-31.<br />
33. Price DD. Psychological mechanisms of pain and<br />
analgesia. Seattle: IASPPress, 1999: 48-54.<br />
34. Konietnzny F, Perl E, Trevino D, Light A, Hensel H.<br />
Sensory experiences in man evoked intraneural<br />
eletrical stimulation of intact cutaneous afferent fibers.<br />
Exp Brain Res 1981; 42: 219-22.<br />
35. Valbo A. Sensations evoked from the glabreus skin of<br />
human hand by electrical stimulation of unitary<br />
mechanosensitive afferents. Brain Res 1981; 215: 359-<br />
63.<br />
36. Christensen B, Perl E. Spinal neurons spesifically<br />
excited by noxious or thermal stimuli: Marginal zone<br />
of the dorsal horn. J Neurophysiol 1970; 33; 293-307.<br />
37. Craig A, Kniffki KD. Sphinothalamic lumbosacral<br />
lamina I cells reponsive to skin and muscle stimulation<br />
in the cat. J Physiol 1985; 365: 197-221.<br />
38. Cervero F, Iggo A, Molony V. Supraspinal linkage of<br />
substantia gelatinosa neurones: Effect of descending<br />
impulses. Brain Res 1979; 136: 3512-355.<br />
39. Gerber G, Randic M. Participation of excitatory amino<br />
acids receptors in the slow excitatory synaptic<br />
transmission in the rat spinal cord in vitro. Neurosci<br />
Lett 1989; 106: 220-8.<br />
40. Urban L, Randic M. Slow excitatory transmission in<br />
rat dorsal horn: Possible mediation by peptides. Brain<br />
Res 1984; 290: 336-41.<br />
41. Price D, Mao J, Frenk H, Mayor DJ. The N-methyl-Daspartate<br />
receptor antagonist dextro-methorphan<br />
selectively reduces temporal summation of second pin<br />
in man. Pain 1994; 59: 165-74.<br />
42. Minami T, Nishihara I, Uda R, Ito S, Hyodo M,<br />
Hayaishi O. Involvement of glutamate receptors in<br />
allodynia induced by prostoglandins E2 and F2 alpha<br />
injected int conscious mice. Pain 1994; 57: 225-31.<br />
43. Aydin ON, Erenmemisoglu A. An antinociceptive<br />
effect of the intraperitoneal administration of central<br />
acting drugs in mice.Aðrý 2000; 12: 48-9.<br />
44. Malmberg A, Yaksh T. Hyperalgesia mediated by<br />
spinal glutamate or SP receptors blocked by spinal<br />
cyclooxygenase inhibition. Science 1992; 257; 1276-<br />
9.<br />
45. Radhakrishnan V, Yashpal K, Hui-Chan C, Henry JL.<br />
Implication of anitric oxide synthase mechanism in the<br />
action of substance P: L-NAME blocks the thermal<br />
hyperalgesia induced by endogenous and oxgenous<br />
substance Pin the rat. Eur J Neurosci 1995; 7: 1920-5.<br />
46. Hirshberg RM, Al-Chaer ED, Lawand NB, Westlund<br />
KN, Willis WD. Is there a pathway in the posterior<br />
funiculus that signals visceral pain?<br />
1996;67:291-305.<br />
Pain<br />
47. Hoheisel V, Koch K, Mense S, Functional<br />
reoorganization in rat dorsal horn during experimental<br />
myositis. Pain 1994; 59: 111-8.<br />
48. Mense S, Hoheisel V, Kaske A, Reinert A. Muscle<br />
pain: Basic mechanisms and clinical correllates. In:<br />
Jensen TS, Turner JA, Wiesenfeld-Hallin Z (eds):<br />
th<br />
Proceedings of the 8 World Congress in Pain<br />
Research and Management, Philadelphia: IASP press,<br />
1997; 479-96.<br />
49. Melzac R, Casey KL. Sensory, motivational and<br />
central control determinants of pain. In: Kenshalo DR<br />
(ed). Skin senses. New York: Springfield, IL., 1968:<br />
423-35.<br />
50. Boivie J. An anatomical reinvestigation of termination<br />
47
Aðrý ve aðrý mekanizmalarýna...<br />
of the spinothalamic tract in the monkey. J Comp.<br />
Neurol. 1979; 186: 343-70.<br />
51. Craig AD, Reiman EM, Evans A, Bushnell MC.<br />
Functional imaging of an illusion of pain. Nature 1996;<br />
21: 456-8 (Abstract).<br />
52. Coghill RC. Brain mechanisms supporting the pain<br />
experience: A distributed processing system. In: Max<br />
M (ed). Pain 1999-An Upgrated Review (Refresher<br />
Course Syllabus). Seattle: IASPPress, 1999: 67-77.<br />
53. Casey KL, Minoshima S, Morrow TJ, Koeppe RA.<br />
Comparison of human cerebral activation pattern<br />
during cutaneous warmth, heat pain, and deep cold<br />
pain. J. Neurophysiol. 1996; 76: 571-81.<br />
54. Coghii RC, Talbot JD, Meyer E, Gjedde A, Evans AC,<br />
Bushnell MC, Duncan GH. Distributed processing of<br />
pain and vibration in the human brain. J Neurosci 1994;<br />
14: 4095-108.<br />
55. Iadorola MJ, Berman KF, Zeffir TA, Byas-Smith MG,<br />
Gracely RH, Max MB, Bennet GJ. Neural activation<br />
during acute capsaicin-evoked pain and allodynia<br />
assessed with positron emission tomography. Brain<br />
1998; 121: 931-47.<br />
56. Rainville P, Duncan GH, Price DD, Carrier B, Bushnell<br />
MC. Pain affect encoded in human anterior cingulate<br />
but not somatosensory cortex. Science 1997; 277: 968-<br />
71.<br />
57. Wall PD, The mechanisms by which tissue damage and<br />
pain are related. In Campbell JN (ed) Pain 1996-An<br />
Updated Review, Seattle: IASPPress, 1996: 123-6.<br />
58. Turk D, Rudy TE. IASP taxonomy of chronic pain<br />
syndromes, preliminary assessment of reliability. Pain<br />
1987; 177: 177-89.<br />
YAZIÞMAADRESÝ<br />
Yrd. Doç. Dr. <strong>Osman</strong> <strong>Nuri</strong> AYDIN<br />
Adnan Menderes Üniversitesi Týp Fakültesi<br />
Anesteziyoloji ve Reanimasyon Anabilim Dalý, 09100<br />
Aydýn<br />
Tel : 0 256 2124078<br />
Faks : 0 256 2120146<br />
E-Posta<br />
: onaydin@superonline.com<br />
Geliþ tarihi : 15.10.2001<br />
Kabul Tarihi : 08.04.2002<br />
48