Nachwachsende Rohstoffe als Teil des geschlossenen ... - Gmehling
Nachwachsende Rohstoffe als Teil des geschlossenen ... - Gmehling
Nachwachsende Rohstoffe als Teil des geschlossenen ... - Gmehling
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
<strong>Nachwachsende</strong> <strong>Rohstoffe</strong> <strong>als</strong> <strong>Teil</strong> <strong>des</strong> <strong>geschlossenen</strong> Kreislaufs der Biosphäre<br />
1
Maßnahmen zur Sicherung <strong>des</strong> Energiebedarfs<br />
• Streckung der Ressourcen<br />
– Energieeinsparung (z.B. verbesserte Wärmeisolierung, Elektrogeräte – Standby<br />
abschalten, weniger energieintensive Geräte einsetzen, 3 l-Auto, Brennstoffzelle (H 2 -<br />
Technologie), ...)<br />
– Exploration neuer Lagerstätten<br />
– verfeinerte Abbaumethoden (sek. und tert. Erdölförderung)<br />
• Alternative Energien<br />
– Wasserkraft (z.B. Österreich), Gezeiten<br />
– Sonne (Solarzelle, Aufwindkraftwerk, Hochtemperatursolarwärme)<br />
– Windenergie ( Windparks z.B. auch off-shore)<br />
– Fusion, Kernenergie<br />
– Erdwärme ( Geothermie )<br />
• Alternative <strong>Rohstoffe</strong><br />
– Ölschiefer, Teersände<br />
– nachwachsende <strong>Rohstoffe</strong> (Oleochemie)<br />
– Gas-Hydrate<br />
– Recycling<br />
– evtl. C1-Chemie, Kohle-Oleo-Chemie<br />
große Vorkommen in<br />
Alberta/Kanada (Vorkommen<br />
größer <strong>als</strong> Erdölreserven in<br />
Saudi-Arabien)<br />
2
Abgefackeltes Erdgas<br />
Gesamtmenge an abgefackeltem<br />
Erdgas weltweit:<br />
100 *10 9 m³ pro Jahr<br />
E.Europe<br />
&FSU<br />
6,8%<br />
West.<br />
Europe<br />
3,1%<br />
C&S<br />
America<br />
11,6%<br />
Middle<br />
East<br />
14,7%<br />
Africa<br />
39,3%<br />
Ökonomische Nutzung <strong>des</strong> abgefackelten<br />
Erdgases zur Erzeugung<br />
wertvoller Produkte durch Lurgi´s „gas-<br />
North<br />
America<br />
16,7%<br />
Far East &<br />
Oceania<br />
7,7%<br />
to-chemic<strong>als</strong>“-Technologie<br />
z.B.:<br />
Herstellung von 130 Mt/a Methanol!<br />
in 74 Mega-Methanol (bzw MTP)-Anlagen!<br />
Source:<br />
Energy Information Administration (EIA): ”International Natural Gas Information” 14 Feb 2001, http://www.eia.doe.gov<br />
3
Aufwindkraftwerk<br />
Erzeugte Energie<br />
proportional zur<br />
Intensität der<br />
Sonnenstrahlung,<br />
Kollektorfläche und<br />
Turmhöhe<br />
4
Aufwindkraftwerk<br />
Testphase <strong>des</strong> ersten Aufwindkraftwerks in Manzanares/Spanien von<br />
1986-1989 ( Prof. Jörg Schlaich, Universität Stuttgart )<br />
Leistung 50 kW, Durchmesser Kollektorfläche: 240 m, Kamin: Höhe<br />
195 m, Durchmesser 10 m<br />
der in Sparbauweise errichtete Blechturm bricht 1989 bei einem Orkan<br />
zusammen<br />
2005 soll größtes Aufwindkraftwerk in Australien mit 200 MW Leistung<br />
ans Netz gehen ( Durchmesser Kollektorfläche 5000 m, Turm: Höhe<br />
1000 m, Durchmesser 130 m, Investition ca. 700 Mio. $, geplanter<br />
Baubeginn Ende 2003 )<br />
Ziel Australiens: Erzeugung von jährlich 925 Mio. kWh durch<br />
erneuerbare Energiequellen<br />
5
Hochtemperatursolarenergie<br />
6
Basis, Anteil und Preis der Stromerzeugung<br />
Vergütungssätze* nach dem Erneuerbare-Energien-Gesetz (EEG)<br />
vom 21.7.04 für Neuanlagen:<br />
Wasserkraft: 3.7 – 9.67 ct/kWh<br />
Deponiegas, Klärgas, Grubengas: 6.65 – 9.67 ct/kWh<br />
Biomasse: 3.9 – 17.5 ct/kWh<br />
Geothermie: 7.16 – 15.0 ct/kWh<br />
Windenergie: 5.5 – 8.7 ct/kWh<br />
Solare Energie: 45.7 – 62.4 ct/kWh<br />
(Ziel: Anteil der erneuerbaren Energien an der Stromversorgung auf<br />
min<strong>des</strong>tens 12.5 % bis 2010 ( 20 % bis 2020 ) zu steigern).<br />
*Vergütungssatz in erster Linie abhängig vom Leistungsbereich.<br />
VDI nachrichten 15. Juni 2001<br />
7
Recent and projected trends in population growth<br />
8
Strukturwandel der Rohstoffbasis der Chemischen Industrie<br />
9
Wasserkraft<br />
Shasta Dam, California<br />
America`s second largest dam, Shasta Dam has a spillway three times higher than Niagara<br />
Falls and holds 4.5 million acre-feet of water. Hydroelectricity was the world`s fastest growing<br />
fuel in 1997, and US consumption rose to almost 30 million tons of oil equivalent.<br />
10
Gashydrate<br />
• Fundort: wenige bis 180 Meter unter dem Meeresboden,<br />
bevorzugt in Sedimenten an Kontinentalhängen und in arktischen<br />
Permafrostgebieten *<br />
• Vorkommen vor Nordwesteuropa: ca. 430 000 km 2<br />
• Zusammensetzung: ca. 90% CH 4 und Eis (Clathrate)<br />
• Erforderlich: hoher Druck, niedrige Temperatur, org. Material<br />
• In Gashydraten gespeicherte Menge an Methan übertrifft das in<br />
anderen Kohlenwasserstoff-Reservoirs gespeicherte<br />
Energiepotential um ein Vielfaches *<br />
• 1 m 3 Gashydrat entspricht 163 m 3 CH 4<br />
• Förderung gefährlich aufgrund möglicher Instabilität (geogene<br />
Risikofaktoren, u. a. Klimagas, Kontinentalhangstabilität)<br />
*<br />
http://www.kfa-juelich.de/beo/frgashyd.htm<br />
11
Gashydrate<br />
Gashydrate.cdr<br />
Förderung schwierig:<br />
Temperaturerhöhung<br />
Drucksenkung<br />
Lösungsmittel<br />
12
Gashydrate (Struktur, Vorkommen, ..)<br />
http://www.g-o.de/geo.htm<br />
13
Gashydrat aus der Pipeline ( Petrobras )<br />
14
Förderung der Brennstoffzellenentwicklung<br />
15
Rheinisches Braunkohlerevier<br />
Welche Anstrengung<br />
man bei der Förderung<br />
fossiler Energieträger<br />
auf sich nimmt, soll am<br />
Beispiel<br />
Braunkohleförderung<br />
gezeigt werden.<br />
Umsiedlung Dörfer inkl.<br />
Kirche, Friedhof, ..<br />
Verlegung Autobahn,<br />
Eisenbahnstrecken usw.<br />
Grundwasserprobleme<br />
Großer Aufwand auch<br />
bei der Überführung der<br />
Riesenbagger beim<br />
Wechsel der Abbaustelle<br />
( Entfernung Brücken<br />
usw. )<br />
16
Tagebau<br />
Hambach<br />
17
Schaufelbagger beim Braunkohleabbau<br />
Schaufelbagger:<br />
Höhe 96 m<br />
Länge 225 m<br />
Durchmesser<br />
Schaufelrad 22 m<br />
5 Personen zuständig<br />
Leistung:<br />
240 000 m 3 /Tag<br />
18
Primary energy sources in the United States<br />
since the early 19th century<br />
Chemical Innovation/January 2001<br />
19
Distribution of intercity transportation mileage in the United States<br />
( Chemical Innovation / January 2001 )<br />
20
1700 Chemieunternehmen in Deutschland<br />
Kleine<br />
Unternehmen<br />
49 %<br />
Mittlere<br />
Unternehmen<br />
42 %<br />
< 50 Mitarbeiter<br />
50 bis 499 Mitarbeiter<br />
> 500 Mitarbeiter<br />
Quelle: Destatis, in: Chemische Industrie im Überblick, VCI 2003<br />
Großunternehmen<br />
9 %<br />
21
Die 22 umsatzstärksten deutschen Chemieunternehmen<br />
Rang Firma Umsatz (in Mio. DM)<br />
1 BASF AG 70304<br />
2 Bayer AG 60574<br />
3 Degussa AG 39639<br />
4 Aventis Pharma AG 31471<br />
5 Merck KGaA 13182<br />
6 Boehringer Ingelheim 12126<br />
7 Agfa Gevaert-Gruppe 10288<br />
8 Celanese 10194<br />
9 Fresenius AG 9685*<br />
10 Schering AG 8788<br />
11 Beiersdorf AG 8050<br />
12 Procter & Gamble GmbH 7810<br />
13 Rütgers AG 6118<br />
14 Wacker-Chemie GmbH 5979<br />
15 Wella AG 5523<br />
16 Dynamit Nobel AG 5244<br />
17 Henkel KGaA 4994<br />
18 Dow Deutschland Inc. 4945*<br />
19 Roche Deutschland 4850*<br />
20 B. Braun 4663<br />
21 Clariant GmbH 4370*<br />
22 Solvay Deutschland GmbH 3434<br />
Quelle: VCI, vorläufige Ergebnisse * 1999<br />
22
Sparten der chemischen Industrie<br />
Produktionswerte<br />
1985: 143.8 Mrd. DM<br />
1994: 165.0 Mrd. DM<br />
Anteil der<br />
Sparten<br />
Mrd. DM<br />
Anorganica 9.0 5.5<br />
Organica 26.0 15.8<br />
Düngemittel 1.0 0.6<br />
Kunststoffe 4.5 2.7<br />
Chemiefasern 4.5 2.7<br />
Lacke 8.1 4.9<br />
Seifen und Waschmittel 4.8 2.9<br />
Körperpflegemittel 9.0 5.5<br />
Pharmazeutika 32.8 19.9<br />
TEGEWA* 3.7 2.2<br />
Mineralfarben 6.1 3.7<br />
Pflanzenschutzmittel 2.8 1.7<br />
Photochemie 3.3 2.0<br />
Bautenschutzmittel,<br />
Dachbahnen<br />
In Prozent<br />
3.4 2.1<br />
Klebstoffe 1.7 1.0<br />
Sonstige 23.0 13.9<br />
*Textil-, Papier- und Lederhilfsmittel, Gerb- und Waschrohstoffe<br />
23
Wichtige Produktionsgebiete<br />
(Anteile am Produktionswert in Prozent)<br />
Arzneimittel<br />
Organ. Grundstoffe<br />
Darin enthalten:<br />
Anorg. Grundstoffe<br />
Chemiefasern<br />
7,6<br />
3,7<br />
1,5<br />
1,4<br />
8,6<br />
4,9<br />
20,2<br />
17,9 Kunststoffe u. synth. Kautschuk<br />
16,2<br />
25 Fein- u. Spezialchemikalien<br />
Farben, Lacke, Druckfarben u. Kitte<br />
Farbstoffe u. Pigmente<br />
Fotochemische Erzeugnisse<br />
Klebstoffe u. Gelatine<br />
Wasch- u. Körperpflegemittel<br />
3,8 Pflanzenschutz und Düngemittel<br />
2,4<br />
0 10 20 30<br />
%<br />
24<br />
Quelle: Destatis, in: Chemische Industrie im Überblick, VCI 2003
Anteile ausgewählter Branchen am Umsatz <strong>des</strong><br />
verarbeitenden Gewerbes (2002, in %)<br />
19<br />
13<br />
12<br />
10 10<br />
5<br />
Automobilindustrie Elektrotechnik Maschinenbau Chemie Ernährung Metallerzeugung<br />
Quelle: Destatis<br />
25
Die größten deutschen Unternehmen<br />
26
Größte Chemie-Nationen der Welt 2002<br />
(Nach Umsatz in Milliarden Euro)<br />
500 -<br />
400 -<br />
489<br />
300 -<br />
200 -<br />
100 -<br />
204<br />
132 125<br />
83<br />
0 -<br />
USA<br />
Japan<br />
Deutschland<br />
China<br />
Quelle: Cefic, VCI, in: Chemische Industrie im Überblick, VCI 2003<br />
Frankreich<br />
27
Rank<br />
2001<br />
Global Top 50 Chemical Producers<br />
(Based on the chart showing chemical sales in Chem. Eng. News, July 2002, page 15 – 18)<br />
Rank<br />
2000<br />
Company<br />
Rank<br />
2001<br />
Rank<br />
2000<br />
Company<br />
1 3 Dow Chemical (U.S.)<br />
2 2 DuPont (U.S.)<br />
3 1 BASF (Germany)<br />
4 5 Bayer (Germany)<br />
5 6 TotalFinaElf (France)<br />
6 4 ExxonMobil (U.S.)<br />
7 8 Shell (U.K./Netherlands)<br />
8 17 Degussa (Germany)<br />
9 10 BP (U.K.)<br />
10 9 ICI (U.K.)<br />
11 11 Akzo Nobel (Netherlands)<br />
12 15 Huntsman Corp. (U.S.)<br />
13 14 Mitsui Chemic<strong>als</strong> (Japan)<br />
14 13 Mitsubishi Chemical (Japan)<br />
15 18 Dainippon Ink & Chemic<strong>als</strong> (Japan)<br />
16 16 General Electric (U.S.)<br />
17 21 Henkel (Germany)<br />
18 22 SABIC (Saudi Arabia)<br />
19 20 DSM (Netherlands)<br />
20 12 Sumitomo Chemical (Japan)<br />
21 24 Rhodia (France)<br />
22 26 Air Liquide (France)<br />
23 17 Chevron Phillips (U.S.)<br />
24 29 PPG Industries (U.S.)<br />
25 19 Equistar (U.S.)<br />
Customers of LTP resp. DDBST<br />
26 25 China Petroleum & Chemic<strong>als</strong> (China)<br />
27 30 Clariant (Switzerland)<br />
28 -- Teijin (Japan)<br />
29 37 Air Products & Chemical Corp. (U.S.)<br />
30 43 Formosa Plastics (Taiwan)<br />
31 28 Toray Industries (Japan)<br />
32 23 Syngenta (Switzerland)<br />
33 35 Eastman Chemical (U.S.)<br />
34 45 BOC (U.K.)<br />
35 36 Asahi Kasei (Japan)<br />
36 41 Praxair (U.S.)<br />
37 -- Shin-Etsu (Japan)<br />
38 31 Reliance Industries (India)<br />
39 40 Norsk Hydro (Norway)<br />
40 32 Rohm and Haas (U.S.)<br />
41 38 Solvay (Belgium)<br />
42 42 Ineos Group (U.K.)<br />
43 33 Aventis (France)<br />
44 44 Celanese (Germany)<br />
45 39 Ciba Specialties (Switzerland)<br />
46 34 ENI (Italy)<br />
47 40 Monsanto (U.S.)<br />
48 -- Borealis (Denmark)<br />
49 46 Honeywell (U.S.)<br />
50 47 Lyondell (U.S.)<br />
Members of our UNIFAC consortium<br />
28
Die 30 größten Industrieunternehmen<br />
der Erde<br />
29
Hochschulfinanzierung: Deutschland an der kurzen Leine<br />
30<br />
Aus: Forschung & Lehre 7/2003<br />
S. 346
Top 50 chemical products<br />
31
Ausgewählte Produktionszahlen der Chemischen Industrie Deutschland<br />
1950 - 1990 (in Mio Tonnen)<br />
32
Beschäftigte der chemischen Industrie<br />
VCI - Chemiewirtschaft in Zahlen 2004<br />
*<br />
567668<br />
564878<br />
558730<br />
548834<br />
550321<br />
716734<br />
675000<br />
600000<br />
525000<br />
450000<br />
557033<br />
567126<br />
571802<br />
1980<br />
1981<br />
1982<br />
1983<br />
1984<br />
1985<br />
1986<br />
1987<br />
1988<br />
1989<br />
1990<br />
1991<br />
1992<br />
1993<br />
1994<br />
1995<br />
575310<br />
581958<br />
591895<br />
654769<br />
608705<br />
569998<br />
535896<br />
517531<br />
500546<br />
484639<br />
477613<br />
1966<br />
1997<br />
1998<br />
1999<br />
2000<br />
2001<br />
2002<br />
470308<br />
467029<br />
461713<br />
463314<br />
2003<br />
33<br />
*ab 1991: 16 Bun<strong>des</strong>länder; Veränderungsraten ggü. Vorjahr beziehen sich auf diesen neuen Berichtskreis; Quelle: Destatis
Chemiestatistik<br />
34
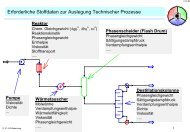
Unterschied zwischen Labor- und technischen Verfahren<br />
I Probleme <strong>des</strong> größeren Maßstabs<br />
II Wirtschaftlichkeit (d.h. Ziel: Veredlung)<br />
1) Reaktionswärme<br />
2) Umweltprobleme<br />
3) Sicherheit<br />
a) Abluft<br />
b) Abwasser<br />
c) Abfall<br />
Unterschiede<br />
Gewinn = Erlös - Herstellkosten > 0<br />
1) Rohstoffkosten (Standortfrage)<br />
2) Energie (Standortfrage)<br />
3) Betriebsweise<br />
4) Kapazität<br />
5) Stoffverbund<br />
6) Apparate<br />
7) Personalkosten<br />
8) .....<br />
•Art der Durchführung ( disk. kontinuierlich )<br />
•Unterschiedliche Edukte<br />
•Unterschiedliche Verfahren<br />
•Unterschiedliche Apparaturen<br />
Erlös = verkaufte<br />
•Problem<br />
Produktmenge<br />
Wärme<br />
* Preis / Mengeneinheit<br />
35
Laborverfahren -<br />
Technische Verfahren<br />
36
Technische Phenolsynthese<br />
37
Vergleich der Phenolverfahren<br />
Verfahren<br />
Phenolausbeute<br />
bezogen auf Benzol Koppelprodukte<br />
Besonderheiten<br />
(bzw. Toluol) (%)<br />
Benzolsulfonatverfahren 90 – 92 Na 2 SO 3 , Na 2 SO 4 Hoher Bedarf an<br />
Hilfsstoffen<br />
Raschig-Hooker-Verfahren 86 – 88<br />
-<br />
Stark korrosive<br />
Reaktionssysteme, große<br />
Kreislaufströme<br />
alkalische Hydrolyse von<br />
Chlorbenzol 80 – 88 * -<br />
hoher Energiebedarf zur<br />
Erzeugung der Hilfsstoffe<br />
(Cl 2 , NaOH)<br />
Cumolverfahren 91 – 93 Aceton -<br />
Toluoloxidation ca. 70 - stark korrosive<br />
Reaktionssysteme<br />
Dehydrierung von<br />
Cyclohexanol/<br />
Cyclohexanon<br />
80 Wasserstoff, wird zur<br />
Hydrierung von Benzol<br />
verwertet<br />
*Der höhere Wert gilt bei Wiedereinsatz <strong>des</strong> gebildeten Diphenylethers<br />
Produktionskapazitäten für Phenol (1993)<br />
Westeuropa USA Japan<br />
Kapazität ( Mio. t/a ) 1.5 1.9 0.9<br />
-<br />
Cumolverfahren (%) 92 96 65<br />
Toluoloxidation (%) 7 2 13<br />
andere<br />
- - 21<br />
Syntheseverfahren (%)<br />
Phenol aus Teer (%) 1 2 1<br />
38
Herstellung Azofarbstoff<br />
39
Vakuumdrehfilter<br />
40
Bandtrockner<br />
41
Mühlen<br />
42
Sprühtrockner<br />
43
Von der Labor- zur Chemieanlage<br />
Capillary<br />
Vacuum<br />
T<br />
Vacuum<br />
Vigreux<br />
column<br />
44
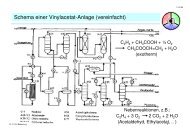
Schema einer typischen Produktionsanlage in der Chemischen Industrie<br />
Anlsched.cdr<br />
Rückführung von A und B<br />
Inerten-<br />
Ausschleusung<br />
Edukte<br />
A + B<br />
Vorbereitung Reaktion Aufarbeitung<br />
Produkte<br />
C + D<br />
A + B<br />
C + D<br />
evtl. auftretende<br />
Nebenprodukte E + F<br />
45
Grundbegriffe*<br />
Umsatz:<br />
X<br />
j<br />
<br />
n<br />
n<br />
n<br />
jo<br />
jo<br />
j<br />
i = Produkt<br />
j = Edukt z.B. Schlüsselkomponente<br />
k = Schlüsselkomponente<br />
Ausbeute:<br />
Y<br />
ik<br />
<br />
n i<br />
n<br />
n<br />
ko<br />
io<br />
<br />
<br />
k<br />
i<br />
Selektivität:<br />
S<br />
ik<br />
<br />
Y<br />
X<br />
ik<br />
k<br />
<br />
n<br />
n<br />
i<br />
ko<br />
n<br />
n<br />
io<br />
k<br />
<br />
<br />
k<br />
i<br />
* Annahme: kontinuierlicher Betrieb<br />
46
Chlorierung von Benzol<br />
Annahme:<br />
Reaktion 1.Ordnung<br />
<br />
k1t<br />
cA<br />
cAoe<br />
k1<br />
k1t<br />
k2<br />
c <br />
<br />
B<br />
cAo<br />
e e<br />
k2<br />
k1<br />
<br />
t<br />
<br />
<br />
c<br />
C<br />
c<br />
Ao<br />
<br />
c<br />
A<br />
<br />
c<br />
B<br />
47
Reaktionswärme:<br />
Wärmeabfuhr:<br />
Vergleich <strong>des</strong> Oberflächen/Volumen-Verhältnisses<br />
von Labor- und technischem Reaktor<br />
<br />
Q R V<br />
h<br />
r dh . . prop.<br />
R R i<br />
<br />
a) 1 dm 3 Rundkolben ( vereinfacht Kugel ) b) Technischer Reaktor, Zylinderform, V R = 10 m 3<br />
V<br />
T<br />
T <br />
dh . . prop A<br />
Q<br />
A<br />
k<br />
w<br />
A<br />
k<br />
.<br />
R<br />
A = r 2 + 2 r h<br />
V = r 2 h<br />
S = 1 h = 2 r<br />
V = 2 r 3 A = 5 r 2<br />
für V = 10 m 3<br />
r = 1.17 m A = 21.4 m 2<br />
3<br />
3 4 3<br />
V10<br />
m r r 0. 06204m<br />
3<br />
A 4<br />
r<br />
2<br />
<br />
A<br />
V<br />
3 m<br />
48.4<br />
r m<br />
2<br />
3<br />
S h r,m A,m 2 A/V, m 2 /m 3<br />
1 2r 1.17 21.4 2.14<br />
2 4r 0.927 24.3 2.43<br />
3 6r 0.810 26.8 2.68<br />
S = Schlankheitsgrad = h/d = h/2r<br />
Extremfall: adiabate Reaktion führt vereinfacht gerechnet ( keine latente Wärme<br />
berücksichtigt ) zu einer Temperaturerhöhung von ca. 425 °C<br />
48
Kühlung<br />
Chlor<br />
teuer!<br />
49
Konzentrationsverlauf und Selektivität von Folgereaktionen<br />
Benzolchlorierung:<br />
A<br />
k 1 k<br />
B <br />
2<br />
C<br />
Fragestellung: bis zu welchem Umsatz Selektivität von 0.9 zu erreichen?<br />
Chlorierung von Benzol ( 40 – 50 °C ): k 1 = 10 k 2<br />
Oxychlorierung von Benzol: k 1 = k 2<br />
Annahme:<br />
Reaktion 1. Ordnung<br />
c<br />
c<br />
c<br />
exp( k t)<br />
A Aa<br />
1<br />
k<br />
<br />
1<br />
c<br />
(exp( k t) exp( k<br />
t))<br />
<br />
Aa<br />
1<br />
k2<br />
k1<br />
<br />
B 2<br />
c<br />
C<br />
<br />
c<br />
Aa<br />
c<br />
A<br />
c<br />
50<br />
B
Konzentrationsverlauf und Selektivität von Folgereaktionen<br />
51
Beispiele für homogene und heterogene Reaktionen<br />
Homogene Reaktionen:<br />
katalyse.cdr, 30.10.01<br />
<br />
Loder<br />
<br />
G<br />
<br />
Loder<br />
<br />
G<br />
<br />
Loder<br />
<br />
G<br />
<br />
Loder<br />
<br />
G<br />
Veresterungen im Rohrreaktor<br />
Heterogene Reaktionen:<br />
<br />
L<br />
<br />
G<br />
Methanchlorierung<br />
im Rührkesselreaktor<br />
<br />
G<br />
Reaktionsgemisch<br />
(Eintritt)<br />
<br />
L<br />
<br />
L<br />
Katalysator<br />
(fest)<br />
<br />
G<br />
<br />
L<br />
<br />
G<br />
Katalysator<br />
(fest)<br />
Wärmeträger<br />
Veresterungen im<br />
Suspensionsreaktor<br />
Chlorierung<br />
von Benzol<br />
in der Blasensäule<br />
Katalytisches<br />
Cracken im<br />
Wirbelbettreaktor<br />
Heterogen katalysierte<br />
Gasreaktionen<br />
Rohrbündelreaktor<br />
52
Kinetik<br />
zu unterscheiden:<br />
Mikrokinetik, d.h. zeitlicher Ablauf der chemischen<br />
Reaktion, ohne Berücksichtigung <strong>des</strong> Einflusses von<br />
Transportprozessen ( Wärme- und Stofftransport )<br />
Reaktionsgeschwindigkeit<br />
[kmol/m 3 h] bzw. [kmol/kg h]:<br />
Makrokinetik, d.h. Beschreibung der Geschwindigkeit<br />
der chemischen Reaktion unter Berücksichtigung der<br />
überlagerten Transportprozesse.<br />
r<br />
i<br />
<br />
1<br />
V<br />
R<br />
dn<br />
dt<br />
i<br />
bzw.<br />
r<br />
i<br />
1<br />
m<br />
Kat.<br />
dn<br />
dt<br />
i<br />
Äquivalentreaktionsgeschwindigkeit:<br />
Katalysator<br />
r<br />
1<br />
<br />
<br />
i<br />
1<br />
V<br />
R<br />
dn<br />
dt<br />
i<br />
r<br />
1 1<br />
<br />
m<br />
i Kat.<br />
dn<br />
dt<br />
i<br />
r <br />
ir<br />
i<br />
r<br />
r<br />
i<br />
i<br />
53
Messungen zur Kinetik in der Rührzelle<br />
0.4<br />
Molenbruch Essigsäure<br />
0.35<br />
0.3<br />
0.25<br />
0.2<br />
0.15<br />
304.2 K<br />
313.5 K<br />
323.1 K<br />
332.2 K<br />
0.1<br />
0 2000 4000 6000 8000 10000<br />
Zeit [s]<br />
r<br />
=<br />
1<br />
ν<br />
i<br />
HOAc + MeOH MeOAc + H 2 O<br />
k -1<br />
<br />
1<br />
m<br />
Kat.<br />
<br />
dn<br />
dt<br />
i<br />
<br />
k<br />
1<br />
a<br />
HOAc<br />
k1<br />
a<br />
MeOH<br />
k<br />
-1<br />
a<br />
MeOAc<br />
a<br />
54<br />
H<br />
2<br />
O
Differentialkreislaufreaktoren<br />
A + B<br />
C + D<br />
diffreak.cdr, 02.11.99<br />
a) äußerer Kreislauf:<br />
c A 0 , c B 0 , ...<br />
dX A, dX B, ...<br />
V 0<br />
b) innerer Kreislauf:<br />
c A 0 , c B 0 , ...<br />
dX A , dX B, ...<br />
für T = konstant:<br />
i A B C D<br />
r c c c c<br />
m Kat<br />
. . . . .<br />
. . . . .<br />
. . . . .<br />
. . . . .<br />
. . . . .<br />
V 0<br />
m Kat<br />
55
Integralmethode<br />
r<br />
A + B<br />
<br />
f(ci)<br />
1<br />
A<br />
1<br />
V<br />
R<br />
<br />
dn<br />
dt<br />
c<br />
c<br />
A<br />
<br />
Ao<br />
A<br />
dc<br />
f c<br />
<br />
A<br />
i<br />
<br />
<br />
C<br />
k(T)f (c<br />
i<br />
)<br />
für V R = konstant:<br />
r <br />
dc<br />
dt<br />
A<br />
<br />
k(T)f (c<br />
i<br />
)<br />
cA<br />
cA 2<br />
cAcB<br />
c<br />
ln<br />
c<br />
A<br />
Ao<br />
A<br />
1 <br />
c<br />
c<br />
Bo<br />
...... ......<br />
1<br />
<br />
1<br />
c<br />
c<br />
Ao<br />
Ao<br />
c<br />
ln<br />
c<br />
B<br />
Bo<br />
c<br />
c<br />
Ao<br />
A<br />
56
Differentialmethode<br />
57
Differentialmethode<br />
58
Zusammenfassung<br />
kinetik.cdr, 30.10.2000<br />
c<br />
Rührkesselreaktor:<br />
Differentialreaktor:<br />
t cA<br />
dc A/dt A<br />
c A<br />
0 cA c A<br />
dX A<br />
: :<br />
1 :<br />
: :<br />
: :<br />
c A<br />
0<br />
dc /dt A<br />
c A<br />
t<br />
dc<br />
r = - A<br />
= k · f(c ) = k · c<br />
dt<br />
Steigung k<br />
c A<br />
n<br />
c A<br />
<br />
dc<br />
- A<br />
c<br />
n<br />
A<br />
c A<br />
0<br />
<br />
A A A n = ln k + n·ln c A<br />
= k · dt = k·t<br />
ln -<br />
dc A<br />
dt<br />
für n = 1 folgt: ln<br />
ln<br />
c<br />
0<br />
A<br />
c A<br />
c<br />
0<br />
A<br />
c A<br />
= k·t<br />
dc<br />
ln - A<br />
dt<br />
tan = k<br />
ln k<br />
tan = n<br />
t<br />
ln<br />
c A<br />
59
Bestimmung der Aktivierungsenergie<br />
k i<br />
[mol*g -1 *s -1 ]<br />
425<br />
213<br />
0.000182<br />
0.000091<br />
1/T [1/K]<br />
0 0.001 0.002 0.003 0.004<br />
k<br />
0<br />
1 = 114000 mol*g -1 *s -1<br />
E A,1 = 52.2 kJ*mol -1<br />
k -1<br />
0<br />
= 13100 mol*g -1 *s -1<br />
E A,-1 = 55.6 kJ*mol -1<br />
10<br />
8<br />
6<br />
4<br />
2<br />
0<br />
-2<br />
-4<br />
-6<br />
-8<br />
-10<br />
-12<br />
ln(ki)<br />
ln<br />
<br />
0<br />
k ln k <br />
i<br />
k1<br />
HOAc + MeOH MeOAc + H 2 O<br />
k -1<br />
i<br />
<br />
E<br />
A,i<br />
R<br />
<br />
1<br />
T<br />
1124<br />
1000<br />
T = 124 K<br />
1/T [K]<br />
310<br />
300<br />
T = 10 K<br />
-14<br />
60
Selektivität für Folgereaktionen<br />
61
Berechnung <strong>des</strong> Konzentrationsverlaufs<br />
der Folgereaktion mit<br />
MS-Excel<br />
A B C D E F G H<br />
0.<br />
3 Zeitschritt 0,10 t ca cb cc<br />
4 k1 1,00 0,0000 1,0000 0,0000 0,0000<br />
5 k2 1,01 0,1000 0,9048 0,0904 0,0047<br />
6 caa 1,00 0,2000 0,8187 0,1636 0,0177<br />
7 0,3000 0,7408 0,2219 0,0373<br />
8<br />
=E4+$C$3<br />
0,4000 0,6703 0,2676 0,0621<br />
9 0,5000 0,6065 0,3025 0,0910<br />
Eingabebereich<br />
10 0,6000 0,5488 0,3283 0,1229<br />
=$C$6*EXP(-$C$4*E4)<br />
11 0,7000 0,4966 0,3464 0,1570<br />
12 0,8000 0,4493 0,3580 0,1926<br />
13 0,9000 0,4066 0,3643 0,2292<br />
14 1,0000 0,3679 0,3660 0,2661<br />
15 1,1000 0,3329 0,3642 0,3030<br />
=$C$6*($C$4/($C$5-$C$4)*(EXP(-$C$4*E4)-EXP(-$C$5*E4)))<br />
16 1,2000 0,3012 0,3593 0,3395<br />
17 kopieren 1,3000 0,2725 0,3520 0,3755<br />
=$C$6-F4-G4<br />
18 1,4000 0,2466 0,3428 0,4106<br />
19 1,5000 0,2231 0,3322 0,4447<br />
20 Folgereaktion1,6000 0,2019 0,3205 0,4776<br />
21 1,7000 0,1827 0,3079 0,5094<br />
22 1,0<br />
1,8000 0,1653 0,2949 0,5398<br />
23 0,9<br />
1,9000 0,1496 0,2815 0,5689<br />
24 2,0000 0,1353 0,2680 0,5967<br />
0,8<br />
ca<br />
25 2,1000 0,1225 0,2545 0,6231<br />
0,7<br />
cb<br />
26 2,2000 0,1108 0,2411 0,6481<br />
0,6<br />
cc<br />
27 2,3000 0,1003 0,2280 0,6718<br />
28 0,5<br />
2,4000 0,0907 0,2151 0,6942<br />
29 0,4<br />
2,5000 0,0821 0,2027 0,7152<br />
30 0,3<br />
2,6000 0,0743 0,1906 0,7351<br />
31 0,2<br />
2,7000 0,0672 0,1790 0,7538<br />
32 2,8000 0,0608 0,1679 0,7713<br />
0,1<br />
33 2,9000 0,0550 0,1573 0,7877<br />
0,0<br />
34 3,0000 0,0498 0,1471 0,8031<br />
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 5,0<br />
35 3,1000 0,0450 0,1375 0,8174<br />
36<br />
Zeit t<br />
3,2000 0,0408 0,1284 0,8309<br />
37 3,3000 0,0369 0,1197 0,8434<br />
38 3,4000 0,0334 0,1116 0,8551<br />
39 exp( t)<br />
A<br />
<br />
Aa<br />
<br />
1<br />
3,5000 0,0302 0,1039 0,8659<br />
40 3,6000 0,0273 0,0966 0,8761<br />
41 3,7000 0,0247 0,0898 0,8855<br />
42 k<br />
3,8000 0,0224 0,0834 0,8942<br />
1<br />
43 c<br />
3,9000 0,0202 0,0774 0,9023<br />
B<br />
cAa( (exp( k1t)<br />
exp( k2t)))<br />
44 k<br />
4,0000 0,0183 0,0718 0,9099<br />
2<br />
k1<br />
45 4,1000 0,0166 0,0666 0,9169<br />
46 4,2000 0,0150 0,0617 0,9233<br />
47 4,3000 0,0136 0,0571 0,9293<br />
c<br />
48 C<br />
cAa<br />
cA<br />
cB<br />
4,4000 0,0123 0,0528 0,9349<br />
49 4,5000 0,0111 0,0489 0,9400<br />
50 Dr. J. Rarey, 27.10.98 4,6000 0,0101 0,0452 0,9448<br />
62
Input: experimentelle Daten <strong>als</strong> f(t)<br />
c<br />
c<br />
c<br />
exp( k t)<br />
A Aa<br />
1<br />
k<br />
<br />
1<br />
c<br />
(exp( k t) exp( k<br />
t))<br />
<br />
Aa<br />
1<br />
k2<br />
k1<br />
<br />
B 2<br />
63
Simplex-Nelder-Mead-Methode<br />
z.B.:<br />
F =<br />
<br />
i<br />
Komp<br />
j<br />
Daten<br />
c c 2<br />
i,j,ber<br />
i,j,exp<br />
Nelder J.A., Mead R., Comp. J. 7,308 (1965)<br />
Simplex2g.cdr<br />
64
Komplexes<br />
Reaktionsnetzwerk<br />
A<br />
k 1<br />
k 2<br />
B<br />
B<br />
k 3<br />
C<br />
A<br />
k 4<br />
D<br />
65
Reaktionskinetik<br />
Definition der Reaktionsgeschwindigkeit:<br />
r<br />
i<br />
<br />
1<br />
V<br />
R<br />
dn<br />
dt<br />
i<br />
mol<br />
3<br />
hm<br />
<br />
<br />
<br />
bzw.<br />
r<br />
'<br />
i<br />
<br />
1<br />
m<br />
Kat.<br />
dn<br />
dt<br />
i<br />
mol<br />
<br />
hkg<br />
Äquivalentreaktionsgeschwindigkeit:<br />
r<br />
r 1 1 dn<br />
i<br />
i mol <br />
<br />
3<br />
v v V dt hm<br />
<br />
<br />
i<br />
i<br />
R<br />
r<br />
1<br />
v<br />
' 1<br />
<br />
i<br />
i<br />
m<br />
Kat.<br />
dn<br />
dt<br />
i<br />
mol<br />
<br />
hkg<br />
Allgemeiner reaktionskinetischer Ansatz:<br />
r<br />
<br />
f<br />
( T)<br />
f2<br />
( c<br />
1 i<br />
k <br />
k<br />
o<br />
e<br />
)<br />
E<br />
A<br />
RT<br />
m i<br />
c i<br />
benötigt:<br />
<strong>Teil</strong>ordnungen<br />
Stoßfaktor<br />
Aktivierungsenergie<br />
Gesamtordnung<br />
m i<br />
k o<br />
E A<br />
m=m i<br />
66
Ermittlung der kinetischen Parameter (m i , k o, E A )<br />
1) Integralmethode<br />
dc i<br />
dt<br />
c<br />
<br />
c o<br />
dc<br />
f(<br />
c)<br />
kf(c)<br />
kt<br />
c<br />
<br />
c o<br />
dc<br />
f(<br />
c)<br />
ln<br />
<br />
3) Numerische Verfahren<br />
(z.B. Lineare Regression)<br />
dc <br />
dt<br />
dc<br />
dt<br />
A<br />
A<br />
kc<br />
a<br />
A<br />
c<br />
b<br />
B<br />
<br />
lnk<br />
alnc<br />
<br />
A<br />
blnc<br />
B<br />
<br />
Y = a o + a 1 x 1 + a 2 x 2<br />
2) Differentialmethode<br />
a)<br />
dc<br />
i<br />
r <br />
dt<br />
A<br />
m<br />
r kc A<br />
kf(c)<br />
P<br />
b) ln(r ) = lnk + mlnc A<br />
4) Ermittlung von k o<br />
und E A<br />
Arrhenius:<br />
k k<br />
o<br />
lnk<br />
lnk<br />
e<br />
o<br />
<br />
E<br />
A<br />
RT<br />
E<br />
A<br />
RT<br />
67
Messungen zur Kinetik in der Rührzelle<br />
0.4<br />
Molenbruch Essigsäure<br />
0.35<br />
0.3<br />
0.25<br />
0.2<br />
0.15<br />
304.2 K<br />
313.5 K<br />
323.1 K<br />
332.2 K<br />
0.1<br />
0 2000 4000 6000 8000 10000<br />
Zeit [s]<br />
r<br />
=<br />
1<br />
ν<br />
i<br />
HOAc + MeOH MeOAc + H 2 O<br />
k -1<br />
<br />
1<br />
m<br />
Kat.<br />
<br />
dn<br />
dt<br />
i<br />
<br />
k<br />
1<br />
a<br />
HOAc<br />
k1<br />
a<br />
MeOH<br />
k<br />
-1<br />
a<br />
MeOAc<br />
a<br />
68<br />
H<br />
2<br />
O
Molenbrüche (ideal) - Aktivitäten (UNIQUAC)<br />
k 1<br />
HOAc + MeOH MeOAc + H 2 O<br />
k -1<br />
ln ki [mol*g -1 *s -1 ]<br />
Molenbrüche (ideal)<br />
Aktivitäten (UNIQUAC)<br />
-7<br />
-7<br />
-8<br />
-8<br />
k 1 -9<br />
-9<br />
-10<br />
-10<br />
k -1 -11<br />
k -1<br />
-11<br />
-12<br />
-12<br />
-13<br />
0.0029 0.003 0.0031 0.0032 0.0033<br />
1/T [1/K]<br />
1/T [1/K]<br />
ln ki [mol*g -1 *s -1 ]<br />
0.0029 0.003 0.0031 0.0032 0.0033<br />
, Hydrolyse vermessen , Veresterung vermessen<br />
k 1<br />
69
Heiratsvermittlerin<br />
70
Katalyse Absenkung der Aktivierungsenergie E A<br />
E A,Kat<br />
Aktivierungsenergie.cdr<br />
E<br />
E A<br />
A<br />
B<br />
Heiratsvermittlerin<br />
A<br />
B<br />
Reaktionskoordinate<br />
71
Vergleich von homogener und heterogener Katalyse<br />
Homogene<br />
Katalyse<br />
Heterogene<br />
Katalyse<br />
Aktivität (bezogen auf den Metallgehalt) hoch unterschiedlich<br />
Selektivität hoch unterschiedlich<br />
Reaktionsbedingungen mild rauh<br />
Katalysatorstandzeiten unterschiedlich lang<br />
Empfindlichkeit gegenüber Katalysatorgiften niedrig hoch<br />
Diffusionsprobleme keine können von<br />
Bedeutung sein<br />
Katalysatorrückführung teuer nicht nötig<br />
sterische und elektronische<br />
Katalysatoreigenschaften<br />
einstellbar?<br />
mechanistische Interpretation<br />
möglich<br />
möglich in<br />
wenigen Fällen<br />
nicht möglich<br />
mehr oder weniger<br />
unmöglich<br />
*(a) Private Mitteilung, Nachr. Chem. Tech. Lab. 1979, 27, 257; (b) J. Falbe, H. Bahrmann, Chem. Zeit 1981, 15, 37; W. Keim in<br />
Industrial Applications of Homogeneous Catalysis, D. Reidel, Dordrecht, 1988.<br />
72
Einige Meilensteine der Katalysatorentwicklung<br />
73
Catalyst Suppliers offer tailor made solutions<br />
by a range of Catalysts<br />
74
Stofftransport und Reaktion<br />
E<br />
E A<br />
A<br />
A<br />
B<br />
E A,Kat<br />
ln k<br />
unkatalysiert (Steigung: E A /R)<br />
StofftransportundReaktion.cdr<br />
1.5<br />
Filmdiffusionshemmung (D ~ T )<br />
Porendiffusionshemmung<br />
(Steigung: E /2R)<br />
A,Kat<br />
B<br />
Mikrokinetik<br />
(Steigung: E<br />
A,Kat<br />
/R)<br />
Reaktionskoordinate<br />
1 / T<br />
(1a) Filmdiffusion<br />
(1b) Porendiffusion<br />
(2) Adsorption<br />
(3) Oberflächenreaktion<br />
(4) Desorption<br />
(5a) Porendiffusion<br />
(5b) Filmdiffusion<br />
1a<br />
5b<br />
5a<br />
1b<br />
äußere<br />
Oberfläche<br />
2-4<br />
Grenzschicht<br />
innere<br />
Oberfläche<br />
75
Zu berücksichtigender Stoff- und Wärmetransport bei heterogenen<br />
Reaktionen<br />
Stofftransport_Kat.cdr<br />
äußere<br />
Oberfläche<br />
p A<br />
Gas-Flüssig<br />
Grenzfläche<br />
p A,i<br />
Oberfläche <strong>des</strong><br />
Katalysator<br />
5b<br />
1a<br />
5a<br />
1b<br />
2-4<br />
innere<br />
Oberfläche<br />
c A,l<br />
c A,i<br />
c A,s<br />
flüssige Phase<br />
Gasfilm Flüssigkeitsfilm<br />
Film über dem<br />
Katalysator<br />
Drei-Phasen-Suspensionsreaktor<br />
(1a)<br />
(1b)<br />
(2)<br />
(3)<br />
(4)<br />
(5a)<br />
(5b)<br />
Grenzschicht<br />
Filmdiffusion<br />
Porendiffusion<br />
Adsorption<br />
Oberflächenreaktion<br />
Desorption<br />
Porendiffusion<br />
Filmdiffusion<br />
76