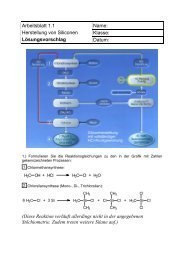
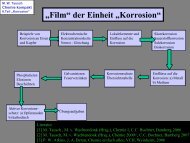
Simulation der „Zementation“ - Chemie und ihre Didaktik, Universität ...
Simulation der „Zementation“ - Chemie und ihre Didaktik, Universität ...
Simulation der „Zementation“ - Chemie und ihre Didaktik, Universität ...
- Keine Tags gefunden...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Experiment 6<br />
<strong>Simulation</strong> <strong>der</strong> Zementation<br />
<strong>Simulation</strong> <strong>der</strong> <strong>„Zementation“</strong><br />
Zeitbedarf für die Versuchsdurchführung: ca. 30 Min.<br />
Geräte:<br />
Magnetrührer mit Magnetrührstäbchen <strong>und</strong> Heizfunktion<br />
Thermometer<br />
Becherglas (600 ml - Weithals)<br />
Trichter mit Filterpapier<br />
Reagenzglas<br />
Nutschapparatur / Filter<br />
Pipette<br />
Spatel<br />
Chemikalien:<br />
Zinksulfat-Lösung aus Experiment 4<br />
Zinkstaub,<br />
Zn, R10-15, S7/8-43<br />
Dimethylglyoxim,<br />
C 4 H 8 N 2 O 2 , Xn, R22<br />
Methanol,<br />
CH 3 OH, F, T, R11-23/24/25-39/23/24/25, S7-16-36/37-45<br />
Ammoniak,<br />
NH 3 , T, N, R10-23-34-50, S9-16-26-36/37/39-45-61<br />
tri-Natriumcitrat-Dihydrat,<br />
C 6 H 5 Na 3 O 7 • 2 H 2 O<br />
Versuchsaufbauskizze:<br />
a) Reaktionsapparatur<br />
Thermometer<br />
Zinkstaub<br />
pH-Elektrode<br />
Becherglas<br />
pH-Anzeige<br />
Zinksulfat-<br />
Lösung 1 14<br />
(nach <strong>der</strong> Eisen-<br />
Mangan-Fällung)<br />
Magnetrührer<br />
1
Experiment 6<br />
<strong>Simulation</strong> <strong>der</strong> Zementation<br />
b) Nutschapparatur<br />
Becherglas mit<br />
Reaktionsgemisch<br />
Büchner-<br />
Trichter<br />
Wasserstrahlpumpe<br />
Saugflasche<br />
Zinksulfat-<br />
Fertiglauge<br />
Durchführung:<br />
Das Filtrat aus Experiment 4 wird auf 60-65°C auf <strong>der</strong> Heizplatte erwärmt <strong>und</strong> gerührt. Nach<br />
Erreichen <strong>der</strong> Temperatur werden 7 g Zinkstaub zugegeben. Die Lösung wird 10 Minuten bei<br />
60-65°C stark gerührt.<br />
Danach werden weitere 3 g Zinkstaub zugegeben. Nach weiteren 10 Minuten wird eine Probe<br />
(Volumen etwa 5 ml) für den Nickel-Nachweis gezogen <strong>und</strong> in ein Reagenzglas filtriert.<br />
Zur Probe für den Nickel-Nachweis werden 3ml ammoniakalische Natriumcitrat-Lösung <strong>und</strong><br />
1,5 ml 1%ige methanolische Dimethylglyoxim-Lösung gegeben. Falls eine Rotfärbung zu<br />
verzeichnen ist, müssen dem Reaktionsgemisch nochmals 3 g Zinkstaub zugefügt <strong>und</strong> nach 5<br />
Minuten wie<strong>der</strong> eine Probe „analysiert“ werden.<br />
Wenn die Probe keine Rotfärbung zeigt, wird das Reaktionsgemisch abgenutscht.<br />
Das Filtrat wird für die folgenden Versuche verwendet.<br />
2
Experiment 6<br />
<strong>Simulation</strong> <strong>der</strong> Zementation<br />
Beobachtung:<br />
Nach Zugabe des Zinkstaubes fällt sofort ein schwarzer Nie<strong>der</strong>schlag aus <strong>und</strong> es ist eine<br />
leichte Gasentwicklung zu verzeichnen.<br />
Nach dem Abnutschen ist die erhaltene Lösung leicht weißlich trübe.<br />
Deutung:<br />
Der Zinkstaub reagiert in einer Redoxreaktion mit den Ionen von edleren Metallen, die sich<br />
noch in <strong>der</strong> Lösung befinden. Außerdem wird Wasserstoff freigesetzt.<br />
Es finden folgende Reaktionen statt:<br />
Cu 2+ + Zn Cu ↓ + Zn 2+<br />
Pb 2+ + Zn Pb ↓ + Zn 2+<br />
Ni 2+ + Zn Ni ↓ + Zn 2+<br />
Cd 2+ + Zn Cd ↓ + Zn 2+<br />
Zn + H 2 SO 4 ZnSO 4 + H 2 ↑<br />
Der größte Teil <strong>der</strong> Pb 2+ -Ionen ist schon im Versuch „<strong>Simulation</strong> <strong>der</strong> Anteigrührwerke“ als<br />
schwerlösliches Bleisulfat ausgefällt worden. Die aufgr<strong>und</strong> <strong>der</strong> Restlöslichkeit im<br />
Reaktionsgemisch verbliebenen Pb 2+ -Ionen werden bei <strong>der</strong> Zementation zu elementarem Blei<br />
reduziert (vgl. Experiment 2).<br />
Überschüssiges Kaliumpermanganat, das sich von <strong>der</strong> Eisen-Mangan-Fällung noch in <strong>der</strong><br />
Lösung befindet, wird durch den entstehenden Wasserstoff zu Mangandioxid reduziert:<br />
2 KMnO 4 + 3 H 2 + H 2 SO 4 2 MnO 2 ↓ + 4 H 2 O + K 2 SO 4<br />
Die Nachweisreaktion mit Dimethylglyoxim findet wie folgt statt:<br />
Ni 2+ + C 4 H 7 N 2 O 2 [Ni(C 4 H 7 N 2 O 2 ) 2 ] 2+<br />
rot<br />
3
Experiment 6<br />
<strong>Simulation</strong> <strong>der</strong> Zementation<br />
Die Struktur des Nickeldimethylgyoxim-Komplexes sieht wie folgt aus:<br />
) 1<br />
Es handelt sich dabei um einen sogenannten Chelatkomplex (lat.: chelae = Scheren (von<br />
Krebstieren)), bei dem das Zentralatom von einem mehrzähnigen Liganden aufgr<strong>und</strong> von<br />
Wechselwirkungen mit einsamen Elektronenpaaren o<strong>der</strong> mit Elektronenlücken „scherenartig“<br />
eingeschlossen wird.<br />
Der systematische Name lautet „Bis(2,3-butandion-dioximato)nickel“.<br />
Entsorgung:<br />
Die Lösung muss, soweit sie nicht für die folgenden Versuche verwendet wird, dem<br />
Schwermetallabfall zugeführt werden.<br />
1 Aus: „CD Römpp <strong>Chemie</strong> Lexikon“, Vers. 1.0, Stuttgart/ New York: Georg Thieme Verlag, 1995, Stichwort<br />
„Chelate“<br />
4