Versuch 2.2.1
Versuch 2.2.1
Versuch 2.2.1
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
2. Eliminierungsreaktionen www.ioc-praktikum.de<br />
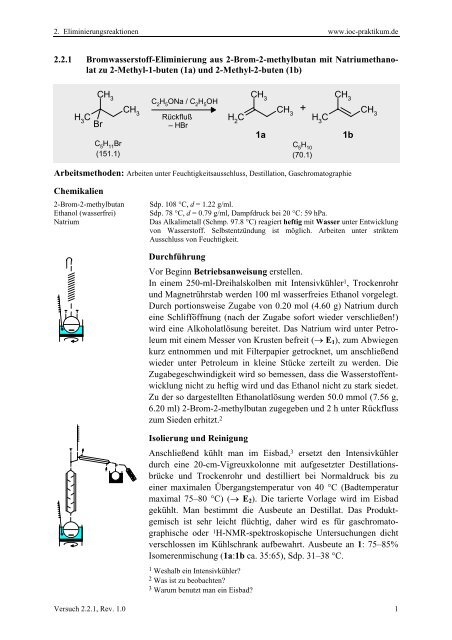
<strong>2.2.1</strong> Bromwasserstoff-Eliminierung aus 2-Brom-2-methylbutan mit Natriumethanolat<br />
zu 2-Methyl-1-buten (1a) und 2-Methyl-2-buten (1b)<br />
CH 3<br />
CH<br />
H 3<br />
C<br />
3<br />
Br<br />
C 5<br />
H 11<br />
Br<br />
(151.1)<br />
C 2<br />
H 5<br />
ONa / C 2<br />
H 5<br />
OH<br />
Rückfluß<br />
– HBr<br />
+<br />
CH 3<br />
CH 3<br />
CH<br />
H 2<br />
C<br />
3<br />
CH<br />
H 3<br />
C<br />
3<br />
1a<br />
C 5<br />
H 10<br />
(70.1)<br />
1b<br />
Arbeitsmethoden: Arbeiten unter Feuchtigkeitsausschluss, Destillation, Gaschromatographie<br />
Chemikalien<br />
2-Brom-2-methylbutan<br />
Ethanol (wasserfrei)<br />
Natrium<br />
Sdp. 108 °C, d = 1.22 g/ml.<br />
Sdp. 78 °C, d = 0.79 g/ml, Dampfdruck bei 20 °C: 59 hPa.<br />
Das Alkalimetall (Schmp. 97.8 °C) reagiert heftig mit Wasser unter Entwicklung<br />
von Wasserstoff. Selbstentzündung ist möglich. Arbeiten unter striktem<br />
Ausschluss von Feuchtigkeit.<br />
Durchführung<br />
Vor Beginn Betriebsanweisung erstellen.<br />
In einem 250-ml-Dreihalskolben mit Intensivkühler 1 , Trockenrohr<br />
und Magnetrührstab werden 100 ml wasserfreies Ethanol vorgelegt.<br />
Durch portionsweise Zugabe von 0.20 mol (4.60 g) Natrium durch<br />
eine Schlifföffnung (nach der Zugabe sofort wieder verschließen!)<br />
wird eine Alkoholatlösung bereitet. Das Natrium wird unter Petroleum<br />
mit einem Messer von Krusten befreit (→ E 1 ), zum Abwiegen<br />
kurz entnommen und mit Filterpapier getrocknet, um anschließend<br />
wieder unter Petroleum in kleine Stücke zerteilt zu werden. Die<br />
Zugabegeschwindigkeit wird so bemessen, dass die Wasserstoffentwicklung<br />
nicht zu heftig wird und das Ethanol nicht zu stark siedet.<br />
Zu der so dargestellten Ethanolatlösung werden 50.0 mmol (7.56 g,<br />
6.20 ml) 2-Brom-2-methylbutan zugegeben und 2 h unter Rückfluss<br />
zum Sieden erhitzt. 2<br />
Isolierung und Reinigung<br />
Anschließend kühlt man im Eisbad, 3 ersetzt den Intensivkühler<br />
durch eine 20-cm-Vigreuxkolonne mit aufgesetzter Destillationsbrücke<br />
und Trockenrohr und destilliert bei Normaldruck bis zu<br />
einer maximalen Übergangstemperatur von 40 °C (Badtemperatur<br />
maximal 75–80 °C) (→ E 2 ). Die tarierte Vorlage wird im Eisbad<br />
gekühlt. Man bestimmt die Ausbeute an Destillat. Das Produktgemisch<br />
ist sehr leicht flüchtig, daher wird es für gaschromatographische<br />
oder 1 H-NMR-spektroskopische Untersuchungen dicht<br />
verschlossen im Kühlschrank aufbewahrt. Ausbeute an 1: 75–85%<br />
Isomerenmischung (1a:1b ca. 35:65), Sdp. 31–38 °C.<br />
1 Weshalb ein Intensivkühler?<br />
2 Was ist zu beobachten?<br />
3 Warum benutzt man ein Eisbad?<br />
<strong>Versuch</strong> <strong>2.2.1</strong>, Rev. 1.0 1
2. Eliminierungsreaktionen www.ioc-praktikum.de<br />
Hinweise zur Entsorgung (E)<br />
E 1 : Natrium-Reste → Entsorgung: Siehe Buch Kap. 0.2 oder "Arbeitsmethoden".<br />
E 2 : Destillationsrückstand, basische Ethanolatlösung mit Spuren anderer organischer Verbindungen und<br />
anorganischen Salzen: Neutralisation mit verdünnter Salzsäure → Entsorgung (H 2 O mit RHal/Halogenid).<br />
Auswertung des <strong>Versuch</strong>s<br />
1 H-NMR-Spektrum von 1a (300 MHz, CDCl 3 ): δ = 1.03 (3 H), 1.72 (3 H), 2.01 (2 H), 4.64–4.69 (2 H).<br />
615.5 Hz<br />
608.0 Hz<br />
600.6 Hz<br />
593.1 Hz<br />
315.3 Hz<br />
307.8 Hz<br />
300.3 Hz<br />
6.0<br />
5.0<br />
4.0<br />
3.0 2.0 1.0 [ppm] 0.0<br />
13 C-NMR-Spektrum (75.5 MHz, CDCl 3 ) von 1a: δ = 12.28 (CH 3 ), 22.44 (CH 3 ), 30.52 (CH 2 ), 108.33 (CH 2 ),<br />
147.73 (C).<br />
LM<br />
160 140<br />
120<br />
100 80<br />
60 40 20 [ppm] 0<br />
IR-Spektrum von 1a (Film):<br />
100<br />
T [%]<br />
50<br />
1375<br />
3075<br />
1650<br />
2885<br />
1450<br />
885<br />
2970<br />
2935<br />
0<br />
4000 3000 2000 1500 1000 ν ~ [cm -1 ]<br />
<strong>Versuch</strong> <strong>2.2.1</strong>, Rev. 1.0 2
2. Eliminierungsreaktionen www.ioc-praktikum.de<br />
1 H-NMR-Spektrum von 1b (300 MHz, CDCl 3 ): δ = 1.55 (3 H), 1.60 (3 H), 1.68 (3 H), 5.18 (1 H).<br />
5.2<br />
5.1<br />
1.7<br />
1.6<br />
1.5<br />
6.0<br />
5.0<br />
4.0<br />
3.0 2.0 1.0 [ppm] 0.0<br />
13 C-NMR-Spektrum (75.5 MHz, CDCl 3 ) von 1b: δ = 13.36 (CH 3 ), 17.25 (CH 3 ), 25.58 (CH 3 ), 118.44 (CH),<br />
132.04 (C).<br />
LM<br />
160 140<br />
120<br />
100 80<br />
60 40 20 [ppm] 0<br />
IR-Spektrum von 1b (Film):<br />
100<br />
T [%]<br />
1675<br />
50<br />
3025<br />
1375<br />
805<br />
1450<br />
2860<br />
2970<br />
2920<br />
0<br />
4000 3000 2000 1500 1000 ν ~ [cm -1 ]<br />
Von der Produktmischung wird ein 1 H-NMR-Spektrum aufgenommen. Aus der Integration ist das Produktverhältnis<br />
1a:1b zu bestimmen.<br />
Gaschromatographische Analyse des Reaktionsgemisches<br />
Gaschromatographische Bedingungen: Säule 2 m, 10 % SE 30 auf Chromosorb 60/80 mesh, Säulentemperatur:<br />
30 °C, Injektortemperatur: 70 °C. Man identifiziere die GC-Peaks mit Hilfe von Referenzsubstanzen (Assistent!).<br />
Aus dem Gaschromatogramm wird das Verhältnis der Olefine ermittelt (der Flächenfaktor wird vereinfacht<br />
mit 1 angenommen). Genauigkeit und Fehlerquellen sind zu bestimmen. Das Ergebnis ist mit dem NMRspektroskopisch<br />
bestimmten Produktverhältnis zu vergleichen.<br />
<strong>Versuch</strong> <strong>2.2.1</strong>, Rev. 1.0 3
2. Eliminierungsreaktionen www.ioc-praktikum.de<br />
* Formulieren Sie den zu 1a und 1b führenden Reaktionsmechanismus.<br />
* Man vergleiche das Produktverhältnis 1a/1b mit dem Produktverhältnis von <strong>Versuch</strong> 2.1.1 (1a/1b) und<br />
<strong>Versuch</strong> 2.2.6 (6a/6b). Diskutieren Sie die unterschiedlichen Reaktionsmechanismen in Hinblick auf ihre<br />
Regioselektivität.<br />
Weitere denkbare Reaktionsprodukte:<br />
CH 3<br />
CH 3<br />
OC 2<br />
H 5<br />
CH<br />
H 3<br />
C<br />
3<br />
OC 2<br />
H 5<br />
CH<br />
H 3<br />
C<br />
3<br />
A B<br />
* Mit welchen spektroskopischen Daten und einfachen <strong>Versuch</strong>en lassen sich A und B ausschließen?<br />
* Diskutieren Sie die denkbaren Reaktionsmechanismen.<br />
Literatur, allgemeine Anwendbarkeit der Methode<br />
Die Dehydrohalogenierung von Halogenalkanen mit starken Basen ist vielseitig einsetzbar, bedarf aber sorgfältig<br />
ausgewählter Reaktionsbedingungen, um Nebenprodukte zu vermeiden und eine hohe Produktselektivität zu<br />
erreichen. Siehe Einführung zu Kap. 2.2.<br />
<strong>Versuch</strong> <strong>2.2.1</strong>, Rev. 1.0 4