7.4.3: 3-Nitrophenol
7.4.3: 3-Nitrophenol
7.4.3: 3-Nitrophenol
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
7. Substitutionen an Aromaten und Heterocyclen www.ioc-praktikum.de<br />
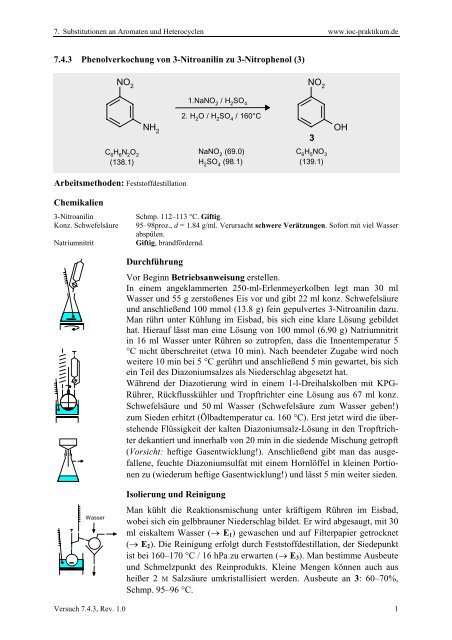
<strong>7.4.3</strong> Phenolverkochung von 3-Nitroanilin zu 3-<strong>Nitrophenol</strong> (3)<br />
NO 2<br />
NO 2<br />
1.NaNO 2<br />
/ H 2<br />
SO 4<br />
NH 2<br />
2. H 2<br />
O / H 2<br />
SO 4<br />
/ 160°C<br />
3<br />
OH<br />
C 6<br />
H 6<br />
N 2<br />
O 2<br />
(138.1)<br />
NaNO 2<br />
(69.0)<br />
H 2<br />
SO 4<br />
(98.1)<br />
C 6<br />
H 5<br />
NO 3<br />
(139.1)<br />
Arbeitsmethoden: Feststoffdestillation<br />
Chemikalien<br />
3-Nitroanilin<br />
Konz. Schwefelsäure<br />
Natriumnitrit<br />
Schmp. 112–113 °C. Giftig.<br />
95–98proz., d = 1.84 g/ml. Verursacht schwere Verätzungen. Sofort mit viel Wasser<br />
abspülen.<br />
Giftig, brandfördernd.<br />
Durchführung<br />
Vor Beginn Betriebsanweisung erstellen.<br />
In einem angeklammerten 250-ml-Erlenmeyerkolben legt man 30 ml<br />
Wasser und 55 g zerstoßenes Eis vor und gibt 22 ml konz. Schwefelsäure<br />
und anschließend 100 mmol (13.8 g) fein gepulvertes 3-Nitroanilin dazu.<br />
Man rührt unter Kühlung im Eisbad, bis sich eine klare Lösung gebildet<br />
hat. Hierauf lässt man eine Lösung von 100 mmol (6.90 g) Natriumnitrit<br />
in 16 ml Wasser unter Rühren so zutropfen, dass die Innentemperatur 5<br />
°C nicht überschreitet (etwa 10 min). Nach beendeter Zugabe wird noch<br />
weitere 10 min bei 5 °C gerührt und anschließend 5 min gewartet, bis sich<br />
ein Teil des Diazoniumsalzes als Niederschlag abgesetzt hat.<br />
Während der Diazotierung wird in einem 1-l-Dreihalskolben mit KPG-<br />
Rührer, Rückflusskühler und Tropftrichter eine Lösung aus 67 ml konz.<br />
Schwefelsäure und 50 ml Wasser (Schwefelsäure zum Wasser geben!)<br />
zum Sieden erhitzt (Ölbadtemperatur ca. 160 °C). Erst jetzt wird die überstehende<br />
Flüssigkeit der kalten Diazoniumsalz-Lösung in den Tropftrichter<br />
dekantiert und innerhalb von 20 min in die siedende Mischung getropft<br />
(Vorsicht: heftige Gasentwicklung!). Anschließend gibt man das ausgefallene,<br />
feuchte Diazoniumsulfat mit einem Hornlöffel in kleinen Portionen<br />
zu (wiederum heftige Gasentwicklung!) und lässt 5 min weiter sieden.<br />
Wasser<br />
Isolierung und Reinigung<br />
Man kühlt die Reaktionsmischung unter kräftigem Rühren im Eisbad,<br />
wobei sich ein gelbbrauner Niederschlag bildet. Er wird abgesaugt, mit 30<br />
ml eiskaltem Wasser (→ E 1 ) gewaschen und auf Filterpapier getrocknet<br />
(→ E 2 ). Die Reinigung erfolgt durch Feststoffdestillation, der Siedepunkt<br />
ist bei 160–170 °C / 16 hPa zu erwarten (→ E 3 ). Man bestimme Ausbeute<br />
und Schmelzpunkt des Reinprodukts. Kleine Mengen können auch aus<br />
heißer 2 M Salzsäure umkristallisiert werden. Ausbeute an 3: 60–70%,<br />
Schmp. 95–96 °C.<br />
Versuch <strong>7.4.3</strong>, Rev. 1.0 1
7. Substitutionen an Aromaten und Heterocyclen www.ioc-praktikum.de<br />
Hinweise zur Entsorgung (E)<br />
E 1 : Wässriges, saures Filtrat: Neutralisation mit Natronlauge → Entsorgung (H 2 O mit RH).<br />
E 2 : Filterpapier → Entsorgung (Org. Feststoffe).<br />
E 3 : Destillationsrückstand und verunreinigte Fraktionen in wenig Aceton aufnehmen → Entsorgung (RH).<br />
Auswertung des Versuchs<br />
1 H-NMR-Spektrum von 3 (300 MHz, DMSO-d 6 ): δ = 7.13–7.20 (1 H), 7.34–7.43 (1 H), 7.50–7.54 (1 H), 7.56–<br />
7.62 (1 H), 10.38 ( 1 H).<br />
7.5 7.0<br />
11.0 10.0 9.0 8.0 7.0 6.0 5.0 4.0 3.0 2.0 1.0 [ppm] 0.0<br />
13 C-NMR Spektrum von 3 (75.5 MHz, DMSO-d 6 ): δ = 109.45 (CH), 113.54 (CH), 122.12 (CH), 130.22 (CH),<br />
148.48 (C), 158.10 (C).<br />
LM<br />
160<br />
140<br />
120<br />
100 80<br />
60 40 20 [ppm] 0<br />
IR-Spektrum von 3 (KBr):<br />
100<br />
T [%]<br />
3090<br />
3110<br />
50<br />
1625<br />
3390<br />
1525<br />
1350<br />
0<br />
~<br />
4000 3000 2000 1500 1000 ν [cm -1 ]<br />
* Formulieren Sie den zu 3 führenden Reaktionsmechanismus.<br />
Versuch <strong>7.4.3</strong>, Rev. 1.0 2
7. Substitutionen an Aromaten und Heterocyclen www.ioc-praktikum.de<br />
Weitere denkbare Reaktionsprodukte:<br />
NO 2<br />
NO 2 NO 2<br />
NO 2<br />
N<br />
NO<br />
H<br />
A B C<br />
* Mit welchen spektroskopischen Daten lassen sich A–C ausschließen?<br />
* Diskutieren Sie die denkbaren Reaktionsmechanismen mit allen Zwischenstufen.<br />
Literatur, allgemeine Anwendbarkeit der Methode<br />
O<br />
Die Reaktion von Diazoniumsalzen mit Wasser unter Stickstoffabspaltung wird als Phenolverkochung<br />
bezeichnet. Die Reaktion kann unabhängig vom Gegenion des Salzes durchgeführt werden. Üblicherweise<br />
werden jedoch Hydrogensulfate gegenüber Chloriden oder Nitraten bevorzugt, da letztgenannte als Nucleophile<br />
in Konkurrenz treten können.<br />
Versuch <strong>7.4.3</strong>, Rev. 1.0 3