2.2.5: Phenylacetylen
2.2.5: Phenylacetylen
2.2.5: Phenylacetylen
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
2. Eliminierungsreaktionen www.ioc-praktikum.de<br />
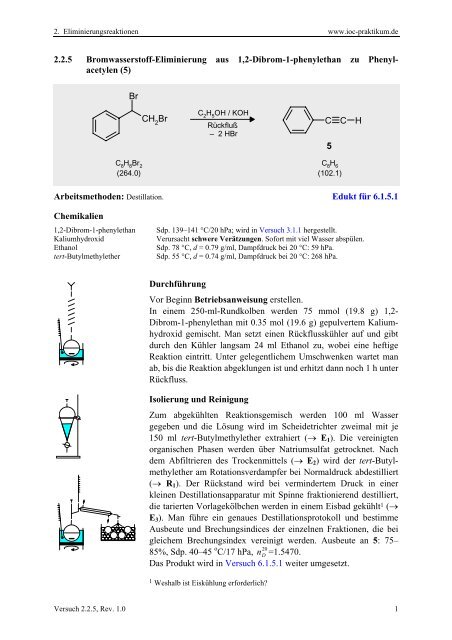
<strong>2.2.5</strong> Bromwasserstoff-Eliminierung aus 1,2-Dibrom-1-phenylethan zu <strong>Phenylacetylen</strong><br />
(5)<br />
Br<br />
CH 2<br />
Br<br />
C 2<br />
H 5<br />
OH / KOH<br />
Rückfluß<br />
– 2 HBr<br />
C C H<br />
5<br />
C 8<br />
H 8<br />
Br 2<br />
(264.0)<br />
C 8<br />
H 6<br />
(102.1)<br />
Arbeitsmethoden: Destillation. Edukt für 6.1.5.1<br />
Chemikalien<br />
1,2-Dibrom-1-phenylethan<br />
Kaliumhydroxid<br />
Ethanol<br />
tert-Butylmethylether<br />
Sdp. 139–141 °C/20 hPa; wird in Versuch 3.1.1 hergestellt.<br />
Verursacht schwere Verätzungen. Sofort mit viel Wasser abspülen.<br />
Sdp. 78 °C, d = 0.79 g/ml, Dampfdruck bei 20 °C: 59 hPa.<br />
Sdp. 55 °C, d = 0.74 g/ml, Dampfdruck bei 20 °C: 268 hPa.<br />
Durchführung<br />
Vor Beginn Betriebsanweisung erstellen.<br />
In einem 250-ml-Rundkolben werden 75 mmol (19.8 g) 1,2-<br />
Dibrom-1-phenylethan mit 0.35 mol (19.6 g) gepulvertem Kaliumhydroxid<br />
gemischt. Man setzt einen Rückflusskühler auf und gibt<br />
durch den Kühler langsam 24 ml Ethanol zu, wobei eine heftige<br />
Reaktion eintritt. Unter gelegentlichem Umschwenken wartet man<br />
ab, bis die Reaktion abgeklungen ist und erhitzt dann noch 1 h unter<br />
Rückfluss.<br />
Isolierung und Reinigung<br />
Zum abgekühlten Reaktionsgemisch werden 100 ml Wasser<br />
gegeben und die Lösung wird im Scheidetrichter zweimal mit je<br />
150 ml tert-Butylmethylether extrahiert (→ E 1 ). Die vereinigten<br />
organischen Phasen werden über Natriumsulfat getrocknet. Nach<br />
dem Abfiltrieren des Trockenmittels (→ E 2 ) wird der tert-Butylmethylether<br />
am Rotationsverdampfer bei Normaldruck abdestilliert<br />
(→ R 1 ). Der Rückstand wird bei vermindertem Druck in einer<br />
kleinen Destillationsapparatur mit Spinne fraktionierend destilliert,<br />
die tarierten Vorlagekölbchen werden in einem Eisbad gekühlt 1 (→<br />
E 3 ). Man führe ein genaues Destillationsprotokoll und bestimme<br />
Ausbeute und Brechungsindices der einzelnen Fraktionen, die bei<br />
gleichem Brechungsindex vereinigt werden. Ausbeute an 5: 75–<br />
85%, Sdp. 40–45 o C/17 hPa, n 20 D<br />
=1.5470.<br />
Das Produkt wird in Versuch 6.1.5.1 weiter umgesetzt.<br />
1 Weshalb ist Eiskühlung erforderlich?<br />
Versuch <strong>2.2.5</strong>, Rev. 1.0 1
2. Eliminierungsreaktionen www.ioc-praktikum.de<br />
Hinweise zur Entsorgung (E), Recycling (R) der Lösungsmittel<br />
E 1 : Wässrige alkalische Lösung mit organischen Verbindungen: Neutralisation, → Entsorgung (H 2 O mit<br />
RHal/Halogenid).<br />
E 2 : Kontaminiertes Trockenmittel → Entsorgung (Anorg. Feststoffe).<br />
E 3 : Destillationsrückstand und verunreinigte Fraktionen mit wenig Aceton lösen → Entsorgung (RHal).<br />
R 1 : Abdestilliertes Lösungsmittel → Recycling (tert-Butylmethylether).<br />
Auswertung des Versuchs<br />
1 H-NMR-Spektrum von 5 (300 MHz, CDCl 3 ): δ = 3.10 (1 H), 7.29–4.41 (3 H), 7.48–7.56 (2 H).<br />
8.0 6.0 4.0 2.0 [ppm] 0.0<br />
13 C-NMR-Spektrum (75.5 MHz, CDCl 3 ) von 5: δ = 77.21 (CH), 83.71 (C), 122.18 (C), 128.35 (CH), 128.81<br />
(CH), 132.18 (CH).<br />
* * *<br />
* LM<br />
140<br />
120<br />
100 80<br />
60 40 20 [ppm] 0<br />
IR-Spektrum von 5 (Film):<br />
100<br />
T [%]<br />
50<br />
3030<br />
3060<br />
3080<br />
2110<br />
1595<br />
1570<br />
1440<br />
1480<br />
3290<br />
0<br />
4000 3000 2000 1500 1000 ν ~ [cm -1 ]<br />
* Formulieren Sie den zu 5 führenden Reaktionsmechanismus.<br />
Versuch <strong>2.2.5</strong>, Rev. 1.0 2
2. Eliminierungsreaktionen www.ioc-praktikum.de<br />
Weitere denkbare Reaktionsprodukte:<br />
Br<br />
H<br />
H<br />
H<br />
H<br />
H 5<br />
C 2<br />
O<br />
H<br />
H<br />
H<br />
OC 2<br />
H 5<br />
O<br />
CH 3<br />
H<br />
Br<br />
OC 2<br />
H 5<br />
H<br />
A B C D E<br />
* Mit welchen spektroskopischen Daten und einfachen Versuchen lassen sich A – E ausschließen?<br />
* Diskutieren Sie die denkbaren Reaktionsmechanismen.<br />
Literatur, allgemeine Anwendbarkeit der Methode<br />
[1] K.N. Campbell, B.K. Campbell in Organic Syntheses Coll. Vol. 4 (Hrsg. N. Rabjohn), J. Wiley & Sons,<br />
New York, 1963, S. 763–765.<br />
Versuch <strong>2.2.5</strong>, Rev. 1.0 3