Teil II
Teil II
Teil II
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Organomagnesiumverbindungen<br />
1) Darstellungsmethoden<br />
a) Direktsynthese<br />
Lösungsmittel<br />
R‐X + Mg RMgX (Inertgasatmosphäre)<br />
Lösungsmittel: Ether, THF, NEt 3 , HMPT, Lösungsmittelgemische<br />
Reaktivität: X = I > Br > Cl >> F<br />
Aktivierung des Mg durch chemische oder physikalische Methoden:<br />
i) BrCH 2 ‐CH 2 Br + Mg MgBr 2 + CH 2 =CH 2<br />
ii) MgBr 2 + 2 K + KI {Mg} RIEKE‐Magnesium: sehr reaktiv<br />
KBr<br />
Ermöglicht Grignard‐Reaktionen bei sehr niedrigen Temperaturen.<br />
iii) Ultraschall
) Metallierung<br />
R‐H + R‘MgX<br />
RMgX + R‘H<br />
R = Alkin, Cyclopentadien, Inden, Fluoren, Trityl, …
Beispiele:<br />
HCX 3 + i PrMgCl CX 3 MgCl + i PrH<br />
THF, HMPT<br />
78 °C
c) Metall‐Halogen‐Austausch<br />
R‐X + R‘MgX RMgX + R‘X<br />
(vorzugsweise R‘ = i Pr, siehe Arbeiten von P. KNOCHEL)<br />
Der Austausch erfolgt vermutlich über einen „Vierzentren‐<br />
Mechanismus“:
Beispiele:<br />
0 °C, THF<br />
EtBr<br />
51% 25%<br />
THF<br />
70 °C
d) weitere Methoden<br />
Dioxan<br />
i) MgR 2 + MgX 2 2 RMgX SCHLENK‐Gleichgewicht!<br />
ii) HgR 2 + Mg MgR 2 + Hg<br />
iii) LiR + MgX 2<br />
RMgX + LiX<br />
Zn, Cu<br />
iv) Me 3 SiCHBr 2 Me 3 SiCHBr 2 (ZnBr) 2<br />
Mg<br />
Zn<br />
Me 3 SiCH(MgBr) 2
2) Nebenreaktionen<br />
a) WURTZ‐Kupplung<br />
2 RX + Mg R‐R R + MX MgX 2<br />
RMgX+ R‘X R‐R‘ + MgX 2<br />
Diese Reaktionen werden durch Übergangsmetallsalze<br />
Diese Reaktionen werden durch Übergangsmetallsalze<br />
katalysiert: z.B. Co 2+ , Ni 2+ , Fe 2+ , Pd 2+ , Cu + , Ag +
) Radikal‐Disproportionierung<br />
Bei T > 100 C erfolgt Bildung von Alkenen und Alkanen.<br />
c) Reaktionen mit Lösungsmitteln<br />
Etherspaltung!<br />
Δ
3) Funktionell substituierte Grignardreagenzien<br />
a) α‐funktionalisierte f i t Gi Grignardreagenzien<br />
i<br />
ROCH 2MgCl stabil bis 20 °C<br />
R 3 SiCH 2 MgCl, (EtO) 2 P(O)CH 2 MgI, R 2 C=C(MgCl)NMe 2<br />
b) β‐ funktionalisierte Grignardreagenzien sind in der Regel<br />
nicht stabil.<br />
Mg<br />
2 2 2 2 g 2<br />
E‐CH 2 ‐CH 2 ‐X CH 2 =CH 2 + EMgX E: z.B. Br, NR 2
Ausnahmen:<br />
Me 2 NCH 2 CH 2 MgCl (i) CO 2, (ii) H 2 O<br />
Me 2 NCH 2 CH 2 COOH<br />
(hergestellt aus RIEKE‐<br />
Magnesium bei 100 °C)
c) γ‐funktionalisierte Grignardreagenzien<br />
E‐CH 2 CH 2 CH 2 ‐MgX E = R 2 N, R 2 P, R 2 As, RO, RS, R 3 Si, R 3 Sn<br />
1. RMgCl<br />
2 2 2 2. Mg/THF<br />
2 2 2<br />
i) Cl‐CH 2 CH 2 CH 2 ‐OH ClMg‐CH 2 CH 2 CH 2 OMgCl + RH<br />
ii) Bu 3 SnO‐CHR‐CHR‘‐CHR‘‘‐Br<br />
Mg<br />
BrMgO‐CHR‐CHR CHR‘ ‐CHR‘‘‐SnBu 3<br />
1,4‐carbanionische Umlagerung
4) Schützen von reaktiven funktionellen Gruppen<br />
(Ketone, Aldehyde)<br />
5) Multifunktionelle Grignard‐Reagenzien<br />
E(CH 2 CH 2 CH 2 ‐MgX) MX)(E 2 = RN, O, S, R 2 Si, R 2 Sn)<br />
Me 3 SiCH(MgBr) 2 , XMg‐(CH 2 ) n ‐MgBr (n ≥ 3)<br />
(Me 3 Si) 2 C(MgBr) 2 ,<br />
N(CH 2 CH 2 CH 2 ‐MgCl) 3<br />
CH 2 (MgX) 2 (X = Cl, Br), B)<br />
2
RMgX: Reaktivität
RMgX: Das Schlenk‐Gleichgewicht
Strukturen von Organomagnesiumverbindungen<br />
(Adv. Organomet. Chem. 32 (1991), 47)<br />
bis 1989 waren 64 Strukturen mit Mg‐C‐Bindung<br />
Bekannt.<br />
Die Elektronegativität von Mg ist höher als die von Li,<br />
d. h., die Mg‐C‐Bindung g ist kovalenter und thermisch<br />
Stabiler.<br />
R‐Mg‐R lineare Struktur in der Gasphase:<br />
z. B. R = Me 3 CH 2
(Me 3 Si) S) 3 C‐Mg‐C(SiMe C(S 3 ) 3 lineare e Struktur tu auch im Festzustand<br />
Normalerweise werden polymere Strukturen gefunden.<br />
Mehrzentrenelektronen‐<br />
mangel‐Bindung<br />
tt tetraedrische di Koordination ist itder Normalzustand
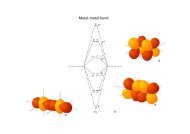
Verschiedene Structurtypen<br />
E = 0NR
drei Grundtypen:<br />
a) monomer<br />
tetraedrisch<br />
R = Ph, X = Br, L = THF<br />
R = Et, X = Br, L = Et 2 O<br />
R = Me, X = Me, L = NEt 3<br />
b) dimer<br />
R = Et, X = Br, L = NEt 3
unsymmetrische 3Z‐2e‐Bindung<br />
Mg‐C: 2.245 Å<br />
2.313 Å<br />
Beide Formen liegen im gleichen Kristall vor!
c) In Abwesenheit koordinierender i d Lösungsmittel bilden<br />
sich in der Regel polymere Strukturen.<br />
(Ph 2 M) Mg) n<br />
Der C‐Mg‐C‐Winkel möchte möglichst groß sein:<br />
keine Fünf‐ und Sechsringe<br />
[(CH 2 ) 4 Mg ∙2Dioxan] 2<br />
→ Zehnring<br />
[(CH 2 ) 5 Mg ∙2THF] 2<br />
→ Zwölfring
Nachfolgend sind einige Molekülstrukturen<br />
von Organomagnesiumverbindungen gezeigt.<br />
Die entsprechenden Kristalle wurden aus<br />
Lösungen der formalen RMgCl‐Verbindungen<br />
erhalten. Die strukturelle Vielfalt ist<br />
beeindruckend und ist ein Beleg für das<br />
Vorliegen des Schlenk‐Gleichgewichts.<br />
(siehe Chem. Commun. 2006, 2039;<br />
Organometallics Oga 2009, 28, 1598).
[{MeMgCl(thf)} 2 {MgCl 2 (thf) 2 } 2 ]
[{EtMgCl(thf)} 2 {MgCl 2 (thf) 2 } 2 ]
The cluster [{MgCl(thf) 2 } 3 (μ‐C 3 H 5 ) 2 ] + [Mg(C 3 H 5 ) 4 ]ˉ<br />
Kationischer<br />
Magnesiumcluster:<br />
+
Tetraallylmagnesiat‐Anion als<br />
Gegenion:<br />
2‐<br />
Das Magnesiumatom ist tetraedrisch konfiguriert.
MgCl 2 (C 5 H 5 N) 4
[{t‐BuMgCl(thf)} 2 {MgCl 2 (thf) 2 } 2 ]
[{Mg 2 Cl 3 (thf) 6 } {t‐BuMgCl 2 (thf)}]
(Ph 2 MgCl) 2 [{Mg 2 Cl 3 (thf) 3 }] 2
[{Mg 2 Cl 3 (thf) 6 } {PhMgCl 2 (thf)}]
[{PhMgCl(thf)} 2 {MgCl 2 (thf) 2 } 2 ]
[{Me 2 NCH 2 CH 2 CH 2 MgCl(thf)} 2 {MgCl 2 (thf) 2 } 2 ]
(Me 3 Si) 2 PMgBr(THF): Eine P‐haltige „Grignard“‐Verbindung<br />
(Eur. J. Inorg. Chem. 2010, 5471–5477) 5477)<br />
Si1<br />
Si2<br />
P<br />
Mg‘<br />
Br‘<br />
O‘<br />
O<br />
Br<br />
Mg<br />
P‘<br />
Si2‘<br />
Si1‘<br />
Die Mg‐Atome sind über P<br />
Die Mg‐Atome sind über P<br />
und nicht über Br verbrückt!
Ti<br />
Cl/Br2<br />
Mg1<br />
Cl/Br1<br />
Cl/Br5<br />
Mg2‘<br />
Cl/Br4<br />
Cl/Br3<br />
Mg2<br />
Mg1‘<br />
Ti‘
Me 3 SiMgBr(TMEDA): Eine Si‐analoge Grignard‐<br />
Verbindung<br />
(Angew. Chem. Int. Ed. Engl. 1995, 34, 1030)<br />
Si‘<br />
N2<br />
Br<br />
Mg‘<br />
N1‘<br />
N1<br />
Mg<br />
Br‘<br />
N2‘<br />
Si<br />
Essentiell ist die Verwendung von TMEDA<br />
Essentiell ist die Verwendung von TMEDA<br />
als Donorlösungsmittel!
Magnesium‐Anthracen Derivate<br />
Anthracen fungiert als Phasentransfer‐Katalysator für<br />
Magnesium. Im Gleichgewicht i ht kommt es ständig zur Bildung<br />
von atomarem Magnesium.
Magnesium‐Anthracen<br />
Hochtemperaturspeicher für Wasserstoff<br />
hochreaktives Magnesium
Magnesium‐Anthracen<br />
Ambidente Reaktivität<br />
i) ‚Aktiviertes‘ Mg zur Herstellung von Grignardreagenzien<br />
ii) Bifunktionelle Organomagnesiumverbindungen<br />
Problem: Häufig geringe Regioselektivität
Wie entsteht eine<br />
Grignard‐Verbindung?<br />
d<br />
H. M. Walborsky, Chemie in unserer Zeit 1991, 25, 108)<br />
40
Stereochemischer Verlauf der Bildung von<br />
Cyclopropyl‐Grignard‐Verbindungen<br />
1) Mg, THF<br />
2) CO 2 , 3) H +<br />
(S)‐(+)<br />
(+) (S)‐(‐)<br />
( )
X t(h) Ausbeute optische<br />
(%) Rihi(%) Reinheit Cl 3 89 26<br />
Br 3 79 17<br />
I 3 36 2<br />
Die Ausbeute und die optische Reinheit sind unabhängig<br />
von der Reaktionszeit t.<br />
Die Reaktion verläuft z. T. unter Erhalt der Konfiguration,<br />
d. h. Retention.<br />
Die Grignard‐Verbindung ist unter den Reaktionsbedingungen<br />
Die Grignard Verbindung ist unter den Reaktionsbedingungen<br />
konfigurativ stabil.
Racemisierung vor oder nach der Bildung<br />
von RMgX?<br />
1) MgBr 2<br />
2) MeOCH 2 CH 2 OMe<br />
(R)<br />
MgBr 2 , Ether<br />
‐LiBr<br />
Das MeOCH 2 CH 2 OMe zerstört<br />
evtl. noch vorhandenes RLi.<br />
(R)<br />
3) CO 2<br />
CO 2<br />
Die Grignard‐Verbindung ist unter den<br />
Reaktionsbedingungen konfigurativ stabil.<br />
Die Racemisierung muss offensichtlich vor<br />
ihrer Bildung stattfinden.<br />
(s)‐(‐) 100% Retention
Nebenprodukte: Radikale sind im Spiel !<br />
1) Mg, Ether<br />
+<br />
2) CO 2 , 3)H +<br />
+<br />
+
optisch und konfigurativ stabil !<br />
Die teilweise Racemisierung bei der Reaktion mit CO 2 findet<br />
also vor der Bildung von RMgBr statt.<br />
Radikale sind im Spiel!
2∙10 ‐11 s<br />
Warum erfolgt die Racemisierung dann aber<br />
nur teilweise?<br />
Die Reaktion läuft an der Metalloberfläche ab!
R<br />
∙<br />
X Kontaktionenpaar<br />
∙Mg<br />
R‐X<br />
Mg<br />
Mg<br />
(3)<br />
Retention<br />
(4 )<br />
R‐Mg‐X<br />
R ∙ MgX<br />
Mg<br />
Racemisierung<br />
Disproportionierung<br />
Dimerisierung<br />
lockeres Radikalpaar<br />
(Rotation von R∙ ist möglich)
1) SET von der Magnesiumoberfläche in das<br />
antibindende Orbital der C‐X‐Bindung:<br />
Es entsteht das Radikal‐Anion R‐Xˉ<br />
als Kontaktionenpaar mit Mg + .<br />
2) Die Lebensdauer dieses Kontaktionenpaares<br />
ist entscheidend für den weiteren Reaktionsverlauf.<br />
a) Ist die Lb Lebensdauer kurz (z.B. für X = Cl),<br />
erfolgt Reaktion 4 unter Retention.<br />
b) Ist die Lebensdauer lang (z.B. für X = I),<br />
bildet sich ein lockeres Radikalpaar und die<br />
Reaktion erfolgt unter Racemisierung.
RMgX ‐ Bildungsmechanismus<br />
SET‐Mechanismus<br />
R—X + Mg RXˉ• + Mg + R • + MgX •<br />
TMPO, ein „freies“ Radikal<br />
TMPO<br />
R—MgX