CVVHD mit EMiC®2-Filter - Fresenius Medical Care Austria GmbH
CVVHD mit EMiC®2-Filter - Fresenius Medical Care Austria GmbH
CVVHD mit EMiC®2-Filter - Fresenius Medical Care Austria GmbH
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
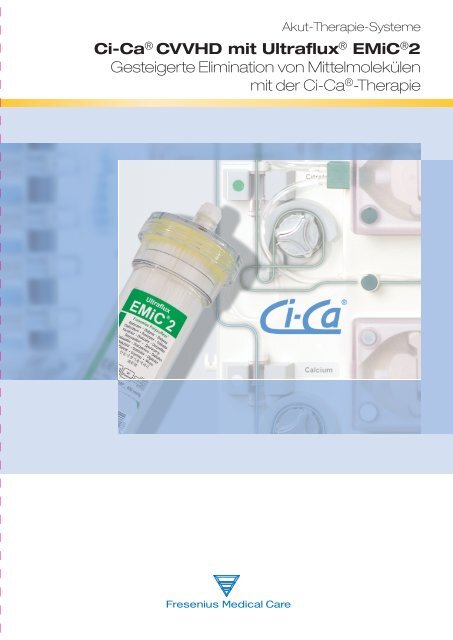
Akut-Therapie-Systeme<br />
Ci-Ca ® <strong>CVVHD</strong> <strong>mit</strong> Ultraflux ® EMiC ® 2<br />
Gesteigerte Elimination von Mittelmolekülen<br />
<strong>mit</strong> der Ci-Ca ® -Therapie
Ci-Ca ® <strong>CVVHD</strong> <strong>mit</strong> Ultraflux ® EMiC ® 2<br />
Ci-Ca ® <strong>CVVHD</strong> <strong>mit</strong> Ultraflux ® EMiC ® 2 ist eine neue CRRT-Therapie, die die Vorteile der<br />
Citratantikoagulation im <strong>CVVHD</strong>-Modus <strong>mit</strong> einer verbesserten Elimination von<br />
Mittelmolekülen verbindet<br />
• Signifikant erhöhte Mittelmolekül Clearance –<br />
vergleichbar <strong>mit</strong> einer CVVH-Therapie<br />
• Albuminkonzentration weitgehend stabil<br />
• Zuverlässige Citratantikoagulation<br />
• Hohe Effektivität auch bei niedrigen<br />
Blutflüssen<br />
• multiFiltrate Ci-Ca ® – integriertes Citratund<br />
Calciummanagement<br />
Einsatz der kombinierten Ci-Ca ® EMiC ® 2-Therapie:<br />
Patienten <strong>mit</strong> hohen Mittelmolekülkonzentrationen<br />
• Hohe Konzentration von Myoglobin aufgrund<br />
von Rhabdomyolyse<br />
• Hohe Konzentrationen von Cytokinen, Interleukinen<br />
und anderen Faktoren bei Patienten <strong>mit</strong> Sepsis<br />
(Studien müssen eine Verbesserung im Behandlungsergebnis<br />
noch zeigen)<br />
Patienten <strong>mit</strong> hohem Blutungsrisiko und HIT<br />
• Akute Blutung oder erhöhtes Blutungsrisiko aufgrund<br />
von Traumata oder nach operativen Eingriffen<br />
• Bei heparininduzierter Thrombozytopenie (HIT II),<br />
bei der Citrat zusätzlich zur notwendigen<br />
systemischen Antikoagulation eingesetzt wird<br />
Mittelmolekül<br />
Molekulargewicht<br />
ß2-Mikroglobulin (ß2m)<br />
12 kDa<br />
Cystatin C<br />
13 kDa<br />
Myoglobin<br />
17 kDa<br />
Interleukin-1ß (IL-1ß)<br />
18 kDa<br />
Interleukin-6 (IL-6)<br />
21 kDa<br />
Freie Leichte Immunglobulinkette kappa (FLC kappa) 25 kDa<br />
Interleukin-10 (IL-10)<br />
37 kDa
Ultraflux ® EMiC ® 2 profitiert von modernster Membrantechnologie durch eine<br />
höher permeable Membran und angepassten Cut-off<br />
Vorteile des Ultraflux ® EMiC ® 2<br />
• Enhanced Middle Molecule Clearance<br />
• Cut-off liegt bei ~ 40 kDa<br />
• Fortschrittliche Ondulationstechnologie sichert<br />
gleichmäßigen Dialysatfluss zwischen den Fasern<br />
und erhöht da<strong>mit</strong> die Eliminationsleistung<br />
• Steile Siebkoeffizientenkurve nähert sich der<br />
glomerulären Basalmembran an<br />
• Verringert die Lücke zur physiologischen<br />
Funktion der Niere<br />
1<br />
0,8<br />
Siebkoeffizient<br />
0,6<br />
0,4<br />
0,2<br />
Low Flux<br />
High Flux<br />
EMiC ® 2<br />
Glomeruläre<br />
Basalmembran<br />
0<br />
0,2<br />
1 10 100<br />
IL-10<br />
Molekulargewicht in kDa<br />
ß2m<br />
FLC kappa<br />
Cystatin C<br />
IL-6<br />
Myoglobin<br />
IL-1ß Albumin<br />
Elimination von Mittelmolekülen – bei gleichzeitiger Erhaltung der Albuminkonzentration im Serum<br />
EMiC ® 2 <strong>CVVHD</strong><br />
• Signifikant erhöhte Mittelmolekül Clearance 1<br />
• Albumin-Serumkonzentration: <strong>CVVHD</strong> EMiC ® 2<br />
vergleichbar <strong>mit</strong> CVVH <strong>mit</strong> Standardfilter 1<br />
• Vergleichbare hämodynamische und respiratorische<br />
Toleranz bei beiden Verfahren 2<br />
Mittelmolekül Clearance*<br />
Albumin Clearance<br />
Clearance (mL/min)<br />
20<br />
16<br />
12<br />
8<br />
4<br />
* p < 0,001 0,20 0,20 * p < 0,001* p < 0,001 <strong>CVVHD</strong> <strong>mit</strong> <strong>CVVHD</strong> EMiC ® <strong>mit</strong> 2 EMiC ® 2<br />
CVVH <strong>mit</strong> CVVH AV1000S <strong>mit</strong> AV1000S<br />
*<br />
*<br />
*<br />
*<br />
Clearance (mL/min)<br />
0,15<br />
0,10<br />
0,05<br />
Clearance (mL/min)<br />
0,15<br />
0,10<br />
* *<br />
0,05<br />
* *<br />
* * * *<br />
0<br />
15 min<br />
1h 4h 12h 24h<br />
0<br />
0<br />
15 min 15 1h min 1h 4h 4h 12h 12h 24h 24h<br />
*FLC kappa (25 kDa)
Ci-Ca ® EMiC ® 2 baut die Vorteile der multiFiltrate Ci-Ca ® weiter aus:<br />
Vorteile der Citratantikoagulation<br />
• Zuverlässige extrakorporale Antikoagulation 3<br />
• Deutlich reduziertes Risiko von Blutungskomplikationen<br />
im Vergleich zur systemischen<br />
Antikoagulation z. B. <strong>mit</strong> Heparin 4<br />
• Effektivere Behandlung und minimierte Therapieunterbrechungen<br />
durch weniger Clotting 5<br />
Vorteile des Behandlungsmodus <strong>CVVHD</strong><br />
• Hohe Effektivität bei niedrigen Blutflüssen<br />
• Niedrige Blutflüsse reduzieren den<br />
Bedarf an Citrat<br />
• Kleinere, weniger invasive Katheter einsetzbar<br />
• Längere <strong>Filter</strong>laufzeiten als <strong>mit</strong> konvektiven<br />
Verfahren 6
Bestellinformation für das multiFiltrate-Kit<br />
multiFiltrate-Kit Ci-Ca ® <strong>CVVHD</strong> EMiC ® 2<br />
Bezeichnung<br />
Ultraflux ® EMiC ® 2<br />
multiFiltrate Ci-Ca ® -Kassette<br />
Dialysatsystem multiFiltrate<br />
Art.-Nr. F00001172<br />
Beschreibung<br />
Ultraflux ® -Dialysator, dampfsterilisiert, 1,8 m² Oberfläche,<br />
<strong>Fresenius</strong> Polysulfon ® -Membran, Blutfüllvolumen 130 mL<br />
multiFiltrate-Kassette <strong>mit</strong> arteriellem und venösem Blutschlauchsystem,<br />
Filtratsystem sowie integrierten Citrat- und Calciumleitungen<br />
Dialysatsystem für multiFiltrate <strong>mit</strong> integriertem Heizbeutel<br />
Leistungsdaten/Technische Daten<br />
Ultraflux ® EMiC ® 2<br />
Effektive Oberfläche (m²) 1,8<br />
Wandstärke/inneres Lumen (µm) 35/220<br />
Blutfüllvolumen (mL) 130<br />
Bereich für empfohlenen Blutfluss (mL/min) 100 – 350<br />
Maximaler Dialysatfluss (mL/min) 1000<br />
Maximaler Filtratfluss (mL/min)<br />
10% vom Blutfluss<br />
Gesamtmenge an Ultrafiltrat, generiert in 24 h (inkl. Antikoagulation) 12000 mL<br />
Membranmaterial <strong>Fresenius</strong> Polysulfon ®<br />
Gehäusematerial<br />
Vergussmasse<br />
Sterilisationsmethode<br />
Polycarbonat<br />
Polyurethan<br />
INLINE-Dampfsterilisation<br />
Literatur<br />
1. Mathieu Page, Charles-Eric Ber, Davy Hayi-Slayman, Bernard Allaouchiche, Thomas Rimmelé, Removal of Middle-Molecular Weight Molecules<br />
with High Cut-Off Continuous Hemodialysis; ASA Annual Meeting, 17.-21. October 2009, New Orleans<br />
2. Mathieu Page, Charles-Eric Ber, Davy Hayi-Slayman, Bernard Allaouchiche, Thomas Rimmelé, Clinical Tolerance of Continuous Hemodialysis<br />
with a High Cut-Off Membrane; ASA Annual Meeting, 17.-21. October 2009, New Orleans<br />
3. Stanislao Morgera, Michael Schneider, Torsten Slowinski, Ortrud Vargas-Hein, Heidrun Zuckermann-Becker, Harm Peters, Detlef Kindgen-Milles,<br />
Hans-Hellmut Neumayer, A Safe Citrate Anticoagulation Protocol with Variable Treatment Efficacy and Excellent Control of the Acid-Base Status;<br />
Crit <strong>Care</strong> Med 2009; 37 (6): 2018-2024<br />
4. Heleen M. Oudemans-van Straaten, Citrate Anticoagulation for Continuous Renal Replacement Therapy in the Critically Ill; Blood Purif 2010, 29: 191-196<br />
5. Stanislao Morgera, Cornelia Scholle, Gitana Voss, Michael Haase, Ortrud Vargas-Hein, Dietmar Krausch, Christoph Melzer, Simone Rosseau,<br />
Heidrun Zuckermann-Becker, Hans-H. Neumayer, Metabolic Complications during Regional Citrate Anticoagulation in Continuous Venovenous Hemodialysis:<br />
Single-Center Experience; Nephron Clin Pract 2004, 97: c131-c136<br />
6. Zaccaria Ricci, Claudio Ronco, Alessandra Bachetoni, Giuseppe D‘amico, Stefano Rossi, Elisa Alessandri, Monica Rocco, and Paolo Pietropaoli, Solute Removal<br />
during Continuous Renal Replacement Therapy in Critically Ill Patients: Convection Versus Diffusion; Critical <strong>Care</strong> 2006; 10: R67<br />
Die <strong>mit</strong> „®“ markierten Zeichen/Namen sind in ausgewählten Ländern registrierte Marken des <strong>Fresenius</strong> Konzerns.
F00001835 D (1 HH-KCM 11.10) © Copyright 2010 <strong>Fresenius</strong> <strong>Medical</strong> <strong>Care</strong> Deutschland <strong>GmbH</strong> -zertifi ziert. PEFC/04-31-0768<br />
Firmensitz: <strong>Fresenius</strong> <strong>Medical</strong> <strong>Care</strong> Deutschland <strong>GmbH</strong> · 61346 Bad Homburg v.d.H. · Deutschland · Telefon: +49 (0) 6172-609-0 · Fax: +49 (0) 6172-609-2191<br />
Deutschland: <strong>Fresenius</strong> <strong>Medical</strong> <strong>Care</strong> <strong>GmbH</strong> · Else-Kröner-Str. 1 · 61352 Bad Homburg v.d.H. · Telefon: +49 (0) 6172-609-0 · Fax: +49 (0) 6172-609-8740<br />
Österreich: <strong>Fresenius</strong> <strong>Medical</strong> <strong>Care</strong> <strong>Austria</strong> <strong>GmbH</strong> · Lundenburgergasse 5 · 1210 Wien · Telefon: +43 (0) 1-2923501 · Fax: +43 (0) 1-292350185 · E-mail: fmc.austria@fmc-ag.com<br />
Schweiz: <strong>Fresenius</strong> <strong>Medical</strong> <strong>Care</strong> (Schweiz) AG · Spichermatt 30 · 6370 Stans · Telefon: +41 (0) 41-6195050 · Fax: +41 (0) 41-6195080 · E-mail: info.ch@fmc-ag.com<br />
www.fmc-ag.com