Juveniler Morbus Adamantiades - Städtisches Klinikum Dessau
Juveniler Morbus Adamantiades - Städtisches Klinikum Dessau
Juveniler Morbus Adamantiades - Städtisches Klinikum Dessau
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
258<br />
Hautarzt<br />
1997 · 48:258–261 © Springer-Verlag 1997<br />
Zusammenfassung<br />
Der 12jährige Junge entwickelte innerhalb<br />
von zwei Jahren den vollen Symptomenkomplex<br />
eines <strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet.<br />
Es handelte sich um die mukokutane Variante<br />
der Erkrankung mit rezidivierenden<br />
bis persistierenden oralen Aphthen mit Beteiligung<br />
der Rachenhinterwand, rezidivierenden<br />
Genitalulzera, perianalen Ulzerationen<br />
und ein positives Pathergie-Phänomen.<br />
Eine Augenbeteiligung sowie weitere, mit<br />
der Erkrankung asoziierte, Symptome wurden<br />
nicht nachgewiesen, allerdings wiesen<br />
das junge Alter beim Auftreten der Erkrankung<br />
und das männliche Geschlecht eher auf<br />
eine schlechte Prognose hin. Beim Vater des<br />
jungen Patienten bestand ein Asthma bronchiale<br />
mit rezidivierenden Infekten der<br />
Atemwege. Es war ein IgG-3-Subklassendefekt<br />
bekannt. Die immunologischen Untersuchungen<br />
des Jungen sowie seines Vaters<br />
zeigten im Lymphozytentransformationstest<br />
jeweils eine stark erniedrigte Stimulation<br />
mit Anti-CD3-monoklonalem Antikörper bei<br />
normaler Stimulation mit PWM, CoA und<br />
PHA. Darüber hinaus war bei beiden Patienten<br />
der lösliche Interleukin-6-Rezeptor im<br />
Serum stark reduziert.<br />
Schlüsselwörter<br />
<strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet · Immundefekt<br />
| Der Hautarzt 4·97<br />
Farbbildkasuistik<br />
Katja Krüger 1 · Klaus Fritz 1 · Volker Daniel 2 · Christos C. Zouboulis 3 · 1 Gemeinschaftspraxis<br />
Dr.Klaus Fritz, Dr.Isabel Gahlen, Landau · 2 Institut für Immunologie (Leiter:Prof.Dr.S.C.Meurer),<br />
Universität, Heidelberg · 3 Universitäts-Hautklinik und Poliklinik (Leiter und Geschäftsf.Direktor:<br />
Prof.Dr.Prof.h.c.C.E.Orfanos), <strong>Klinikum</strong> Benjamin Franklin, Freie Universität, Berlin<br />
<strong>Juveniler</strong> <strong>Morbus</strong> <strong>Adamantiades</strong>-<br />
Behçet bei erniedrigter Stimulation<br />
mit Anti-CD3-monoklonalen<br />
Antikörper<br />
Beim <strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet<br />
handelt es sich um eine schubweise,<br />
meist chronisch progredient verlaufende<br />
Allgemeinerkrankung vom Typ einer<br />
Systemvaskulitis mit polytoper Organbeteiligung<br />
[28]. Die Originalbeschreibungen<br />
stammen aus den Jahren<br />
1931 und 1937 [1, 5]. Die Erkrankung<br />
wird klinisch durch das rezidivierende<br />
Auftreten von oralen Aphthen, Genitalulzera<br />
und Iritis mit Hypopyon gekennzeichnet.<br />
Die Prognose ist ernst; die<br />
Schwere der Erkrankung wird in der<br />
Regel vom Grad der Behinderung<br />
durch Erblindung, systemische vaskuläre<br />
Manifestationen, neurologische<br />
Ausfälle und Darmperforation bestimmt<br />
[28]. In 2–7% der Fälle kommen<br />
letale Verlaufsformen vor.<br />
Der <strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet<br />
beginnt gewöhnlich – unabhängig von<br />
Geschlecht oder geographischer Region<br />
– im dritten oder vierten Lebensjahrzehnt<br />
[28]. Allerdings wurde auch ein<br />
sehr früher oder später Anfangszeitpunkt<br />
registriert. Kinder können an<br />
einzelnen Symptomen eines <strong>Morbus</strong><br />
<strong>Adamantiades</strong>-Behçet erkranken [12,<br />
20]. Der volle Symptomenkomplex ist<br />
allerdings im Kindesalter selten und<br />
manifestiert sich lediglich bei 1,5–3,1%<br />
der Patienten vor dem 15. bzw. dem 16.<br />
Lebensjahr [13, 22].<br />
Obwohl die Erkrankung seit der<br />
Antike beobachtet wird, bleibt ihre<br />
Ätiologie bis heute unklar [28]. Diskutiert<br />
wird das Zusammenspiel verschiedener<br />
Faktoren, insbesondere einer genetischen<br />
Prädisposition, einer potentiellen<br />
infektiösen Genese viraler oder<br />
bakterieller Herkunft, multipler Dysregulationen<br />
des Immunsystems, darunter<br />
auch eine verstärkte Chemotaxis, eines<br />
Defekts an Endothelzellen und einer<br />
gestörten Regulation von Gerinnungsfaktoren.<br />
Man vermutet, daß eine<br />
genetische Prädisposition in Kombination<br />
mit einem exogenen Faktor – z.B.<br />
eine Infektion – zur Störung der Immunregulation<br />
und somit zur Manifestation<br />
der Erkrankung führt [28].<br />
Wir stellen hier den seltenen Fall<br />
eines Kindes mit aktivem mukokutanen<br />
<strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet vor.<br />
Die immunologischen Untersuchungen<br />
sowohl des Patienten als auch seines<br />
Vaters, der an einem bekannten IgG-3<br />
Subklassendefekt bei Asthma bronchiale<br />
und rezidivierenden Infekten der<br />
Atemwege erkrankt ist, zeigten eine<br />
Reihe von Auffälligkeiten<br />
Kasuistik<br />
Anamnese<br />
Bei dem 12jährigen Jungen traten vor zwei<br />
Jahren erstmalig Genitalulzera auf. Kurze<br />
Zeit später folgten orale Aphthen. Während<br />
erstere langsam abheilten zeigten die Aphthen<br />
starke Rezidivfreudigkeit und neigten<br />
zur Persistenz. Insbesondere die hinteren<br />
Abschnitte der Mundhöhle und die Rachenhinterwand<br />
waren mit größeren teils entzündlichen<br />
teils erosiven Läsionen versehen.<br />
Aus der Anamnese ergaben sich keine<br />
Hinweise auf Augen- und Gelenkbeteiligung,<br />
sowie neurologische und gastrointe-<br />
Dr. K Krüger<br />
Praxis Dr. Guldner-Engelmann, Dr. Shih,<br />
Leonberger Straße 97, D-71229 Leonberg&/fn-block:&bdy:
Hautarzt<br />
1997 · 48:258–261 © Springer-Verlag 1997<br />
K. Krüger · K. Fritz · V. Daniel · Ch.C. Zouboulis<br />
Juvenile <strong>Adamantiades</strong>-Behçet’s disease<br />
with diminished response to stimulation<br />
with anti-CD3 monoclonal antibody<br />
Summary<br />
A 12 year old boy developed the complete<br />
symptom complex of <strong>Adamantiades</strong>-Behçet’s<br />
disease over a two-year period. He presented<br />
with the mucocutaneous variant with<br />
recurrent to persistent oral ulcers which extended<br />
into the pharynx, recurrent genital<br />
ulcers, perianal lesions, and a positive pathergy<br />
test. Ocular involvement and other<br />
symptoms associated with the disease were<br />
absent. However, the early onset of the<br />
disease and the male gender indicated a bad<br />
prognosis.The patients father deficiency of<br />
suffered from bronchial asthma with recurrent<br />
respiratory infections. An IgG-3 subclass<br />
was detected. Lymphocyte transformation<br />
tests showed markedly diminished response<br />
to stimulation with anti-CD3 monoclonal antibody<br />
in both patients, while response to<br />
PWM, CoA and PHA was normal. In addition,<br />
the concentration of serum soluble interleukin<br />
6 receptor was reduced in both patients.<br />
Key words<br />
<strong>Adamantiades</strong>-Behçet’s disease · Immune<br />
deficiency<br />
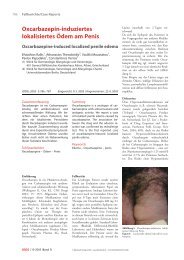
Abb. 1a, b � Histologische Untersuchung<br />
der Pathergiereaktion<br />
bei einem <strong>Morbus</strong> <strong>Adamantiades</strong>-<br />
Behçet. (a) Kräftiges entzündliches<br />
Infiltrat im mittleren Corium.<br />
Im oberen Papillarkörper<br />
sind einige extravasale Erythrozyten<br />
und eine kräftige Ödembildung<br />
zu sehen. Das Epidermis ist<br />
flach mit Spongiose und einer<br />
schmalen korbgeflechtartigen<br />
Hornschicht (H & E, 14,5×).<br />
(b) Massive Akkumulation neutrophiler<br />
Granulozyten im entzündlichen<br />
Infiltrat, die stellenweise<br />
betont perivaskulär liegen<br />
(H & E, 72×)<br />
a<br />
stinale Symptome oder rezidivierende<br />
Thrombophlebitiden. Die familiäre Anamnese<br />
war bzgl. eines <strong>Morbus</strong> <strong>Adamantiades</strong>-<br />
Behçet leer. Beide Elternteile waren deutscher<br />
Herkunft. Der Vater des Jungen litt an<br />
rezidivierenden Atemwegsinfekten mit<br />
Asthma bronchiale bei bekanntem isoliertem<br />
IgG-3-Subklassendefekt. Der Verdacht<br />
einer familiären Koinzidenz immunologischer<br />
Auffälligkeiten war der Anlaß, weitere<br />
Untersuchungen durchzuführen.<br />
Befunde<br />
Bei der klinischen Untersuchung waren in<br />
Abheilung befindende Genitoanalulzera<br />
und eine floride Aphthe an der Rachenhinterwand<br />
zu sehen. Die Genitoanalulzera<br />
heilten mit Hinderlassung von Narben ab.<br />
Nach einer intrakutanen Injektion von 0,1<br />
ml 0,9%iger Kochsalzlösung gelang der<br />
Nachweis eines positiven Pathergiephänomens.<br />
Der HLA-Phänotyp des Sohnes war:<br />
A2, A22, B35, Cw4, DR4, der des Vaters: A11,<br />
A24, B35, B44, Cw2, DR4, DR7. Sowohl beim<br />
Sohn als auch beim Vater zeigten sich im<br />
Lymphozytenstimulationstest eine erniedrigte<br />
Stimulation mit Anti-CD3-monoklonalem<br />
Antikörper bei normaler Stimulation<br />
mit PWM, CoA und PHA. Beim Vater zeigte<br />
sich zusätzlich noch eine erniedrigte allogene<br />
Stimulation. Der lösliche Interleukin-6-<br />
Rezeptor im Serum war stark erniedrigt<br />
sowohl beim Sohn 9157 pg/ml als auch<br />
beim Vater 822 pg/ml (Normbereich 30000–<br />
60000 pg/ml). Der Vater zeigte einen isolierten<br />
IgG-3-Subklassendefekt in Serum mit<br />
0,26 g/l (Normbereich 0,41–1,29 g/l) bei<br />
gleichzeitig niedrigem Gesamt-IgG von 6,3<br />
g/l (Normbereich 8–18 g/l). Dagegen lag der<br />
Sohn mit IgG-3 0,52 g/l im Normbereich<br />
(0,13–1,17 g/l).<br />
Die toxikologische Untersuchung (Lindan,<br />
Pentachlorphenol, polychlorite Biphenyle,<br />
Hexachlorcyclohexan), sowie der Gerinnungsstatus<br />
und die Bestimmung von<br />
Kupfer im Serum waren bei Vater und Sohn<br />
unauffällig. Ein Hinweis auf eine Typ-I-Sensibilisierung<br />
lag nicht vor.<br />
b<br />
Histologische Untersuchung der<br />
Pathergiereaktion<br />
Im Bereich des mittleren Koriums sieht man<br />
ein kräftiges entzündliches Infiltrat mit einer<br />
massiven Akkumulation neutrophiler<br />
Granulozyten (Abb. 1). Stellenweise liegen<br />
die neutrophilen Granulozyten betont perivaskulär.<br />
Allerdings ist weder eine Leukozytoklasie<br />
noch eine fibrinoide Nekrose der<br />
einzelnen Gefäßwände festzustellen. Im<br />
oberen Papillarkörper findet man einige extravasale<br />
Erythrozyten und eine kräftige<br />
Ödembildung. Das Deckepithel ist flach mit<br />
Spongiose und einer schmalen korbgeflechtartigen<br />
Hornschicht.<br />
Besprechung<br />
Der 12jährige Patient zeigte rezidivierende<br />
bis persistierende orale Aphthen<br />
mit Beteiligung der Rachenhinterwand,<br />
Genitalulzera und perianale Ulzera als<br />
kutane Manifestation und ein positives<br />
Pathergie-Phänomen. Mit Hilfe der Kriterien<br />
der “International Study Group<br />
for Behçet’s disease” [15] und nach dem<br />
Ausschluß anderer Erkrankungen stellten<br />
wir die Diagnose eines <strong>Morbus</strong><br />
<strong>Adamantiades</strong>-Behçet.<br />
Die Diagnose eines <strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet<br />
wird häufig durch<br />
monosymptomatische Phasen und<br />
asynchrones Auftreten der Symptome<br />
erschwert. Bei multiplen Aphthen pro<br />
Schub, insbesondere wenn die Aphthen<br />
auch im hinteren Bereich der Mundhöhle<br />
lokalisiert sind, sollte ein <strong>Morbus</strong><br />
<strong>Adamantiades</strong>-Behçet in Erwägung gezogen<br />
werden [7]. Etwa 17% der Patienten<br />
mit einer rezidivierenden Aphthose<br />
entwickeln über die Jahre den vollen<br />
Symptomenkomplex der Erkrankung<br />
[21].<br />
Der Hautarzt 4·97 | 259
260<br />
Perianale Ulzerationen kommen<br />
fast ausschließlich beim juvenilen <strong>Morbus</strong><br />
<strong>Adamantiades</strong>-Behçet vor. Während<br />
sie sich bei weniger als 1% der<br />
erwachsenen Patienten manifestieren,<br />
treten sie bei 6–14% der unter 15 Jahren<br />
alten Patienten auf [13].<br />
Das Phänomen der kutanen Pathergie<br />
bzw. einer Hyperreaktivität der<br />
Haut an Stellen kleiner Verletzungen<br />
gehört heute zu den Hauptkriterien der<br />
Erkrankung [15]. Die kutane Pathergie<br />
manifestiert sich klinisch als erythematöse<br />
Infiltration, Papel oder sterile Pustel<br />
am Ort eines Nadelstiches bzw. einer<br />
kleinen Verletzung bis zu 48 h nach<br />
dem Geschehen. Im deutschsprachigen<br />
Raum wird das Phänomen der kutanen<br />
Pathergie auch Katzenellenbogen-Phänomen<br />
genannt [17]. Die Pathergie-Reaktion<br />
ist bei westeurpäischen Patienten<br />
häufig negativ und weist signifikant<br />
niedrigere Positivitätsraten auf als bei<br />
Patienten, die aus den Endemiegebieten<br />
stammen [27]. Das Pathergie-Phänomen<br />
ist eine vaskuläre Reaktion:<br />
sie weist histologisch subepidermale<br />
Ödembildung, Schwellung der Kapillarendothelien<br />
und dichtes, perivaskuläres,<br />
entzündliches Infiltrat überwiegend<br />
von neutrophilen Granulozyten<br />
auf [16,25].<br />
Das vermehrte Auftreten der Erkrankung<br />
innerhalb von Familien und<br />
das häufige Vorkommen von HLA-B5<br />
bei Patienten unterschiedlicher Herkunft<br />
[28] konnte bei den deutschstämmigen<br />
Patienten des Deutschen<br />
Registers „<strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet“<br />
nicht aufgezeigt werden [29]. Interessanterweise<br />
besteht ein Zusammenhang<br />
zwischen dem Vorhandensein<br />
des HLA-B5-Antigens und einer<br />
Augenbeteiligung bzw. einem Befall<br />
des Gefäßsystems [6, 29]. Somit bekommt<br />
das HLA-B5-Antigen eine prognostische<br />
Bedeutung. Das Fehlen des<br />
HLA-B5 bei unserem Patienten spricht<br />
gegen eine zu erwartende systemische<br />
Gefäßbeteiligung. Im Gegensatz dazu<br />
sind das männliche Geschlecht und die<br />
frühe Manifestation der Erkrankung in<br />
der Regel schlechte Prognosemarker<br />
[28].<br />
Die bei unseren Patienten nachgewiesene<br />
normale Lymphozytenstimulation<br />
mit CoA und PHA bei Kranken<br />
mit <strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet ist<br />
aus einer früheren Studie bekannt [8].<br />
Bei unserem jungen Patienten und sei-<br />
| Der Hautarzt 4·97<br />
Farbbildkasuistik<br />
nem Vater fand sich jeweils im Lymphozytenstimulationstest<br />
eine stark erniedrigte<br />
Stimulation mit Anti-CD3monoklonalem<br />
Antikörper, welches<br />
gegen den T-Zellrezeptorkomplex gerichtet<br />
ist [10]. Dieses ist als Ausdruck<br />
eines Immundefektes zu werten. Bei<br />
<strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet finden<br />
sich in bezug auf die T-Lymphozyten<br />
zum Teil widersprüchliche Beobachtungen,<br />
die auf ein komplexes Ungleichgewicht<br />
innerhalb der T-Zell-<br />
Subpopulationen hinweisen.<br />
Der deutlich erniedrigte lösliche<br />
Interleukin-6-Rezeptor bei unserem<br />
Patienten kann durch eine, wahrscheinlich<br />
reaktiv, ehöhte Serumkonzentration<br />
von Interleukin-6 bei Patienten mit<br />
<strong>Morbus</strong> <strong>Adamantiades</strong>-Behçet erklärt<br />
werden [26]. Darüber hinaus waren<br />
Zeichen einer erhöhten Immunreaktivität<br />
beim jungen Patienten zu finden,<br />
nämlich das erhöhte Serum-IgA [10].<br />
Der Nachweis eines erhöhten Immunglobulinspiegels<br />
im Serum bei Patienten<br />
im Erkrankungsschub weist auf das<br />
Vorliegen einer polyklonalen B-Zell-<br />
Aktivierung ohne obligate begleitende<br />
Zunahme der gesamten Zellzahl hin<br />
[14, 23]. Eine mögliche Zunahme der<br />
Zahl aktivierter, nicht mehr adäquat<br />
stimulierbarer B-Lymphozyten mit<br />
gleichzeitiger Erniedrigung von ruhenden,<br />
zirkulierenden B-Lymphozyten<br />
liegt auch bei bestimmten Virusinfektionen<br />
sowie bei Autoimmunerkrankungen<br />
vor. Die meisten in den letzten<br />
Jahren erhobenen Befunde vertreten<br />
die Auffassung, daß es sich beim <strong>Morbus</strong><br />
<strong>Adamantiades</strong>-Behçet um eine Erkrankung<br />
mit gesteigerter Immunreaktivität<br />
handelt [9].<br />
Das Konzept einer Autoimmunpathogenese<br />
hat durch den Nachweis von<br />
spezifisch gegen verschiedene humane<br />
Antigene gerichtete Antikörper an Bedeutung<br />
gewonnen [18, 28]. Solche<br />
Antikörper richten sich gegen Endothelzellen,<br />
Keratinozyten der oralen<br />
Schleimhaut, neutrophile Granulozyten<br />
(ANCA), Keratinkomponenten, Glukolipide,<br />
Ganglioside, Lipopolysaccharide<br />
und Cardiolipin [2, 3, 24, 30]. Ein vaskulärer<br />
Befall kann auch durch zirkulierende<br />
Immunkomplexe verursacht<br />
werden, die sich an der Gefäßwand vieler<br />
Organe ablagern [4, 11]. Versuche,<br />
ein krankheitspezifisches Antigen aus<br />
isolierten Immunkomplexen zu identifizieren,<br />
sind bisher nicht gelungen.<br />
Für eine Beteiligung bei der Pathogenese<br />
der Erkrankung wurden Umweltschadstoffe,<br />
wie z.B. organische<br />
Phosphatverbindungen, Kupfer, polychlorierte<br />
Biphenyle und Zink, verantwortlich<br />
gemacht [19]. Allerdings erscheint<br />
eine spezifische Rolle dieser<br />
Stoffe bei der Auslösung der Erkrankung<br />
fraglich.<br />
Literatur<br />
1. <strong>Adamantiades</strong> B (1931) Sur un cas d’iritis à hypopyon<br />
récidivant. Ann Oculist (Pais)<br />
168:271–278<br />
2. Aydintug AO,Tokgöz G, D’Cruz DP, Gürler A, Cervera<br />
R, Düzgün N, Atmaca LS, Khamashta MA,<br />
Hughes GRV (1993) Antibodies to endothelial<br />
cells in patients with Behçet’s disease.<br />
Clin Immunol Immunopathol 67:157–162<br />
3. Balcan E, Özgün S, Akoglu T,Yazici H (1993)<br />
Antibodies to keratin components in patients<br />
with Behçet’s disease as compared by<br />
other rheumatological disorders. In:Wechsler<br />
B, Godeau P (eds) Behçet disease. International<br />
Congress Series 1037, Excerpta Medica, Amsterdam<br />
London New York Tokyo, pp 87–90<br />
4. Bang D, Honma T, Saito T, Nakagawa S, Ueki H, Lee<br />
S (1988) Ultrastructure of vascular changes in<br />
cutaneous manifestations of Behçet’s disease.<br />
Acta Dermatol Venereol (Stockh) 68:33–40<br />
5. Behçet H (1937) Über rezidivierende, aphthöse,<br />
durch ein Virus verursachte Geschwüre<br />
am Mund, am Auge und an den Genitalien.<br />
Dermatol Wochenschr 105:1152–1157<br />
6. Chajek-Shaul T, Pisanty S, Knobler H, Matzner Y,<br />
Glick M, Ron N, Rosenman E, Brautbar C (1987)<br />
HLA-B51 may serve as an immunogenetic<br />
marker for a subgroup of patients with Behçet’s<br />
syndrome. Am J Med 83:666–672<br />
7. Cooke BED (1979) Oral ulceration in Behçet’s<br />
syndrome. In: Lehner T, Barnes CG (eds) Behçet’s<br />
syndrome. Clinical and immunological features.<br />
Proceeding of a conference sponsored by the Royal<br />
Society of Medicine, February 1979. Academic<br />
Press, London, pp 143–149<br />
8. Dinehart S, Jorizoo JL (1988) Immunology: cellmediated<br />
immune system. In: Plotkin GR, Calabro<br />
JJ, O‘Duffy JD (eds) Behçet’s disease: a contemporay<br />
synopsis. Futura, Mount Kisco New York,<br />
pp 63–72<br />
9. Djawari D (1984) <strong>Morbus</strong> Behçet. Klinische und<br />
immunopathologische Aspekte.<br />
Zentralbl Haut 150:83–94<br />
10. Fortune F,Walker J, Lehner T (1990) The expression<br />
of γδ T cell receptor and the prevalence<br />
of primed, activated and IgA-bound T cells in<br />
Behçet’s syndrome. Clin Exp Immunol<br />
82:326–332<br />
11. Gupta Rc, O’Duffy JD, McDuffie FC, Meurer M, Jordon<br />
RE (1978) Circulating immune complexes<br />
in active Behçet’s disease. Clin Exp Immunol<br />
34:213–218<br />
12. Häfner R (1987) Das Behçet-Syndrom im Kindesalter.<br />
Z Rheumatol 46:174–178<br />
13. Hamza M (1993) Juvenile Behçet’s disease.<br />
In:Wechsler B, Godeau P (eds) Behçet’s disease. International<br />
Congress Series 1037, Excerpta Medica,<br />
Amsterdam London New York, pp 377–380
14. Hamzaoui K, Kahan A, Hamza M, Ayed K (1991)<br />
Suppressive T cell function of Epstein-Barr virus<br />
induced B cell activation in active Behçet’s<br />
disease. Clin Exp Rheumatol 9:131–135<br />
15. International Study Group for Behçet’s disease<br />
(1990) Criteria for diagnosis of Behçet’s disease.<br />
Lancet 335:1078–1080<br />
16. Jorizzo JL, Solomon AR, Cavallo T (1985) Behçet’s<br />
syndrome: immunopathologic and histopathologic<br />
assessment of pathergy lesions is<br />
useful in diagnosis and follow-up.<br />
Arch Pathol Lab Med 109:747–751<br />
17. Katzenellenbogen I, Feuermann EJ (1965)<br />
Beitrag zum M. Behçet. (Die Bedeutung der<br />
spezifischen Hauthyperreaktivität und der<br />
Behçetinreaktion). Hautarzt 16:13–18<br />
18. Lehner T, Almeida JD, Levinski RJ (1978)<br />
Damaged membrane fragments and immune<br />
complexes in the blood of patients with<br />
Behçet’s syndrome. Clin Exp Immunol<br />
34:206–212<br />
19. Plotkin GR (1988) Pathogenesis: miscellaneous<br />
factors. In: Plotkin GR, Calabro JJ, O’Duffy JD (eds)<br />
Behçet’s disease: a contemporary synopsis. Futura,<br />
Mount Kisco New York, pp 89-100<br />
20. Rakover Y, Adar H,Tal I, Lang Y, Kedar A (1989)<br />
Behçet disease: long-term follow-up of three<br />
children and review of the literature.<br />
Pediatrics 83:986–992<br />
21. Schneider DT, Jorizzo JL (1987)<br />
Behçet’s disease and complex aphthosis.<br />
Dermatol Clin5:769–778<br />
22. Shafaie N, Shahram F, Davatchi F, Akbarian M,<br />
Gharibdoost F, Nadji A (1993) Behçet’s disease<br />
in children. In:Wechsler B, Godeau P (eds) Behçet’s<br />
disease. International Congress Series 1037,<br />
Excerpta Medica, Amsterdam London New York<br />
Tokyo, pp 381–383<br />
23. Taylor PV, Chamberlain MA, Scott JS (1993) Autoreactivity<br />
in patients with Behçet’s disease.<br />
Br J Rheumatol 32:908–910<br />
24. Vaiopoulos G, Hatzinikolaou P,Tsiroyanni A, Navropoulos<br />
S, Stamatelos G,Terzoglou K,Tzonou A,<br />
Economidou I, Kaklamanis Ph (1994) Anti-neutrophil<br />
cytoplasmic antibodies in Adamantiadis-<br />
Behçet’s disease. Br J Rheumatol<br />
33:406–407<br />
25. Wechsler J,Wechsler B, Herreman G, Godeau P,<br />
Touraine R, Pinaudeau Y (1981) Maladie de Behçet.<br />
Etude en immunofluorescence de l’intradermo-réaction<br />
à l’eau distilée. Valeur diagnostique<br />
à propos de 50 malades.<br />
Med Interne 16:112–117<br />
26. Yamakawa Y, Sugita Y,Takahashi S,Takahashi Y, Nagatani<br />
T, Nakajima H (1993) Levels of Interleukin-6<br />
in patients with Behçet’s disease.<br />
J Invest Dermatol 101:446<br />
27. Yazici H, Chamberlain MA,Tüzün Y,Yurdakul S,<br />
Müftüoglu A (1984) A comparative study of the<br />
pathergy reaction among turkish and british<br />
patients with Behçet’s disease.<br />
Ann Rheum Dis 43:74–75<br />
28. Zouboulis ChC (1995) <strong>Morbus</strong> <strong>Adamantiades</strong>-<br />
Behçet. Klinische und experimentelle Befunde<br />
von 53 Patienten aus dem Berliner Raum.<br />
Habilitationsschrift, Universitäts-Hautklinik und<br />
Poliklinik, <strong>Klinikum</strong> Benjamin Franklin, Freie Universität<br />
Berlin<br />
29. Zouboulis ChC, Büttner P, Djawari D, Kirch W, Keitel<br />
W, Garbe C, van Keyserlingk-Eberius H-J, Orfanos<br />
CE (1993) HLA-Muster bei <strong>Morbus</strong> <strong>Adamantiades</strong>-<br />
Behçet in Deutschland: Assoziation zum<br />
Auftreten, der klinischen Symptomatik und<br />
dem Krankheitsverlauf bei 39 Patienten.<br />
Hautarzt 44:81–84 und 256 (Erratum)<br />
30. Zouboulis ChC, Büttner P,Tebbe B, Orfanos CE<br />
(1993) Anticardiolipin antibodies in <strong>Adamantiades</strong>-Behçet’s<br />
disease. Br J Dermatol<br />
128:281–284<br />
&misc:Eingegangen am 22. Februar 1996<br />
Angenommen am 15.Mai 1996<br />
Der Hautarzt 4·97 | 261