Tuyển tập 50 đề thi học sinh giỏi môn hóa học 8 (kèm đáp án) (by Dameva)
LINK BOX: https://app.box.com/s/rvs4eb986tqjlrcpkpj6dzzupgy7yjxk LINK DOCS.GOOGLE: https://drive.google.com/file/d/1OZDfkEZFqAU2HROfc84yI_G0tRcYVpdf/view?usp=sharing
LINK BOX:
https://app.box.com/s/rvs4eb986tqjlrcpkpj6dzzupgy7yjxk
LINK DOCS.GOOGLE:
https://drive.google.com/file/d/1OZDfkEZFqAU2HROfc84yI_G0tRcYVpdf/view?usp=sharing
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
https://twitter.com/daykemquynhon<br />
www.facebook.com/daykem.quynhon<br />
plus.google.com/+DạyKèmQuyNhơn<br />
http://daykemquynhon.blogspot.com<br />
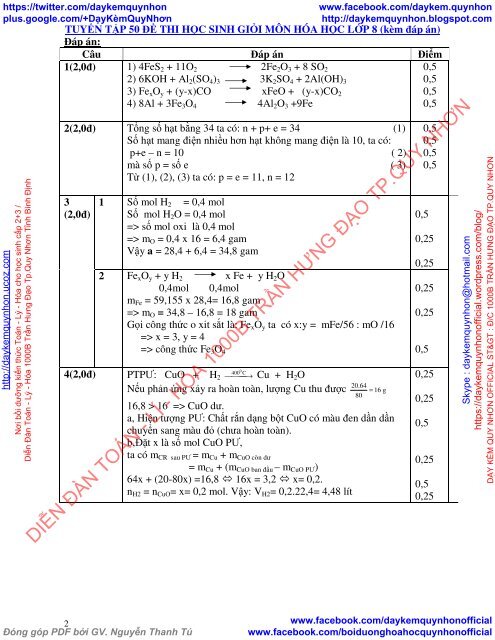
TUYỂN TẬP <strong>50</strong> ĐỀ THI HỌC SINH GIỎI MÔN HÓA HỌC LỚP 8 (<strong>kèm</strong> <strong>đáp</strong> <strong>án</strong>)<br />
Đáp <strong>án</strong>:<br />
Câu Đáp <strong>án</strong> Điểm<br />
1(2,0đ) 1) 4FeS 2 + 11O 2 2Fe 2 O 3 + 8 SO 2<br />
0,5<br />
2) 6KOH + Al 2 (SO 4 ) 3 3K 2 SO 4 + 2Al(OH) 3<br />
0,5<br />
3) Fe x O y + (y-x)CO xFeO + (y-x)CO 2<br />
0,5<br />
4) 8Al + 3Fe 3 O 4 4Al 2 O 3 +9Fe<br />
0,5<br />
http://daykemquynhon.ucoz.com<br />
Nơi bồi dưỡng kiến thức To<strong>án</strong> - Lý - Hóa cho <strong>học</strong> <strong>sinh</strong> cấp 2+3 /<br />
Diễn Đàn To<strong>án</strong> - Lý - Hóa 1000B Trần Hưng Đạo Tp.Quy Nhơn Tỉnh Bình Định<br />
2(2,0đ) Tổng số hạt bằng 34 ta có: n + p+ e = 34 (1)<br />
Số hạt mang điện nhiều hơn hạt không mang điện là 10, ta có:<br />
p+e – n = 10 ( 2)<br />
mà số p = số e ( 3)<br />
Từ (1), (2), (3) ta có: p = e = 11, n = 12<br />
3<br />
(2,0đ)<br />
1 Số mol H 2 = 0,4 mol<br />
Số mol H 2 O = 0,4 mol<br />
=> số mol oxi là 0,4 mol<br />
=> m O = 0,4 x 16 = 6,4 gam<br />
Vậy a = 28,4 + 6,4 = 34,8 gam<br />
2 Fe x O y + y H 2 x Fe + y H 2 O<br />
0,4mol 0,4mol<br />
m Fe = 59,155 x 28,4= 16,8 gam<br />
=> m O = 34,8 – 16,8 = 18 gam<br />
Gọi công thức o xit sắt là: Fe x O y ta có x:y = mFe/56 : mO /16<br />
=> x = 3, y = 4<br />
=> công thức Fe 3 O 4<br />
4(2,0đ) PTPƯ: CuO + H 2 ⎯<br />
4000 ⎯⎯<br />
C → Cu + H 2 O<br />
Nếu phản ứng xảy ra hoàn toàn, lượng Cu thu được<br />
20.64<br />
= 16 g<br />
80<br />
16,8 > 16 => CuO dư.<br />
a, Hiện tượng PƯ: Chất rắn dạng bột CuO có màu đen dần dần<br />
chuyển sang màu đỏ (chưa hoàn toàn).<br />
b,Đặt x là số mol CuO PƯ,<br />
ta có m CR sau PƯ = m Cu + m CuO còn dư<br />
= m Cu + (m CuO ban đầu – m CuO PƯ )<br />
64x + (20-80x) =16,8 16x = 3,2 x= 0,2.<br />
n H2 = n CuO = x= 0,2 mol. Vậy: V H2 = 0,2.22,4= 4,48 lít<br />
DIỄN ĐÀN TOÁN - LÍ - HÓA 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
0,5<br />
0,5<br />
0,5<br />
0,5<br />
0,5<br />
0,25<br />
0,25<br />
0,25<br />
0,25<br />
0,5<br />
0,25<br />
0,25<br />
0,5<br />
0,25<br />
0,5<br />
0,25<br />
Skype : daykemquynhon@hotmail.com<br />
https://daykemquynhonofficial.wordpress.com/blog/<br />
DẠY KÈM QUY NHƠN OFFICIAL ST> : Đ/C 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
2<br />
Đóng góp PDF bởi GV. Nguyễn Thanh Tú<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial