énoncé - Chimie - PCSI
énoncé - Chimie - PCSI
énoncé - Chimie - PCSI
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Lycée Janson<br />
de Sailly<br />
Année scolaire<br />
2012/2013<br />
Classes de <strong>PCSI</strong> 5,6,7<br />
option PSI<br />
Durée de l’épreuve : 2 heures<br />
Usage des calculatrices : autorisé<br />
Devoir surveillé<br />
de chimie n°5<br />
On rappelle que les réponses doivent être justifiées avec concision et les résultats principaux doivent<br />
être encadrés.<br />
Équilibres en solution aqueuse<br />
I) Étude de l’acide pyrophosphorique<br />
L’acide pyrophosphorique est un tétraacide de formule brute H 4P 2O 7, que l’on notera H 4A.<br />
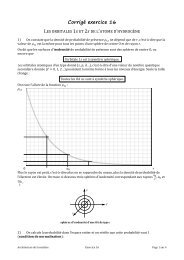
Le diagramme de distribution des espèces acido-basiques issues de l’acide pyrophosphorique est<br />
donné sur le schéma suivant :<br />
1) Attribuer les différentes courbes A à E.<br />
2) Donner la valeur des p
L’ammoniac et l’ammoniaque<br />
II) Réalisation d’un tampon ammoniacal<br />
Dans les conditions usuelles du laboratoire, l’ammoniac, NH 3, est un gaz, très irritant pour les<br />
muqueuses. La température d’ébullition de l’ammoniac est de −33℃, alors que celle de l’eau est de<br />
+100℃.<br />
1) Les deux molécules ont une taille et une masse molaire très proches. Comment peut-on<br />
expliquer une telle différence des températures d’ébullition ?<br />
2) L’ammoniac est très soluble dans l’eau. Interpréter.<br />
Une solution aqueuse concentrée d’ammoniac porte le nom courant d’ammoniaque. On l’utilise comme<br />
nettoyant ou détachant.<br />
Une bouteille commerciale d’un litre d’ammoniaque comporte les indications suivantes : densité
III) Complexation de l’ion argent (I) avec plusieurs ligands<br />
Pour éliminer les ions Ag + lors du traitement d’une ancienne pellicule photographique, on envisage la<br />
complexation avec deux types de ligands : l’ion thiosulfate S 2O 3 2− et l’ion cyanure CN − .<br />
1) Écrire la structure de Lewis de l’ion thiosulfate S 2O 3 2− (l’atome central est un atome de soufre, le<br />
soufre étant l’élément situé sous l’oxygène dans la classification périodique). Déterminer la<br />
géométrie de cet anion. Montrer qu’il peut jouer le rôle de ligand, et préciser par quel atome se<br />
fait la coordination avec les ions Ag + .<br />
Les complexes de l’ion Ag + avec les ligands thiosulfate et cyanure ont pour formules respectives<br />
[Ag(S 2O 3) 2 ] 3− (de constante de dissociation globale