CORRECTIONS EXERCICES CHAPITRE VII - Poly-Prepas
CORRECTIONS EXERCICES CHAPITRE VII - Poly-Prepas
CORRECTIONS EXERCICES CHAPITRE VII - Poly-Prepas
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
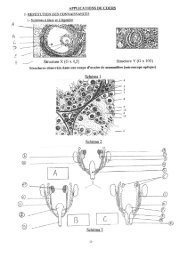
Exercice 5 :<br />
Exploitation du Document 1 :<br />
Le Document 1 représente un diagramme en bâtons montrant l’évolution au cours du temps des qualités du<br />
virus de l’immunodéficience humaine (VIH) et d’anticorps spécifiques chez un individu séropositif au cours<br />
du temps (en années)<br />
On constate qu’au bout de 3 semaines après l’introduction du virus dans l’organisme, celui-ci prolifère<br />
intensément.<br />
L’analyse du graphique montre qu’il y a une production importante d’anticorps anti-VIH suite à l’infection.<br />
Celle-ci est efficace car la quantité de virus diminue de façon spectaculaire.<br />
Cependant à partir de la huitième année qui suit l’infestation, le virus recommence à proliférer et on observe<br />
une diminution rapide du taux d’anticorps anti-VIH. Ce taux est pratiquement nul au bout de la dixième<br />
année.<br />
Interprétation :<br />
Nous pouvons expliquer la première phase (production d’anticorps anti-VIH et diminution du taux de virus<br />
dans l’organisme) par la mise en place d’une réponse immunitaire à médiation humorale (RIMH). Les<br />
lymphocytes B reconnaissent en effet les antigènes viraux ; stimulés, ils subissent une phase de<br />
multiplication et se différencient en plasmocytes sécréteurs d’Ac. Anticorps et antigènes viraux forment des<br />
complexes immuns qui seront éliminés par phagocytose.<br />
Comment peut-on expliquer la seconde phase marquée par l’inhibition de la RIMH et l’augmentation du<br />
nombre des virus ?<br />
Exploitation du Document 2 :<br />
Le Document 2 se présente sous la forme d’un graphique montrant l’évolution du nombre de LT4 et LT8<br />
cultivés en présence de virus du SIDA en fonction du nombre de jours après exposition.<br />
On constate que parmi les lymphocytes la cible privilégiée du VIH est le lymphocyte LT4. Par contre, les<br />
LT8, dans le laps de temps que dure l’expérience, ne semblent pas être affectés par la présence du virus.<br />
Interprétation :<br />
Les chercheurs ont montré qu’il existait une très forte affinité entre les protéines de surface du VIH (gp120)<br />
pour la protéine CD4 présente à la surface des lymphocytes LT4 (mais aussi des macrophages). Cette<br />
particularité favorise l’entrée du virus dans ce type cellulaire.<br />
Ces LT4 constituent le pivot des réponses immunitaires, ils jouent un rôle central dans la mise en place des<br />
réponses immunitaires.<br />
Comment le démontrer ?<br />
Exploitation du Document 3 :<br />
1
L’analyse du Document 3 montre que seul le lot n°3 présente une RIMH caractérisée par l’existence<br />
d’anticorps antivirus. Ce lot correspond à des souris irradiées mais celle-ci ont reçu des LT et des LB.<br />
Par comparaison avec les résultats apportés par les autres lots, on peut en déduire :<br />
- que la réponse immunitaire est SPECIFIQUE : elle nécessite la présence de lymphocytes chez les<br />
animaux irradiés (lot n°4) ;<br />
- que la présence des seuls lymphocytes T n’engendre pas de production d’anticorps (lot n°1)<br />
- que la présence des seuls lymphocytes B ne conduit pas non plus à la production d’anticorps (lot<br />
n°2)<br />
Interprétation :<br />
La mise ne place d’une RIMH nécessite une coopération cellulaire entre LT et LB. On sait que les LT qui<br />
interviennent ici sont les LT4 qu’on qualifie également de lymphocyte auxiliaire (ou herlper).<br />
Conclusion :<br />
L’introduction du virus dans l’organisme entraîne une reconnaissance directe par les LB qui sont activés.<br />
Les LT4 reconnaissent également le virus, mais de façon indirecte celle-ci nécessite que l’antigène viral soit<br />
présenté en association avec les éléments du complexe majeur d’histocompatibilité de classe II. Les LT4<br />
alors activés libèrent des interleukines qui stimulent les LB en provoquant leur expansion clonale et leur<br />
différenciation en plasmocytes sécréteurs d’anticorps en grande quantité.<br />
Toutes ces indications permettent d’interpréter le Document n°1 et l’évolution de la maladie chez un<br />
individu infecté par le VIH. La RIMH permet une diminution de la quantité de VIH.<br />
Au bout d’un certain nombre d’années, l’activité virale, même réduite, contribue à appauvrir l’organisme en<br />
LT4 qui sont une cible privilégiée (Document 2). La RIMH en devient de moins en moins efficace et ne se<br />
produit finalement plus du fait de la quasi disparition des LT4. L’organisme, affaibli par cette profonde<br />
défaillance de la réponse immunitaire, est le siège de maladies opportunistes, ce qui entraînera sa mort à<br />
court terme.<br />
Exercice 6 :<br />
Les lymphocytes sont des cellules sanguines, issues d’une cellule souche commune de la moelle épinière.<br />
Les lymphocytes « précurseurs » sont impossibles à distinguer. Certains quittent la moelle épinière et<br />
migrent vers d’autres organes. Ils acquièrent alors le pouvoir de reconnaître un Ag spécifique par un<br />
processus de maturation. Cette maturation a lieu dans la moelle rouge des os pour les LB, et dans le thymus<br />
pour les LT.<br />
Les LB, après stimulation antigénique, se transforment en plasmocytes, cellules sécrétrices d’Ac. Les LT<br />
stimulés acquièrent d’autres spécialisations. Les LT4 sont indispensables aux placmocytes et aux LT<br />
cytotoxiques.<br />
Lymphocytes B<br />
Lymphocytes T<br />
Organe producteur original Moelle rouge des os longs<br />
Moelle rouge des os longs,<br />
puis thymus<br />
Organes lymphoïdes<br />
secondaires<br />
Ganglions lymphatiques, rate Ganglions lymphatiques, rate<br />
Récepteurs de surface Immunoglobulines IgS Récepteurs T<br />
Effets d’une stimulation<br />
antigénique<br />
Mitoses, spécialisation<br />
cellulaire<br />
Mitoses, spécialisation<br />
cellulaire<br />
2
Types cellulaires dérivés<br />
Capacité à produire des<br />
anticorps<br />
Plasmocytes<br />
Lymphocytes helper,<br />
lymphocytes cytotoxiques<br />
+ -<br />
Exercice 7 :<br />
1. Un Ac est une protéine complexe dont la structure moléculaire de base (Ig) est constituée de 4 chaînes<br />
polypeptidiques identiques 2 à 2 :<br />
- 2 chaînes lourdes (440 A.A.)<br />
- 2 chaînes légères (220 A.A.)<br />
Les 2 chaînes sont reliées par des ponts disulfures (S-S) il existe :<br />
- une zone variable par laquelle l’Ig pourra fixer un fragment de la molécule d’Ag ou épitope : c’est la zone<br />
Fab (on parle aussi de paratope). Il existe 2 sites de fixation de l’Ag par molécule d’Ig ;<br />
- une zone constante identique pour toutes les molécules d’Ig : c’est le fragment Fc.<br />
2. Il existe 2 catégories d’Ac : les Ac fixés à la surface des lymphocytes B (ou des mastocytes) et les Ac<br />
libres (ou circulants). Bien que l’énoncé ne le formule pas expressement, il semble que la question concerne<br />
plus particulièrement les Ac circulants.<br />
Les Ac circulants sont sécrétés par les plasmocytes. A l’origine, on trouve des LB qui sont sélectionnées,<br />
activés et sièges d’une expansion clonale. Ils se différencient ensuite en plasmocytes. C’est alors au sein de<br />
ceux-ci que s’effectue la synthèse d’Ac circulants selon le processus général de synthèse des protéines :<br />
- transcription du gène dans le noyau sous forme d’ARNm<br />
- transfert de l’ARNm dans le cytoplasme<br />
- traduction de l’ARNm en chaîne polypeptidique au niveau d’un ribosome<br />
- passage de la chaîne polypeptidique dans les cavités du REG<br />
- formation de vésicules au niveau des dictyosomes de l’appareil de Golgi<br />
- libération par exocytose<br />
3
3. En présence d’un Ag étranger, les LB compétents sont sélectionnés et stimulés à la suite d’une<br />
reconnaissance directe de l’Ag (par les IgM).<br />
La phase de multiplication clonale est suivie de la différenciation en plasmocytes qui sécrètent les Ac<br />
circulants en abondance. Les Ig libérés dans le milieu intérieur ont pour rôle de neutraliser les Ag en<br />
formant des complexes immuns. La formation de ces complexes immuns va avoir plusieurs conséquences :<br />
- la neutralisation des Ag solubles<br />
- une aide à la phagocytose : le complexe immun se fixe par l’intermédiaire de la région de l’Ig sur un<br />
macrophage.<br />
4. Dans l’expérience du Document 1, lorsque l’on fait intervenir les cellules de la rate séparément ou<br />
ensemble, on obtient des résultats différents.<br />
Lorsque les lymphocytes seuls ou les macrophages seuls sont mis en présence des GRM, il n’y a aucune<br />
cellule sécrétrice d’Ac anti-GRM. Lorsque les lymphocytes et les macrophages sont mis simultanément en<br />
présence des GRM, il y a de nombreuses cellules sécrétrices d’Ac anti-GRM.<br />
On en conclut que la coopération des lymphocytes et des macrophages est indispensable à la production<br />
d’Ac donc indispensable à la réponse immunitaire contre les GRM.<br />
5. Les résultats nous montrent que les LB seuls entraînent une réponse immunitaire faible (que 72 cellules)<br />
et qu’une coopération cellulaire entre LB et LT est nécessaire pour une réponse efficace (960 cellules). De<br />
plus, cette coopération qui consiste en une stimulation des LB par les LT se fait par production de molécules<br />
sécrétées par les LT qui ont pu traverser la membrane. Ces molécules sont des interleukines qui<br />
correspondent à des protéines et qui agissent à distance (communication intercellulaire).<br />
Exercice 8 :<br />
1. Tout composant étranger introduit dans un organisme déclenche en quelques jours l’apparition d’Ac<br />
dirigés contre lui. Les GRM et les GRP injectés aux souris normales sont donc des Ag libres. Certains LB<br />
vierges présents dans la souris au moment de l’injection possédaient dans Ac membranaires dirigés contre<br />
des déterminants antigéniques de ces GR et ont subi une expansion clonale et une différenciation en<br />
plasmocytes sécréteurs d’Ac anit-GRM et anti-GRP.<br />
4
2. Les souris Si sont immunodéficients, le traitement qu’elles ont subi inhibe leurs RI et malgré<br />
l’introduction d’un Ag étranger elles ne sécrètent pas d’Ac. Les clones de LB spécifiques des GRM et les<br />
clones spécifiques des GRP n’existe pas chez cette souris Si ou bien ils sont incapables de s’activer.<br />
3.<br />
Souris Si1 : Lorsqu’on prélève les lymphocytes de la souris Sn qui n’a jamais été mise en présence des<br />
GRP ou des GRM, on lui prélève indifféremment tous ses lymphocytes (LT4, LT8, LB). Certains de ces<br />
lymphocytes, introduits dans une souris Si1, qui normalement ne sécrète pas d’Ac, vont sécréter des Ac<br />
anti-GRM et des Ac anti-GRP. Il existait donc parmi les lymphocytes prévelés à la souris Sn des LB<br />
reconnaissant spécifiquement les GRP et d’autres reconnaissant spécifiquement les GRM. Lorsque la souris<br />
Si1 a été mise en présence de GRP et de GRM, ces clones de LB ont subi une expansion clonale et une<br />
différenciation en plasmocytes sécréteurs d’Ac.<br />
Souris Si2 : Les lymphocytes prélevés à la souris Sn sont encore une fois de toutes les spécificités.<br />
Lorsqu’on met en présence ces lymphocytes avec des GRM, certains de ces lymphocytes s’y fixent. Les<br />
GRM étant des Ag libres, seuls des LB spécifiques des GRM peuvent les reconnaître. Lorsqu’on introduit<br />
dans la souris Si2 des lymphocytes libres, on lui introduit donc tous les lymphocytes de la souris Sn, excepté<br />
les LB anti-GRM. Losqu’on inocule des GRM et des GRP à la souris Si2, celle-ci possède des clones de LB<br />
anti-GRP et sécrète donc des anticorps anti-GRP, mais ne possède aucun clone de LB anti-GRM et ne<br />
sécrète pas d’Ac anti-GRM.<br />
Souris Si3 : Le raisonnement reste le même que sur la souris Si2.<br />
Exercice 9 :<br />
1. Les acteurs intervenant ici sont ceux de l’immunité acquise, ces acteurs ne sont pas immédiatement<br />
mobilisables lors d’une première rencontre avec l’Ag, c’est pourquoi, on attend 15 jours entre le 1 ier contact<br />
avec l’Ag et le 2 nd .<br />
2. Les réactions mises en jeu permettent la lutte contre des Ag libres, les toxines, circulant dans le milieu<br />
intérieur. Les agents permettant le maintien de l’intégrité du milieu extracellulaire sont les Ac. Les cellules<br />
mises en jeu sont donc les LB qui se différencient en plasmocytes sécréteurs d’Ac, et en LB mémoire.<br />
3. La vaccination est une technique de protection préventive contre les infections. Elle consiste à mimer une<br />
réponse immunitaire primaire, en utilisant, non pas un véritable agent pathogène, mais un leurre de cet agent<br />
qui peut être le pathogène tué, très affaiblit ou encore des fragments de ce pathogène. Dans l’expérience<br />
présentée, ce leurre est l’anatoxine tétanique. La réaction primaire provoque une expansion clonale des<br />
lymphocytes sélectionnés (ici des LB anti-toxine tétanique) et une différenciation de ces lymphocytes (ici en<br />
plasmocytes et en LB mémoires).<br />
Les agents de l’immunité acquise ne sont pas immédiatement mobilisables lors d’une première rencontre<br />
avec l’Ag et mettront un peu de temps avant d’être induits.<br />
Ainsi, si la 1 ière rencontre avec l’Ag ne concerne par un leurre mais un véritable pathogène, l’induction des<br />
réactions immunitaires acquises sera trop lente et la maladie peut l’emporter. C’est le cas des 2 souris du cas<br />
A qui meurent si on leur injecte directement la TT ou la TD.<br />
La 2 nde rencontre avec l’Ag résulte cette fois-ci d’un Ag réellement néfaste, la réponse secondaire s’appuie<br />
sur les lymphocytes mémoire (ici les LB mémoire) induits lors de la réponse primaire. Cette réponse<br />
secondaire est plus rapidement mise en place et elle est quantitativement plus importante que la réponse<br />
5
primaire. La souris B qui a effectué une réponse primaire grâce à l’anatoxine résiste à l’injection de toxine<br />
tétanique et survit.<br />
La vaccination ne protège l’individu vacciné que d’un seul pathogène, elle est spécifique. Ainsi, dans<br />
l’expérience, l’inoculation d’anatoxine tétanique ne protège pas de la TD.<br />
Exercice 10 :<br />
1. On appelle Ag une molécule susceptible d’être reconnue comme étrangère par le système immunitaire et<br />
de déclencher une réaction spécifique contre elle. Les molécules antigéniques sont principalement des<br />
protéines et des glycoprotéines. On distingue :<br />
- les Ag particulaires constituant des cellules étrangères (bactéries, particules virales, champignons) et les<br />
allergènes (poussières, acariens, tous les facteurs d’allergies) ;<br />
- les Ag solubles, molécules libres (toxines, protéines sériques)<br />
2. Le sérum antitétanique renferme des Ac spécifiques capables de neutraliser la toxine tétanique<br />
3. Le vaccin anti-tétanique renferme des anatoxines tétaniques, c’est-à-dire des toxines tétaniques qui ont<br />
perdu leur pouvoir pathogène mais qui ont gardé leur pouvoir vaccinant ou pouvoir immunogène.<br />
4. L’enfant est protégé jusqu’au troisième mois par les Ac antitétaniques qu’il a reçu de sa mère immunisée.<br />
Ces Ac sont capables de traverser le placenta lors de la grossesse.<br />
5. L’analyse du graphique montre que l’injection de sérum augmente le taux plasmatique d’antitoxine<br />
tétanique très rapidement (taux maximal une semaine après l’injection) mais de façon temporaire, 7<br />
semaines après l’injection, ce taux est quasi-nul. Le rôle du sérum est donc de conférer à l’organisme une<br />
immunité passive, immédiate et temporaire.<br />
6. L’analyse du graphique montre que l’injection de vaccin provoque une augmentation progressive et<br />
différée du taux d’antitoxine tétanique (taux maximal après 3 à 4 semaines après l’injection). Chaque<br />
nouvelle injection provoque une augmentation du taux d’antitoxine tétanique. Chaque injection de vaccin<br />
stimule le système immunitaire qui se met alors à produire des taux croissants d’antitoxine tétanique. Les<br />
rôles du vaccin est donc de conférer à l’organisme une immunité active et permanente.<br />
7. Le mécedin a pratiqué tout d’abord une sérothérapie afin de détruire immédiatement une éventuelle<br />
contamination par la toxine tétanique puis une vaccination qui protégera durablement le patient contre<br />
d’éventuelles contaminations ultérieures.<br />
6