- Page 1:
IL LEGAME CHIMICO“Fra due atomi o
- Page 4 and 5:
Le forze attrattive dei nucleipreva
- Page 6 and 7:
LEGAME IONICOIl legame ionico è un
- Page 9 and 10:
E ab : energia tra due cariche Z a
- Page 11 and 12:
Energia di formazione della coppia
- Page 13 and 14:
Solidi ioniciI solidi ionici sono c
- Page 15 and 16:
LEGAME COVALENTEUn legame covalente
- Page 17 and 18:
Regola dell’ottettoOgni atomo che
- Page 19 and 20:
Struttura di Lewis di F 2F+FF F7e -
- Page 21 and 22:
Legame covalente polareLa condivisi
- Page 23:
Modello ionico e covalenteNaCl H 2
- Page 26:
L’entità del dipolo elettrico si
- Page 33 and 34:
Legami multipliordine di legame = n
- Page 35 and 36:
Forza di un legame covalente aument
- Page 37 and 38:
Eccezioni alla regola dell’ottett
- Page 39:
Risonanza (mulo!!!)Utilizzando le r
- Page 42:
Eccezioni alla regola dell’ottett
- Page 45:
TEORIA VSEPRVSEPR = Valence Shell E
- Page 51 and 52:
Le repulsioni esercitate tra coppie
- Page 54:
Il metano è tetraedrico con angli
- Page 63 and 64:
Teoria del Legame di Valenza(Valenc
- Page 85 and 86: l’orbitale 1s ha simmetriasferica
- Page 87 and 88: La geometria tetraedrica deriva dal
- Page 89 and 90: Ibridazione a formare legami di tip
- Page 91 and 92: La sovrapposizione di questi orbita
- Page 93 and 94: Ibridazione a formare legami di tip
- Page 95 and 96: Ibridazione a formare legami di tip
- Page 99: B 2 H 63LiBH 4 +4BF 3 →2B 2 H 6 +
- Page 102: Gli orbitali molecolari si estendon
- Page 116 and 117: 4 *C2p2p *3O2pC2s1p2 *O2s1
- Page 119 and 120: Legame MetallicoI metalli costituis
- Page 121 and 122: Forze interioniche edintermolecolar
- Page 124 and 125: dipolo -dipolo indotto
- Page 126 and 127: dipolo istantaneo-dipolo istantaneo
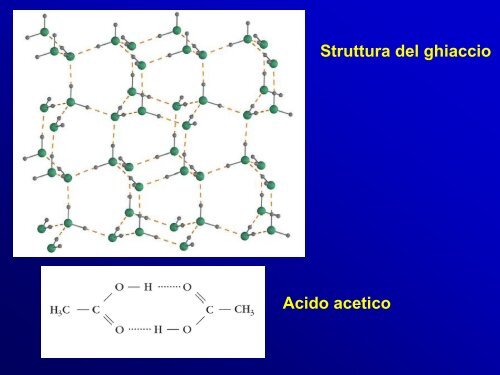
- Page 128 and 129: L’AcquaIl momento di dipolo perma