25/11/2012 – Tabelas de unidades de medida
* Anexo do primeiro estudo de medidas. Um grande número de tabelas com relações métricas, números, constantes, tudo para facilitar a vida dos estudantes de física e das demais ciências que dependem de medidas.
* Anexo do primeiro estudo de medidas. Um grande número de tabelas com relações métricas, números, constantes, tudo para facilitar a vida dos estudantes de física e das demais ciências que dependem de medidas.
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
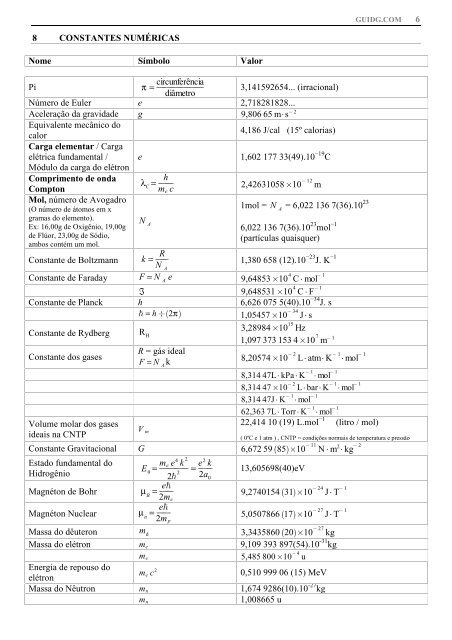
8 CONSTANTES NUMÉRICAS<br />
Nome Símbolo Valor<br />
Pi π = circunferênciaf<br />
diâmetro<br />
3,141592654... (irracional)<br />
Número <strong>de</strong> Euler e 2,718281828...<br />
Aceleração da gravida<strong>de</strong> g @ 2<br />
9,806 65 mAs<br />
Equivalente mecânico do<br />
calor<br />
Carga elementar / Carga<br />
4,186 J/cal (15º calorias)<br />
elétrica fundamental /<br />
Módulo da carga do elétron<br />
e 1,602 177 33(49).10 −19 C<br />
Comprimento <strong>de</strong> onda<br />
Compton<br />
λC = h f<br />
me c<br />
2,42631058B10 @ 12 Mol, número <strong>de</strong> Avogadro<br />
(O número <strong>de</strong> átomos em x<br />
m<br />
gramas do elemento).<br />
Ex: 16,00g <strong>de</strong> Oxigênio, 19,00g<br />
N A<br />
6,022 136 7(36).10<br />
<strong>de</strong> Flúor, 23,00g <strong>de</strong> Sódio,<br />
ambos contém um mol.<br />
23 mol −1<br />
(partículas quaisquer)<br />
1mol = N A = 6,022 136 7(36).10 23<br />
Constante <strong>de</strong> Boltzmann k = R f<br />
1,380 658 (12).10<br />
N A<br />
−23 J. K −1<br />
Constante <strong>de</strong> Faraday F = N A e 9,64853B10 4 @ 1<br />
CA mol<br />
ℑ 9,648531B10 4 @ 1<br />
CA F<br />
Constante <strong>de</strong> Planck h 6,626 075 5(40).10 −34 ` a<br />
- = hD 2π<br />
J. s<br />
1,05457B10 @ 34 JA s<br />
Constante <strong>de</strong> Rydberg RH 3,28984B10 15 Hz<br />
1,097 373 153 4B10 7 @ 1 m<br />
Constante dos gases<br />
Volume molar dos gases<br />
i<strong>de</strong>ais na CNTP<br />
R = gás i<strong>de</strong>al<br />
F = N A k<br />
V m<br />
8,20574B10 @ 2 LA atmA K @ 1 @ 1<br />
A mol<br />
8,314 47LA kPaA K @ 1 @ 1<br />
A mol<br />
8,314 47B10 @ 2 LA barA K @ 1 @ 1<br />
A mol<br />
8,314 47JA K @ 1 @ 1<br />
A mol<br />
62,363 7LA TorrA K @ 1 @ 1<br />
A mol<br />
22,414 10 (19) L.mol −1 (litro / mol)<br />
GUIDG.COM 6<br />
( 0ºC e 1 atm ) , CNTP = condições normais <strong>de</strong> temperatura e pressão<br />
` a @ <strong>11</strong> 2 @ 2<br />
Constante Gravitacional G 6,672 59 85B10<br />
NA mA kg<br />
Estado fundamental do<br />
Hidrogênio<br />
E 0 = me e 4 k 2<br />
Magnéton <strong>de</strong> Bohr μ B = e-<br />
Magnéton Nuclear<br />
2- 2<br />
f e<br />
= 2 kf<br />
13,605698(40)eV<br />
2a0 f ` a @ 24 @ 1<br />
9,2740154 31B10<br />
JA T<br />
2me<br />
μ = n e-f<br />
2m<br />
5,0507866 17<br />
p<br />
` a B10 @ 27 JA T @ 1<br />
` a B10 @ 27 kg<br />
Massa do dêuteron md 3,3435860 20<br />
Massa do elétron me 9,109 393 897(54).10 -31 kg<br />
me 5,485 800B10 @ 4 u<br />
Energia <strong>de</strong> repouso do<br />
elétron<br />
me c 2 0,510 999 06 (15) MeV<br />
Massa do Nêutron mn 1,674 9286(10).10 -27 kg<br />
mn 1,008665 u