- Page 1 and 2: МИНИСТЕРСТВО ОБРАЗ
- Page 3: ТерминТермины, усл
- Page 6 and 7: Продолжение табл.11
- Page 8 and 9: Продолжение табл.1С
- Page 11 and 12: Продолжение таблиц
- Page 13 and 14: 1.2. Металлы. Краткие
- Page 15 and 16: е) Действие щелочей
- Page 18 and 19: N m - ne → N n+ m; N m + me → N
- Page 20 and 21: Номенклатура оксид
- Page 22 and 23: в) Взаимодействие с
- Page 24 and 25: общую схему.Безраз
- Page 26 and 27: Этим же способом мо
- Page 28 and 29: например:HCl H 2 S HNO 3 H
- Page 30: в) Взаимодействие с
- Page 33 and 34: FeOHClAl(OH) 2 Br- гидрокси
- Page 35 and 36: 9) Взаимодействием
- Page 37 and 38: Кислая соль реагир
- Page 39 and 40: 1. Известо, что мета
- Page 41 and 42: Задача № 5. Состави
- Page 43 and 44: рые образуют амфот
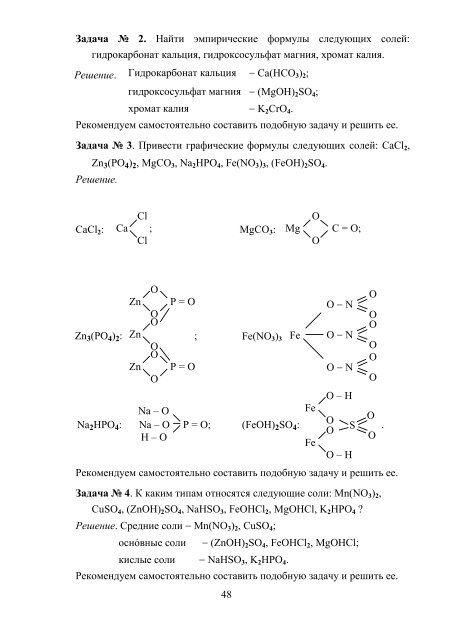
- Page 45 and 46: Задача № 2. Найти эм
- Page 47: SO 2 + HCl ↛;Mg(OH) 2 + 2HCl = Mg
- Page 51 and 52: 5. Какие из перечисл
- Page 53 and 54: 29. К раствору, содер
- Page 55 and 56: Решение. Применим п
- Page 57 and 58: 2.1.2. Задачи для само
- Page 59 and 60: Задача № 4. Вывод хи
- Page 61 and 62: 6. При сжигании 6,2 г
- Page 63 and 64: 2.4. Расчеты по уравн
- Page 65 and 66: Предположим, что ко
- Page 67 and 68: Член уравнения, сод
- Page 69 and 70: 2.5.2 Задачи для само
- Page 71 and 72: m O = m оксида - m Al = 9,44
- Page 73 and 74: Уравнение химическ
- Page 75 and 76: Задача № 6. Дать пол
- Page 77 and 78: 9. Какие элементы от
- Page 79 and 80: Решение. Молекула NC
- Page 81 and 82: CaF 2 : ΔЭО = ЭО (F) - ЭО (C
- Page 83 and 84: 6. ТЕРМОХИМИЧЕСКИЕ
- Page 85 and 86: Решение. Уравнение
- Page 87 and 88: Решение. Рассчитае
- Page 89 and 90: В стандартных усло
- Page 91 and 92: Пример 2. Какой окси
- Page 93 and 94: где k пр - константа
- Page 95 and 96: Аррениуса:Задача №
- Page 97 and 98: [NH 3 ]Решение. K.3[N ] [H ]
- Page 99 and 100:
2) Увеличение конце
- Page 101 and 102:
8. КОНЦЕНТРАЦИЯ РАС
- Page 103 and 104:
Решение.M H 2 SO 4= 98 г/м
- Page 105 and 106:
Vрра3 49 300 10098 1000 1,8424,4
- Page 107 and 108:
Решение. Выведем фо
- Page 109 and 110:
nЭ, AnnЭ, BЭ,CmmCmЭBAAmЭmЭCCB
- Page 111 and 112:
VH2SO4CBa(OH)2nOHVBa(OH)210 C% ρ
- Page 113 and 114:
откудаmK2Cr2O7mH2OR20K Cr O10
- Page 115 and 116:
9. ЭЛЕКТРОЛИТИЧЕСКА
- Page 117 and 118:
Задача № 5. Рассчит
- Page 119 and 120:
ОтсюдаKIд,H2S[H[H22]S].[H]KI
- Page 121 and 122:
Таким образом, посл
- Page 123 and 124:
8. Написать молекул
- Page 125 and 126:
Решение. Для слабог
- Page 127 and 128:
Примем концентраци
- Page 129 and 130:
[Pb +2 ] = X[Cl¯] = 2X.т.к.ПР
- Page 131 and 132:
Пример 6. В каком на
- Page 133 and 134:
2FeOH + + SO -2 4 + 2H 2 O ⇄ 2Fe(
- Page 135 and 136:
Предположив, что со
- Page 137 and 138:
II AlOH 2+ + H 2 O ⇄ Al(OH) + 2 +
- Page 139 and 140:
Задача № 2. Определ
- Page 141 and 142:
8. Проверяем число а
- Page 143 and 144:
Пример 3. Как измени
- Page 145 and 146:
Составляем молекул
- Page 147 and 148:
Задача № 4. Рассчит
- Page 149 and 150:
Электрод с концент
- Page 151 and 152:
ЭДС = Е 0 кат - Е 0 ано
- Page 153 and 154:
HBr H + + Brˉ.Электроли
- Page 155 and 156:
Стандартный электр
- Page 157 and 158:
4Н + + 4NO 3ˉ 4HNO 3 .Сумма
- Page 159 and 160:
U разл.теор = ЭДС = Е
- Page 161 and 162:
VCl2mCumClM2ClЭV2I R96487CuMЭClτ
- Page 164 and 165:
Задача № 3. Кладут в
- Page 166 and 167:
Zn(A)Zn 2+--- - -- ---eO+2HO 2 2 4O
- Page 168 and 169:
Задача № 6. Объясни
- Page 170 and 171:
В нейтральной сред
- Page 172 and 173:
15. ХИМИЧЕСКИЕ СВОЙС
- Page 174 and 175:
Задача № 3. С какими
- Page 176 and 177:
15) Au + HNO 3 + 4HCl H[AuCl 4 ] +
- Page 178 and 179:
%AgAgm100%монеты0,15 1000,305
- Page 180 and 181:
4V + 4KOH + 5O 2 = 4KVO 3 + 2H 2 O;
- Page 182 and 183:
Задача № 4. Вычисли
- Page 184 and 185:
Решение. Запишем хи
- Page 186 and 187:
VNO2222,4 (3663,6X)(25,360,7X)л.П
- Page 188 and 189:
Задача № 3. Хорошо и
- Page 190 and 191:
Задача № 8. Привест
- Page 192 and 193:
По величине конста
- Page 194 and 195:
соответственно сте
- Page 196 and 197:
По этой причине эфф
- Page 198 and 199:
CaO + Al 2 O 3 Ca(AlO 2 ), ΔG o 29
- Page 200 and 201:
19. КОМПЛЕКСНЫЕ СОЕД
- Page 202 and 203:
плексных ионов, в к
- Page 204 and 205:
10) [Cu(NH 3 ) 4 ](OH) 2 + Na 2 S C
- Page 206 and 207:
Задача № 11. Рассчит
- Page 208 and 209:
CoCl 3 ∙2NH 3 ∙2H 2 O (КЧ = 6
- Page 210 and 211:
Задача № 2. Определ
- Page 212 and 213:
2-Чтобы связать ион
- Page 214 and 215:
3Fe 3+ + 3[Fe(CN) 6 ] 4- = Fe 4 [Fe
- Page 216 and 217:
11) NH 2 -NH-CH 2 -CH 2 -CH 2 -NH 2
- Page 218 and 219:
Задача № 3. Какова п
- Page 220 and 221:
3) Индуктивный поло
- Page 222 and 223:
Задача № 10. Состави
- Page 224 and 225:
2C 2 H 5 Cl + 2Na C 4 H 10 + 2NaCl,
- Page 226 and 227:
21.2. Задачи для само
- Page 228 and 229:
22. ЗАДАЧИ ПОВЫШЕННО
- Page 230 and 231:
pH11,0HCl H + +Cl-234pH=lgC HCl2,03
- Page 232 and 233:
рНlgKд,СН3СООН2K(д,СН3
- Page 234 and 235:
Kд,NH4OHПредположим, ч
- Page 236 and 237:
[OH]Kд,NH4OH[NH4OH]1,791050,11,341
- Page 238 and 239:
[H]Кг[NH4][NH OH]4105,59 100,020,
- Page 240 and 241:
22.2. Произведение ра
- Page 242 and 243:
Предположение, что
- Page 244 and 245:
R M,Zn(OH)2моль/л10 -210 -310
- Page 246 and 247:
Е,B3,02,82,62,42,22,01,81,61,41,21
- Page 248 and 249:
E Ox/RedB0Интенсивная к
- Page 250 and 251:
в которой зависимо
- Page 252 and 253:
Пересечение прямых
- Page 254 and 255:
СОДЕРЖАНИЕСтр.Терм
- Page 256:
Учебное изданиеАВД