A. Data Definition Tables
A. Data Definition Tables
A. Data Definition Tables
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
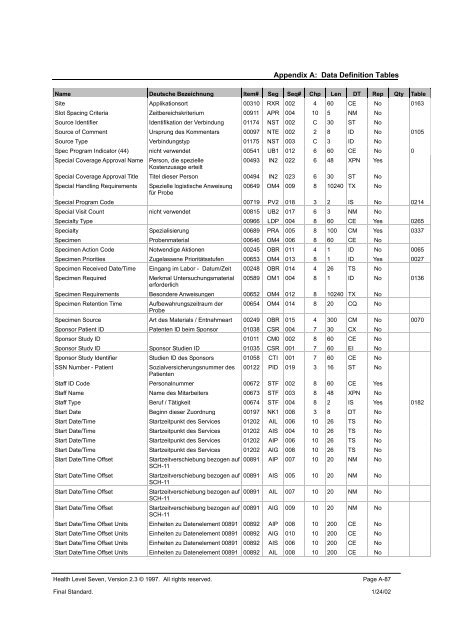
Appendix A: <strong>Data</strong> <strong>Definition</strong> <strong>Tables</strong><br />
Name Deutsche Bezeichnung Item# Seg Seq# Chp Len DT Rep Qty Table<br />
Site Applikationsort 00310 RXR 002 4 60 CE No 0163<br />
Slot Spacing Criteria Zeitbereichskriterium 00911 APR 004 10 5 NM No<br />
Source Identifier Identifikation der Verbindung 01174 NST 002 C 30 ST No<br />
Source of Comment Ursprung des Kommentars 00097 NTE 002 2 8 ID No 0105<br />
Source Type Verbindungstyp 01175 NST 003 C 3 ID No<br />
Spec Program Indicator (44) nicht verwendet 00541 UB1 012 6 60 CE No 0<br />
Special Coverage Approval Name Person, die spezielle<br />
Kostenzusage erteilt<br />
00493 IN2 022 6 48 XPN Yes<br />
Special Coverage Approval Title Titel dieser Person 00494 IN2 023 6 30 ST No<br />
Special Handling Requirements Spezielle logistische Anweisung<br />
für Probe<br />
00649 OM4 009 8 10240 TX No<br />
Special Program Code 00719 PV2 018 3 2 IS No 0214<br />
Special Visit Count nicht verwendet 00815 UB2 017 6 3 NM No<br />
Specialty Type 00966 LDP 004 8 60 CE Yes 0265<br />
Specialty Spezialisierung 00689 PRA 005 8 100 CM Yes 0337<br />
Specimen Probenmaterial 00646 OM4 006 8 60 CE No<br />
Specimen Action Code Notwendige Aktionen 00245 OBR 011 4 1 ID No 0065<br />
Specimen Priorities Zugelassene Prioritätsstufen 00653 OM4 013 8 1 ID Yes 0027<br />
Specimen Received Date/Time Eingang im Labor - Datum/Zeit 00248 OBR 014 4 26 TS No<br />
Specimen Required Merkmal Untersuchungsmaterial<br />
erforderlich<br />
00589 OM1 004 8 1 ID No 0136<br />
Specimen Requirements Besondere Anweisungen 00652 OM4 012 8 10240 TX No<br />
Specimen Retention Time Aufbewahrungszeitraum der<br />
Probe<br />
00654 OM4 014 8 20 CQ No<br />
Specimen Source Art des Materials / Entnahmeart 00249 OBR 015 4 300 CM No 0070<br />
Sponsor Patient ID Patenten ID beim Sponsor 01038 CSR 004 7 30 CX No<br />
Sponsor Study ID 01011 CM0 002 8 60 CE No<br />
Sponsor Study ID Sponsor Studien ID 01035 CSR 001 7 60 EI No<br />
Sponsor Study Identifier Studien ID des Sponsors 01058 CTI 001 7 60 CE No<br />
SSN Number - Patient Sozialversicherungsnummer des<br />
Patienten<br />
00122 PID 019 3 16 ST No<br />
Staff ID Code Personalnummer 00672 STF 002 8 60 CE Yes<br />
Staff Name Name des Mitarbeiters 00673 STF 003 8 48 XPN No<br />
Staff Type Beruf / Tätigkeit 00674 STF 004 8 2 IS Yes 0182<br />
Start Date Beginn dieser Zuordnung 00197 NK1 008 3 8 DT No<br />
Start Date/Time Startzeitpunkt des Services 01202 AIL 006 10 26 TS No<br />
Start Date/Time Startzeitpunkt des Services 01202 AIS 004 10 26 TS No<br />
Start Date/Time Startzeitpunkt des Services 01202 AIP 006 10 26 TS No<br />
Start Date/Time Startzeitpunkt des Services 01202 AIG 008 10 26 TS No<br />
Start Date/Time Offset Startzeitverschiebung bezogen auf 00891<br />
SCH-11<br />
AIP 007 10 20 NM No<br />
Start Date/Time Offset Startzeitverschiebung bezogen auf 00891<br />
SCH-11<br />
AIS 005 10 20 NM No<br />
Start Date/Time Offset Startzeitverschiebung bezogen auf 00891<br />
SCH-11<br />
AIL 007 10 20 NM No<br />
Start Date/Time Offset Startzeitverschiebung bezogen auf 00891<br />
SCH-11<br />
AIG 009 10 20 NM No<br />
Start Date/Time Offset Units Einheiten zu Datenelement 00891 00892 AIP 008 10 200 CE No<br />
Start Date/Time Offset Units Einheiten zu Datenelement 00891 00892 AIG 010 10 200 CE No<br />
Start Date/Time Offset Units Einheiten zu Datenelement 00891 00892 AIS 006 10 200 CE No<br />
Start Date/Time Offset Units Einheiten zu Datenelement 00891 00892 AIL 008 10 200 CE No<br />
Health Level Seven, Version 2.3 © 1997. All rights reserved. Page A-87<br />
Final Standard. 1/24/02