A. Data Definition Tables
A. Data Definition Tables
A. Data Definition Tables
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
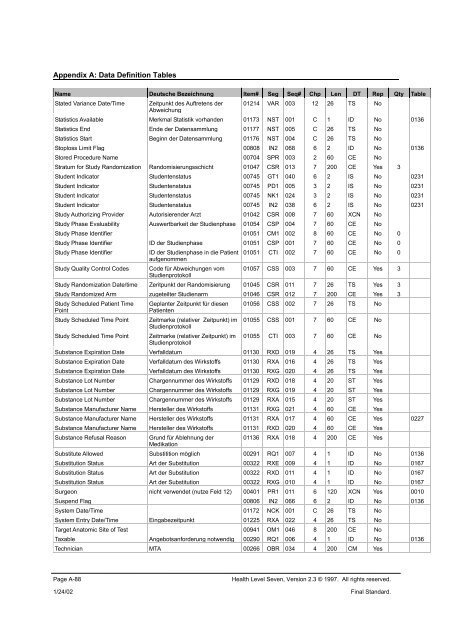
Appendix A: <strong>Data</strong> <strong>Definition</strong> <strong>Tables</strong><br />
Name Deutsche Bezeichnung Item# Seg Seq# Chp Len DT Rep Qty Table<br />
Stated Variance Date/Time Zeitpunkt des Auftretens der<br />
Abweichung<br />
01214 VAR 003 12 26 TS No<br />
Statistics Available Merkmal Statistik vorhanden 01173 NST 001 C 1 ID No 0136<br />
Statistics End Ende der Datensammlung 01177 NST 005 C 26 TS No<br />
Statistics Start Beginn der Datensammlung 01176 NST 004 C 26 TS No<br />
Stoploss Limit Flag 00808 IN2 068 6 2 ID No 0136<br />
Stored Procedure Name 00704 SPR 003 2 60 CE No<br />
Stratum for Study Randomization Randomisierungsschicht 01047 CSR 013 7 200 CE Yes 3<br />
Student Indicator Studentenstatus 00745 GT1 040 6 2 IS No 0231<br />
Student Indicator Studentenstatus 00745 PD1 005 3 2 IS No 0231<br />
Student Indicator Studentenstatus 00745 NK1 024 3 2 IS No 0231<br />
Student Indicator Studentenstatus 00745 IN2 038 6 2 IS No 0231<br />
Study Authorizing Provider Autorisierender Arzt 01042 CSR 008 7 60 XCN No<br />
Study Phase Evaluability Auswertbarkeit der Studienphase 01054 CSP 004 7 60 CE No<br />
Study Phase Identifier 01051 CM1 002 8 60 CE No 0<br />
Study Phase Identifier ID der Studienphase 01051 CSP 001 7 60 CE No 0<br />
Study Phase Identifier ID der Studienphase in die Patient<br />
aufgenommen<br />
01051 CTI 002 7 60 CE No 0<br />
Study Quality Control Codes Code für Abweichungen vom<br />
Studienprotokoll<br />
01057 CSS 003 7 60 CE Yes 3<br />
Study Randomization Date/time Zeritpunkt der Randomisierung 01045 CSR 011 7 26 TS Yes 3<br />
Study Randomized Arm zugeteilter Studienarm 01046 CSR 012 7 200 CE Yes 3<br />
Study Scheduled Patient Time Geplanter Zeitpunkt für diesen 01056 CSS 002 7 26 TS No<br />
Point<br />
Patienten<br />
Study Scheduled Time Point Zeitmarke (relativer Zeitpunkt) im<br />
Studienprotokoll<br />
01055 CSS 001 7 60 CE No<br />
Study Scheduled Time Point Zeitmarke (relativer Zeitpunkt) im<br />
Studienprotokoll<br />
01055 CTI 003 7 60 CE No<br />
Substance Expiration Date Verfalldatum 01130 RXD 019 4 26 TS Yes<br />
Substance Expiration Date Verfalldatum des Wirkstoffs 01130 RXA 016 4 26 TS Yes<br />
Substance Expiration Date Verfalldatum des Wirkstoffs 01130 RXG 020 4 26 TS Yes<br />
Substance Lot Number Chargennummer des Wirkstoffs 01129 RXD 018 4 20 ST Yes<br />
Substance Lot Number Chargennummer des Wirkstoffs 01129 RXG 019 4 20 ST Yes<br />
Substance Lot Number Chargennummer des Wirkstoffs 01129 RXA 015 4 20 ST Yes<br />
Substance Manufacturer Name Hersteller des Wirkstoffs 01131 RXG 021 4 60 CE Yes<br />
Substance Manufacturer Name Hersteller des Wirkstoffs 01131 RXA 017 4 60 CE Yes 0227<br />
Substance Manufacturer Name Hersteller des Wirkstoffs 01131 RXD 020 4 60 CE Yes<br />
Substance Refusal Reason Grund für Ablehnung der<br />
Medikation<br />
01136 RXA 018 4 200 CE Yes<br />
Substitute Allowed Substitition möglich 00291 RQ1 007 4 1 ID No 0136<br />
Substitution Status Art der Substitution 00322 RXE 009 4 1 ID No 0167<br />
Substitution Status Art der Substitution 00322 RXD 011 4 1 ID No 0167<br />
Substitution Status Art der Substitution 00322 RXG 010 4 1 ID No 0167<br />
Surgeon nicht verwendet (nutze Feld 12) 00401 PR1 011 6 120 XCN Yes 0010<br />
Suspend Flag 00806 IN2 066 6 2 ID No 0136<br />
System Date/Time 01172 NCK 001 C 26 TS No<br />
System Entry Date/Time Eingabezeitpunkt 01225 RXA 022 4 26 TS No<br />
Target Anatomic Site of Test 00941 OM1 046 8 200 CE No<br />
Taxable Angebotsanforderung notwendig 00290 RQ1 006 4 1 ID No 0136<br />
Technician MTA 00266 OBR 034 4 200 CM Yes<br />
Page A-88 Health Level Seven, Version 2.3 © 1997. All rights reserved.<br />
1/24/02 Final Standard.