Zusammenfassung AC I - Chemie
Zusammenfassung AC I - Chemie
Zusammenfassung AC I - Chemie
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
1 Chemische Grundlagen<br />
Name der Säure Summenformel Konjugierte Base Summenformel<br />
Flusssäure H 3 O + aq+ F aq – Fluorid F –<br />
Salzsäure H 3 O + aq+ Cl aq – Chlorid Cl –<br />
Bromwasserstoffsäure H 3 O + aq+ Br aq – Bromid Br –<br />
Iodwasserstoffsäure H 3 O + aq+ I aq – Iodid I –<br />
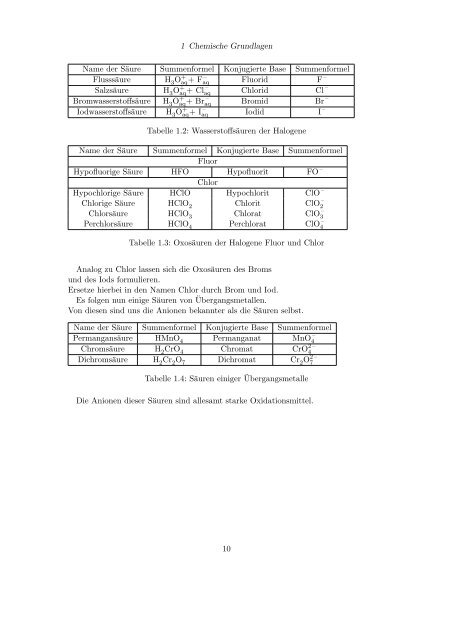
Tabelle 1.2: Wasserstoffsäuren der Halogene<br />
Name der Säure Summenformel Konjugierte Base Summenformel<br />
Fluor<br />
Hypofluorige Säure HFO Hypofluorit FO –<br />
Chlor<br />
Hypochlorige Säure HClO Hypochlorit ClO –<br />
Chlorige Säure HClO 2 Chlorit ClO 2<br />
–<br />
Chlorsäure HClO 3 Chlorat ClO 3<br />
–<br />
Perchlorsäure HClO 4 Perchlorat ClO 4<br />
–<br />
Tabelle 1.3: Oxosäuren der Halogene Fluor und Chlor<br />
Analog zu Chlor lassen sich die Oxosäuren des Broms<br />
und des Iods formulieren.<br />
Ersetze hierbei in den Namen Chlor durch Brom und Iod.<br />
Es folgen nun einige Säuren von Übergangsmetallen.<br />
Von diesen sind uns die Anionen bekannter als die Säuren selbst.<br />
Name der Säure Summenformel Konjugierte Base Summenformel<br />
Permangansäure HMnO 4 Permanganat MnO 4<br />
–<br />
Chromsäure H 2 CrO 4 Chromat CrO 2 4<br />
–<br />
Dichromsäure H 2 Cr 2 O 7 Dichromat Cr 2 O 2 7<br />
–<br />
Tabelle 1.4: Säuren einiger Übergangsmetalle<br />
Die Anionen dieser Säuren sind allesamt starke Oxidationsmittel.<br />
10