4.2.2.9
4.2.2.9
4.2.2.9
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
4. Reaktionen der Cabonylfunktion in Aldehyden, Ketonen, www.ioc-praktikum.de<br />
Carbonsäuren und Carbonsäurederivaten<br />
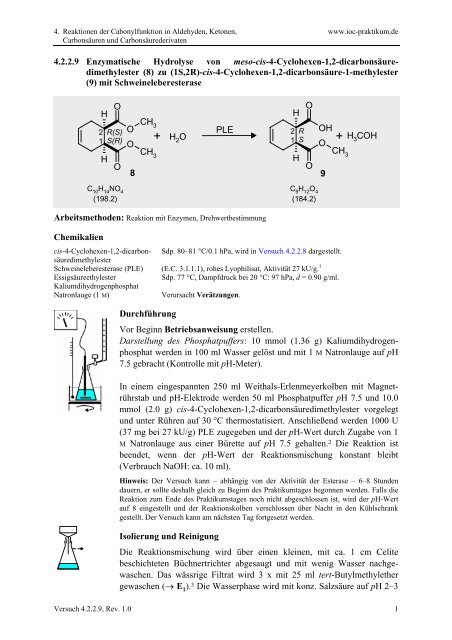
<strong>4.2.2.9</strong> Enzymatische Hydrolyse von meso-cis-4-Cyclohexen-1,2-dicarbonsäuredimethylester<br />
(8) zu (1S,2R)-cis-4-Cyclohexen-1,2-dicarbonsäure-1-methylester<br />
(9) mit Schweineleberesterase<br />
H<br />
O<br />
2 R(S)<br />
1 S(R)<br />
O CH 3<br />
O<br />
CH3<br />
+<br />
H 2<br />
O<br />
PLE<br />
H<br />
2<br />
1<br />
R<br />
S<br />
O<br />
OH<br />
+<br />
O<br />
CH3<br />
H 3<br />
COH<br />
H<br />
O<br />
8<br />
H<br />
O<br />
9<br />
C 10<br />
H 14<br />
NO 4<br />
(198.2)<br />
C 9<br />
H 12<br />
O 4<br />
(184.2)<br />
Arbeitsmethoden: Reaktion mit Enzymen, Drehwertbestimmung<br />
Chemikalien<br />
cis-4-Cyclohexen-1,2-dicarbon- Sdp. 80–81 °C/0.1 hPa, wird in Versuch 4.2.2.8 dargestellt.<br />
säuredimethylester<br />
Schweineleberesterase (PLE) (E.C. 3.1.1.1), rohes Lyophilisat, Aktivität 27 kU/g. 1<br />
Essigsäureethylester<br />
Sdp. 77 °C, Dampfdruck bei 20 °C: 97 hPa, d = 0.90 g/ml.<br />
Kaliumdihydrogenphosphat<br />
Natronlauge (1 M)<br />
Verursacht Verätzungen.<br />
Durchführung<br />
Vor Beginn Betriebsanweisung erstellen.<br />
Darstellung des Phosphatpuffers: 10 mmol (1.36 g) Kaliumdihydrogenphosphat<br />
werden in 100 ml Wasser gelöst und mit 1 M Natronlauge auf pH<br />
7.5 gebracht (Kontrolle mit pH-Meter).<br />
In einem eingespannten 250 ml Weithals-Erlenmeyerkolben mit Magnetrührstab<br />
und pH-Elektrode werden 50 ml Phosphatpuffer pH 7.5 und 10.0<br />
mmol (2.0 g) cis-4-Cyclohexen-1,2-dicarbonsäuredimethylester vorgelegt<br />
und unter Rühren auf 30 °C thermostatisiert. Anschließend werden 1000 U<br />
(37 mg bei 27 kU/g) PLE zugegeben und der pH-Wert durch Zugabe von 1<br />
M Natronlauge aus einer Bürette auf pH 7.5 gehalten. 2 Die Reaktion ist<br />
beendet, wenn der pH-Wert der Reaktionsmischung konstant bleibt<br />
(Verbrauch NaOH: ca. 10 ml).<br />
Hinweis: Der Versuch kann – abhängig von der Aktivität der Esterase – 6–8 Stunden<br />
dauern, er sollte deshalb gleich zu Beginn des Praktikumtages begonnen werden. Falls die<br />
Reaktion zum Ende des Praktikumstages noch nicht abgeschlossen ist, wird der pH-Wert<br />
auf 8 eingestellt und der Reaktionskolben verschlossen über Nacht in den Kühlschrank<br />
gestellt. Der Versuch kann am nächsten Tag fortgesetzt werden.<br />
Isolierung und Reinigung<br />
Die Reaktionsmischung wird über einen kleinen, mit ca. 1 cm Celite<br />
beschichteten Büchnertrichter abgesaugt und mit wenig Wasser nachgewaschen.<br />
Das wässrige Filtrat wird 3 x mit 25 ml tert-Butylmethylether<br />
gewaschen (→ E 1 ). 3 Die Wasserphase wird mit konz. Salzsäure auf pH 2–3<br />
Versuch <strong>4.2.2.9</strong>, Rev. 1.0 1
4. Reaktionen der Cabonylfunktion in Aldehyden, Ketonen, www.ioc-praktikum.de<br />
Carbonsäuren und Carbonsäurederivaten<br />
gebracht und dreimal mit je 50 ml tert-Butylmethylether extrahiert (→ E 2 ).<br />
Die vereinigten organischen Phasen werden über Natriumsulfat getrocknet.<br />
Nach dem Absaugen vom Trockenmittel (→ E 3 ) wird das Lösungsmittel am<br />
Rotationsverdampfer abdestilliert (→ R 1 ), Lösungsmittelreste bei vermindertem<br />
Druck entfernt; das ölige Produkt kristallisiert langsam im Eisbad.<br />
Eine weitere Reinigung ist nicht nötig. Ausbeute Reinprodukt (g, %)? Man<br />
bestimme den spezifischen Drehwert von 9 und berechne den Enantiomerenüberschuss<br />
(ee). Ausbeute an 9: 75–85%, Schmp. 28 °C, [ a]<br />
D<br />
20<br />
=<br />
+11.0° (c = 1.0, Aceton).<br />
1 Die übliche Mengeneinheit bei Einsatz von Enzymen ist 1 U (Unit). Die Aktivität eines<br />
Substrats wird in U/g (Units per g) angegeben, was bei verschiedenen Enzymqualitäten<br />
eine Umrechnung ermöglicht und somit der Reproduzierbarkeit dient. Die hier<br />
verwendete Schweineleberesterase ist bei SIGMA erhältlich (Best.-Nr. E3019).<br />
2 Protokollieren Sie den Verbrauch in Abhängigkeit von der Zeit, graphische Darstellung!<br />
3 Was bewirkt dieser Reinigungsschritt?<br />
Hinweise zur Entsorgung (E), Recycling (R) der Lösungsmittel<br />
E 1 : Organischer Extrakt → Entsorgung (RH).<br />
E 2 : Wässrige Phasen → Entsorgung (H 2 O mit RHal/Halogenid).<br />
E 3 : Trockenmittel → Entsorgung (Anorg. Feststoffe).<br />
R 1 : abdestilliertes Lösungsmittel → Recycling (tert-Butylmethylether).<br />
Auswertung des Versuchs<br />
1 H-NMR-Spektrum von 9 (300 MHz, DMSO-d 6 ): δ = 2.20–2.47 (4 H), 2.90–3.00 (2 H), 3.57 (3 H), 5.55–5.67<br />
(2 H), 12.28 (1 H).<br />
3.0 2.8 2.6<br />
2.4 2.2<br />
13.0 12.0 11.0 10.0 9.0 8.0 7.0 6.0 5.0 4.0 3.0 2.0 [ppm] 0.0<br />
13 C-NMR-Spektrum von 9 (300 MHz, DMSO-d 6 ): 25.21 (CH 2 ), 25.57 (CH 2 ), 38.54 (CH), 38.66 (CH), 51.26<br />
(CH 3 ), 124.89 (CH), 125.20 (CH), 173.23 (C), 174.23 (C).<br />
LM<br />
40<br />
38<br />
180<br />
160<br />
140 120<br />
100<br />
80<br />
60 40 20 [ppm] 0<br />
Versuch <strong>4.2.2.9</strong>, Rev. 1.0 2
4. Reaktionen der Cabonylfunktion in Aldehyden, Ketonen, www.ioc-praktikum.de<br />
Carbonsäuren und Carbonsäurederivaten<br />
IR-Spektrum von 9 (KBr):<br />
100<br />
T [%]<br />
50<br />
3030 2960<br />
1735 1710<br />
0<br />
~<br />
4000 3000 2000 1500 1000 ν [cm -1 ]<br />
* Formulieren Sie den zu 9 führenden Reaktionsmechanismus.<br />
Weitere denkbare Reaktionsprodukte:<br />
O<br />
O<br />
O<br />
OH<br />
OH<br />
OH<br />
OH<br />
O<br />
O<br />
O<br />
A B C<br />
* Mit welchen spektroskopischen Daten lassen sich A–C ausschließen?<br />
* Diskutieren Sie die denkbaren Reaktionsmechanismen.<br />
Literatur, allgemeine Anwendbarkeit der Methode<br />
Literatur, auf der dieser Versuch beruht: [1]. Schweineleberesterase (Pig Liver Eserase, PLE) kann zur stereoselektiven<br />
Hydrolyse einer Vielzahl von Estern eingesetzt werden. [2–4]<br />
Esterasen sind Enzyme (biologische Katalysatoren), die aus pflanzlichen und tierischen Organismen bzw.<br />
Organen (z.B. Schweineleber) isoliert werden können. Sie katalysieren die Hydrolyse von Carbonsäureestern,<br />
mit chiralen Estern reagieren sie enantioselektiv:<br />
O<br />
O OR O OR<br />
O OH<br />
O<br />
C<br />
C<br />
C<br />
C<br />
R S<br />
Schweineleberesterase<br />
H C Me Me C<br />
R<br />
S<br />
H C Me Me C H<br />
+<br />
H C Me H C Me<br />
H C Me H C<br />
S<br />
S H 2<br />
O<br />
S S<br />
C<br />
C<br />
C<br />
C<br />
O OR O OR<br />
O OR<br />
O<br />
meso-<br />
rac-<br />
OR<br />
H<br />
Me<br />
OR<br />
[1] H.-J. Gais, K.L. Lukas, W.A. Ball, S. Braun, H.J. Lindner, Liebigs Ann. Chem. 1986, 687–716.<br />
[2] L.M. Zhu, M.C. Tedford, Tetrahedron, 1990, 46, 6587–6611.<br />
[3] M. Ohno, M. Otsuka, Org. React. 1989, 37, 1–55.<br />
[4] C.-H. Wong, G.M. Whitesides, “Enzymes in Synthetic Organic Chemistry” Pergamon Verlag, 1994.<br />
Versuch <strong>4.2.2.9</strong>, Rev. 1.0 3