Chemische Reaktionen
Chemische Reaktionen
Chemische Reaktionen
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
<strong>Chemische</strong> <strong>Reaktionen</strong>•Heterogene und homogene Gleichgewichte
Lösungsmittel und Löslichkeit• Lösungsmittelpolaritätpolar, unpolarhydrophil, hydrophoblipophob, lipophil• Mischbarkeit von Lösungsmitteln• Gesättigte Lösungen
Löslichkeit von GasenLöslichkeit von Gasen im Blut!
ZweiphasensystemeNichtmischbare LösungsmittelExtraktion
Adsorption an OberflächenLangmuir´sche Adsorptionsisotherme
Membrangleichgewichte•OsmoseDiffusion von (Lösungsmittel-)Molekülen durch einesemipermeable Membran
Hyper- und hypotonische Lösungen
Donnan-Gleichgewicht
Trennverfahren• Destillation• Sublimation• Gefriertrocknung• Kristallisation• Extraktion• Dialyse• ChromatographieSäulen- und DünnschichtchromatographieFlüssig- und Gaschromatographie(HPLC, GC)
• <strong>Chemische</strong> <strong>Reaktionen</strong>Beispiele:•Säure-Base-<strong>Reaktionen</strong>•Fällungs-<strong>Reaktionen</strong>•Redox-<strong>Reaktionen</strong>•Metallkomplex-<strong>Reaktionen</strong>•„Kovalente <strong>Reaktionen</strong>“
Stöchiometrische Berechnungen
Konzentrationsangaben• Molarität MEine einmolare Lösung einer Substanz X enthält1 mol dieser Substanz in 1 L der fertigen Lösung1 M Salzsäure = 1 mol HCl/ L = 36,5 g HCl/ L1mM Salzsäure = 1 mmol HCl/ L = 36, 5 mg HCl/ L1µM Salzsäure = 1 µmol HCL/L = 36,5 µg/ HCl/ LMassenkonzentrationen: g/ L, mg/ L, µg/ L……Massenanteil: „Gewichtsprozente“ (w/ w), g in 100 g…..Volumsanteil: „Volumsprozente“ (v/ v), mL in 100 ml….
<strong>Chemische</strong>s Gleichgewicht• MassenwirkungsgesetzReversible und homogene <strong>Reaktionen</strong>•Prinzip des kleinsten ZwangesSystem weicht dem Druck von außen aus
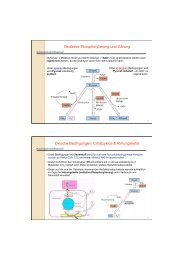
Energetik chemischer <strong>Reaktionen</strong>Energie:Wärme, elektrisch, Licht-, mechanisch
Thermodynamik1. Hauptsatz2. Hauptsatz
Freie Energieund chemisches Gleichgewicht∆G 0 = -RTlnK
• Fließgleichgewicht• Geschlossene Systeme:kein Stoffaustausch mit der UmgebungMassenwirkungsgesetz – stabiles Gleichgewicht• Offene Systeme – Biologie:Stoff- und Energieaustausch mit der UmgebungReaktionsfolgen – Fließgleichgewichtbenötigt Energie, kann Arbeit leisten, ist regulierbar