Die biochemische Bedeutung von ZINK - Userpage
Die biochemische Bedeutung von ZINK - Userpage
Die biochemische Bedeutung von ZINK - Userpage
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
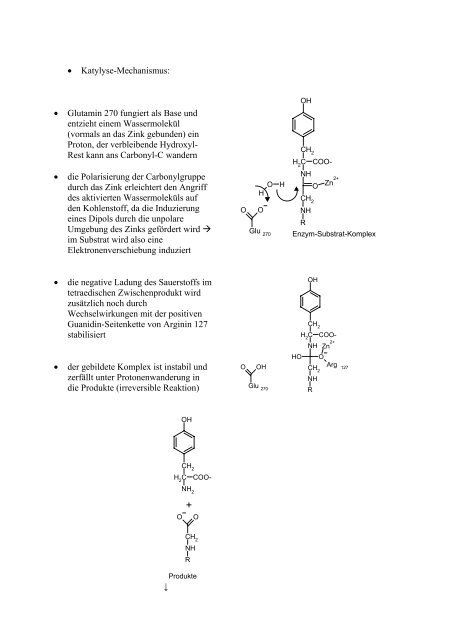
• Katylyse-Mechanismus:<br />
• Glutamin 270 fungiert als Base und<br />
entzieht einem Wassermolekül<br />
(vormals an das Zink gebunden) ein<br />
Proton, der verbleibende Hydroxyl-<br />
Rest kann ans Carbonyl-C wandern<br />
• die Polarisierung der Carbonylgruppe<br />
durch das Zink erleichtert den Angriff<br />
des aktivierten Wassermoleküls auf<br />
den Kohlenstoff, da die Induzierung<br />
eines Dipols durch die unpolare<br />
Umgebung des Zinks gefördert wird �<br />
im Substrat wird also eine<br />
Elektronenverschiebung induziert<br />
• die negative Ladung des Sauerstoffs im<br />
tetraedischen Zwischenprodukt wird<br />
zusätzlich noch durch<br />
Wechselwirkungen mit der positiven<br />
Guanidin-Seitenkette <strong>von</strong> Arginin 127<br />
stabilisiert<br />
• der gebildete Komplex ist instabil und<br />
zerfällt unter Protonenwanderung in<br />
die Produkte (irreversible Reaktion)<br />
↓<br />
OH<br />
CH 2<br />
H 2 C COO-<br />
NH 2<br />
+<br />
O O<br />
CH 2<br />
NH<br />
R<br />
Produkte<br />
O<br />
O<br />
O H<br />
H<br />
O<br />
Glu 270<br />
OH<br />
Glu 270<br />
OH<br />
CH2 H C COO-<br />
2<br />
NH<br />
O<br />
CH 2<br />
Zn 2+<br />
NH<br />
R<br />
Enzym-Substrat-Komplex<br />
OH<br />
CH2 H2C COO-<br />
NH Zn<br />
HO<br />
O<br />
2+<br />
CH 2<br />
NH<br />
R<br />
Arg 127










![[UNBEGRENZTE MÖGLICHKEITEN?] - Userpage](https://img.yumpu.com/22343335/1/184x260/unbegrenzte-moglichkeiten-userpage.jpg?quality=85)





