diagnostik + therapie - Frauenarzt
diagnostik + therapie - Frauenarzt
diagnostik + therapie - Frauenarzt
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
DIAGNOSTIK + THERAPIE<br />
50<br />
MAMMOGRAPHIE<br />
Digitales System eignet sich zum<br />
Erkennen von Mikrokalk<br />
An einem anthropomorphen Phantom wurde die Detektierbarkeit Mikrokalk-ähnlicher<br />
Partikel bei konventioneller und digitaler Mammographie verglichen<br />
Matthias Küchler<br />
Das Ortsauflösungsvermögen eines<br />
Mammographie-Gerätes hängt einerseits<br />
von den geometrischen Verhältnissen,<br />
d.h. von der Größe des<br />
Brennfleckes, vom Fokus-Detektor-<br />
Abstand und vom Objekt-Detektor-<br />
Abstand, und andererseits vom Auflösungsvermögen<br />
des Detektors ab.<br />
Ausgehend davon, dass übliche Film-<br />
Folien-Systeme richtungsunabhängig<br />
mehr als 20 Linienpaare je Millimeter<br />
(Lp/mm) auflösen, wird mit den<br />
verbreiteten Auflösungstests mittels<br />
Bleistrich-Raster oder Edelstahl-<br />
Drahtgewebe im Wesentlichen das<br />
geometrische Auflösungsvermögen<br />
und bei sonst weitgehend identischen<br />
Verhältnissen insbesondere die<br />
effektive Brennfleck-Ausdehnung bestimmt.<br />
Ein direkter Rückschluss auf<br />
die minimale Größe, bis zu der Niedrigkontrast-Objekte<br />
mit einem zur<br />
Detektion ausreichenden Signal-<br />
Rausch-Verhältnis abgebildet werden,<br />
ist dabei nicht möglich.<br />
Beim Einsatz digitaler Detektoren im<br />
Zusammenspiel mit geometrisch optimierten<br />
Mammographie-Geräten<br />
begrenzt derzeit die Pixelstruktur der<br />
Detektoren das Ortsauflösungsvermögen,<br />
während das Auflösungsver-<br />
FRAUENARZT ■ 43 (2002) ■ Nr. 1<br />
mögen der eingesetzten Laser-Imager,<br />
mit denen die digital gewonnenen<br />
Aufnahmen auf Film ausgegeben<br />
werden, mit etwa 36 Lp/mm als ausreichend<br />
hoch angesehen werden<br />
kann. Die Ausgabe über den Laser-<br />
Imager spiegelt sich somit nur in<br />
einer äußerst feinen Linienstruktur<br />
auf dem Film wider, die auch bei<br />
Betrachtung mit üblicher Lupenvergrößerung<br />
kaum erkennbar ist, sodass<br />
ein negativer Einfluss auf die<br />
folgenden Auswertungen wie auch<br />
auf die Diagnostik insgesamt ausgeschlossen<br />
werden kann.<br />
Das Ortsauflösungsvermögen digitaler<br />
Detektoren ist deutlich richtungsabhängig<br />
und führt beim Einsatz<br />
von Auflösungstests, die parallel<br />
zu den Pixelreihen oder -spalten<br />
orientierte lineare Strukturen aufweisen,<br />
zu Überlagerungen, welche<br />
eine Beurteilung des Auflösungsvermögens<br />
erschweren bzw. unmöglich<br />
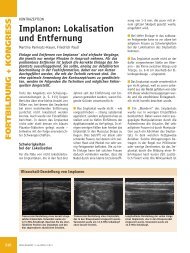
machen. So ist bereits bei einem Auflösungstest<br />
mit 4,5 Lp/mm (s. Abb.<br />
1 oben, linke Gruppe) keine klare und<br />
gleichmäßige Auflösung der sechs<br />
schwarzen Linien dieser Gruppe mehr<br />
erkennbar, während bei 5,0 und 5,5<br />
Lp/mm die sechs bzw. sieben schwar-<br />
Abb. 1: Auflösungstest mit 4,5 / 5,0 / 5,5 Lp/mm parallel (oben) und mit 5,0/5,5/6,0 Lp/mm<br />
schräg (unten) zur Pixelstruktur des Detektors, Ausschnitt jeweils ca. 1 x 10 mm.<br />
zen Linien der jeweiligen Gruppe je<br />
nach konkreter Orientierung zu den<br />
Zusammenfassung<br />
Digitale Detektoren für die Mammographie<br />
zeigen gegenwärtig<br />
noch ein deutlich geringeres Ortsauflösungsvermögen<br />
als konventionelle<br />
Film-Folien-Systeme. Mit dieser<br />
Arbeit soll nachgewiesen werden,<br />
dass hinsichtlich der praktisch<br />
relevanten Detektierbarkeit von<br />
Mikrokalk ein derzeit angebotenes<br />
digitales System (Senographe DMR<br />
2000, Fa. General Electric Medical<br />
Systems mit einem Dry View 8600<br />
Medical Laser Imager der Fa. Kodak)<br />
bereits als mindestens gleichwertig<br />
zu einem konventionellen<br />
System (Alpha RT der Fa. Instrumentarium<br />
Imaging mit dem MinR<br />
2000-Film-Folien-System der Fa.<br />
Kodak) angesehen werden kann.<br />
Dazu wurden Mikrokalk-ähnliche<br />
Partikel (7-µm-Gold-Absorber, Fa.<br />
pehamed) in einer Mamma-äquivalenten<br />
Struktur (Anthropomorphic<br />
Breast Phantom, Fa. Gammex-RMI)<br />
abgebildet. Die Erkennbarkeit dieser<br />
Objekte wurde von zehn mammographisch<br />
tätigen Ärzten getestet.<br />
Acht dieser zehn Ärzte detektierten<br />
auf den digital angefertigten<br />
Aufnahmen mehr Partikel-<br />
Gruppen als auf den konventionell<br />
angefertigten Aufnahmen. Somit<br />
bestehen bei Erfüllung aller sonstigen<br />
Anforderungen keine Hinderungsgründe,<br />
den Einsatz dieses digitalen<br />
System trotz des gemäß<br />
den deutschen Regelungen nominell<br />
unzureichenden Ortsauflösungsvermögens<br />
zu genehmigen.
Abb. 2: Auflösungstest mit regelmäßig<br />
angeordneten 100-µm-Öffnungen (oben)<br />
und einzelner Gold-Absorber mit 80 µm<br />
Durchmesser (unten), Ausschnitt jeweils<br />
ca. 3 x 4 mm<br />
Pixelreihen teils komplett dargestellt<br />
und teils vollkommen ausgelöscht<br />
sind (s. Abb. 1 oben, mittlere und<br />
rechte Gruppe). Ähnliche Beobachtungen<br />
sind bei konventionellen<br />
Mammographie-Geräten als „inverse<br />
Abbildung“ bekannt (1).<br />
Unter diesen Umständen kann dem<br />
digitalen Detektor des Senographe<br />
DMR 2000 nur ein generelles und damit<br />
richtungsunabhängiges Ortsauflösungsvermögen<br />
von etwa 4 Lp/mm<br />
zugeordnet werden, auch wenn bei<br />
günstigerer Orientierung der linearen<br />
Strukturen des Auflösungstests<br />
schräg zu den Pixelreihen und -spalten<br />
weitere Gruppen bis zu 5,5<br />
Lp/mm (s. Abb. 1 unten, mittlere<br />
Gruppe) aufgelöst werden können.<br />
Während die regelmäßig angeordneten<br />
strahlendurchlässigen Öffnungen<br />
des Niedrigkontrast-Auflösungstests<br />
(7 µm Gold als Absorber) aufgrund<br />
von Überlagerungen mit der geometrischen<br />
Struktur des Detektors<br />
bestenfalls bis zu einer Größe von<br />
100 µm (entsprechend der Gruppe<br />
mit 5,0 Lp/mm) als getrennte Objekte<br />
auf den Prüfkörper-Aufnahmen er-<br />
kennbar sind (s. Abb. 2 oben), wird<br />
durch das digitale System jedes einzelne<br />
Partikel mit 80 µm Durchmesser<br />
unabhängig von seiner jeweiligen<br />
Orientierung zum Pixelraster des<br />
Detektors auch vor inhomogenem<br />
Hintergrund noch abgebildet (s. Abb.<br />
2 unten, Partikel im Zentrum), wobei<br />
das sinkende Signal-Rausch-Verhältnis<br />
kleinerer Objekte eine Abgrenzung<br />
gegenüber ähnlichen Artefakten<br />
zunehmend schwieriger gestaltet.<br />
Offensichtlich ist es für die<br />
Wiedergabe kleinster Partikel aber<br />
ausreichend, wenn mehrere benachbarte<br />
Pixel nur teilweise abgeschattet<br />
werden, sodass die Größe der einzelnen<br />
Pixel keine absolute Grenze<br />
für die Abbildung dieser Objekte darstellt.<br />
Material und Methodik<br />
■ Struktur der Testobjekte<br />
zur Erkennbarkeit von Mikrokalk<br />
Als Mikrokalk-ähnliche Niedrigkontrast-Objekte<br />
dienten 7-µm-Gold-<br />
Absorber mit Durchmessern von 250,<br />
200, 160, 120 und 80 µm, von denen<br />
jeweils sechs Partikel gleicher<br />
Größe in einer Gruppe mit gegenseitigen<br />
Abständen von 5 mm (analog<br />
zur Augenanordnung auf einem Würfel)<br />
auf einer strahlendurchlässigen<br />
Folie zusammengefasst waren. Diese<br />
Anordnung sollte vor dem Hintergrund<br />
des anthropomorphen Phantoms,<br />
welches z. T. ebenfalls Mikrokalk-ähnliche,<br />
aber unregelmäßig<br />
angeordnete Strukturen enthielt,<br />
eine relativ sichere Entscheidung ermöglichen,<br />
ob eine mehr oder weniger<br />
vollständig erkennbare Gruppe<br />
oder nur eine Reihe hier störender<br />
Artefakte im geprüften Areal vorhanden<br />
war (s. Abb. 3).<br />
Als Modell für die geforderte eindeutige<br />
Entscheidung diente dabei ein<br />
Stufenprozess. Zuerst müssen überhaupt<br />
zwei oder drei der sich nur<br />
noch wenig vom Hintergrundrauschen<br />
abhebenden Partikel als reale<br />
Objekte erkannt werden – genau das<br />
gleiche Problem, vor dem der mammographisch<br />
tätige Arzt bei der Su-<br />
che nach kleinsten Mikroverkalkungen<br />
steht.<br />
Danach können aufgrund der bekannten<br />
geometrischen Anordnung –<br />
ausgehend von diesen zuerst detektierten<br />
Partikeln – auch weitere minimale<br />
optische Dichteschwankungen<br />
mit noch niedrigerem Signal-Rausch-<br />
Verhältnis mit gewisser Wahrscheinlichkeit<br />
als Abbild der fehlenden Partikel<br />
interpretiert werden. Da auch die<br />
kleinsten Partikel noch erkennbare<br />
Störungen im Hintergrundrauschen<br />
hinterließen (s. Abb. 2 unten) und<br />
letztlich das Vorhandensein einer<br />
Gruppe von Artefakten mit genau bekannter<br />
geometrischer Beziehung mit<br />
deutlich größerer Sicherheit als das<br />
Vorhandensein eines Einzelpartikels<br />
festgestellt werden kann, diente dieser<br />
zweite Schritt im Wesentlichen<br />
nur noch der Vermeidung falschpositiver<br />
Detektionen, während ein direkter<br />
Bezug zur Befundung einer realen<br />
Mammographie nicht mehr gegeben<br />
ist.<br />
Mit dieser Maßnahme gelang es, dass<br />
bei insgesamt 1.540 überprüften Arealen<br />
nur in einem einzigen Fall die<br />
Anwesenheit einer Partikelgruppe in<br />
einem definitiv leeren Areal angegeben<br />
wurde. Diese eine Fehleinschätzung<br />
hat keinerlei Einfluss auf das<br />
Gesamtergebnis; sie blieb aus diesem<br />
Grund in Tabelle 1 (s. S. 52) und bei<br />
allen folgenden Betrachtungen unberücksichtigt.<br />
Die einzelnen Folienstücke mit den<br />
Partikelgruppen (sowie vier Folienstücke<br />
ohne Partikel) waren zwischen<br />
Abb. 3: Anordnung der sechs Gold-Absorber<br />
in jeder Gruppe vor Mamma-äquivalentem<br />
Hintergrund, Ausschnitt ca. 10 x 15 mm<br />
DIAGNOSTIK + THERAPIE<br />
FRAUENARZT ■ 43 (2002) ■ Nr. 1 51
DIAGNOSTIK + THERAPIE<br />
52<br />
jeweils zwei kreisförmigen Stücken<br />
unverarbeiteten Mammographie-Films<br />
eingebettet, und aus den somit vorliegenden<br />
19 Scheiben wurden für<br />
jede Aufnahme jeweils elf, darunter<br />
immer ein bis vier ohne Partikel, zufällig<br />
ausgewählt. Die Scheiben wurden<br />
direkt auf dem Mamma-Auflagetisch<br />
nach immer gleichem Grundschema<br />
(s. Abb. 4 links) angeordnet,<br />
wobei die Orientierung der Partikelgruppen<br />
aus einer von vier vorgegebenen<br />
Richtungen (0°, 90° und<br />
+/- 45°) zufällig gewählt wurde.<br />
Die gesamte Anordnung wurde mit<br />
dem anthropomorphen Phantom abgedeckt.<br />
Dieses Phantom repräsentiert<br />
eine je zur Hälfte aus Fett-<br />
und Bindegewebe bestehende und<br />
auf eine Dicke von 5 cm komprimierte<br />
Brust, wobei die verschiedenen<br />
Schwärzungen im Röntgenbild<br />
(s. Abb. 4 rechts) nicht durch<br />
Dichte-, sondern durch Dickenunterschiede<br />
des Phantommaterials realisiert<br />
werden.<br />
Die Exposition erfolgte in allen Fällen<br />
mit 28 kV sowie Molybdän-Anode<br />
und -Filter. Um absolut gleichmäßig<br />
exponierte Aufnahmen auch bei ge-<br />
FRAUENARZT ■ 43 (2002) ■ Nr. 1<br />
ringfügiger Verschiebung des Phantoms<br />
gegenüber der Messkammer zu<br />
erhalten, wurden die mAs-Werte, die<br />
vorab an beiden Geräten mit der im<br />
Routinebetrieb eingesetzten Einstellung<br />
der Belichtungsautomatik ermittelt<br />
worden waren, jeweils durch<br />
die nächstgelegenen Werte für die<br />
freie Einstellung ersetzt. Damit wurden<br />
einerseits sieben Aufnahmen am<br />
konventionellen Mammographie-Gerät<br />
mit je 63 mAs und andererseits sieben<br />
Aufnahmen am digitalen Gerät mit je<br />
71 mAs exponiert. Die daraus resultierenden<br />
geringen Unterschiede der<br />
Oberflächendosis von 5,3 bzw. 5,9<br />
mGy können sowohl bezüglich ihres<br />
Einflusses auf die hier untersuchten<br />
Detektionsmöglichkeiten (2) als auch<br />
bezüglich der Anforderungen der<br />
Bundesärztekammer (3) beim klinischen<br />
Einsatz digitaler Bilddetektoren<br />
vernachlässigt werden.<br />
Vorversuche mit den digital erstellten<br />
Aufnahmen zeigten, dass bei einer<br />
Optimierung der Monitorwiedergabe<br />
auf die optischen Verhältnisse im jeweils<br />
bezüglich der Anwesenheit einer<br />
Partikelgruppe zu bewertenden<br />
Areal immer eine zweifelsfreie Detektion<br />
aller dort vorhandenen Partikel<br />
Wie viele Gruppen Mikrokalk-ähnlicher Partikel wurden erkannt?<br />
möglich war. Da einerseits die damit<br />
verbundene zeitaufwendige Einzelbewertung<br />
der verschiedenen Dichtebereiche<br />
in der Regel nicht bei jeder Befundung<br />
einer realen Mammographie<br />
vorausgesetzt werden kann und andererseits<br />
ein Verzicht auf diese Optimierungsmöglichkeit<br />
sicher keinen<br />
Einfluss zugunsten der Bewertung der<br />
digitalen Technik hat, wurden auch<br />
die digital erstellten Aufnahmen über<br />
den Laser-Imager ausgegeben. Dabei<br />
wurde analog zu den Anforderungen<br />
für konventionelle Aufnahmen der<br />
Objektumfang durch eine Anpassung<br />
von optischer Dichte und Kontrast auf<br />
dem visuell nutzbaren Schwärzungsbereich<br />
des Laser-Filmes abgebildet,<br />
während auf jede Art weiterer Nachbearbeitung<br />
verzichtet wurde. Alle<br />
Aufnahmen zeigen vor einer Mammaäquivalenten<br />
Gewebestruktur zur<br />
Orientierung eine regelmäßige Anordnung<br />
von elf Kreisen mit 29 mm<br />
Durchmesser (s. Abb. 4 rechts), von<br />
denen sieben bis zehn die beschriebenen<br />
Partikelgruppen enthalten.<br />
Es wurden sieben Paare aus je einer<br />
konventionellen und einer digitalen<br />
Aufnahme mit jeweils gleicher Anzahl<br />
von Gruppen mit identischer Parti-<br />
Digitales System Konventionelles System<br />
Partikeldurchmesser 120 µm 80 µm 120 µm 80 µm<br />
Anzahl vorhandener Gruppen 13 6 13 6<br />
Testpersonen<br />
A 13 3 13 2<br />
B 13 3 13 2<br />
C 13 3 13 1<br />
D 13 1 12 2<br />
E 13 0 13 0<br />
F 13 0 11 0<br />
G 13 0 11 0<br />
H 13 0 10 0<br />
I 12 0 11 0<br />
J 12 0 10 0<br />
Summe insgesamt detektierter Gruppen 128 10 117 7<br />
Anteil insgesamt detektierter Gruppen 98 % 17 % 90 % 12 %<br />
Tab. 1: Anzahl der von den einzelnen Testpersonen detektierten Gruppen Mikrokalk-ähnlicher Partikel
Abb. 4: Schematische Anordnung (links) und Abbildung (rechts) der Scheiben mit den Gruppen Mikrokalk-ähnlicher Partikel hinter dem Mamma-äquivalenten<br />
Phantom<br />
kelgröße gebildet. Diese Paare wurden<br />
zehn mammographisch tätigen<br />
Ärzten in jeweils gleicher Reihenfolge<br />
mit dem Minimum exponierter Partikelgruppen<br />
beim dritten Aufnahmepaar<br />
zur Auswertung vorgelegt. Aufgrund<br />
der insbesondere bei der<br />
Wiedergabe des Mikrokalks erkennbaren<br />
Zeilenstruktur des Laser-Imagers<br />
war dabei jederzeit eine Zuordnung<br />
zum digitalen bzw. konventionellen<br />
System möglich. Unbekannt blieb bei<br />
jeder Aufnahme die genaue Anzahl<br />
der Areale ohne Partikelgruppe.<br />
Ergebnisse<br />
Alle Gruppen mit 250-µm-, 200-µm<br />
und 160-µm-Partikeln wurden durchgehend<br />
von allen Ärzten erkannt. Hier<br />
zeigte sich, dass die aktuelle Anforderung<br />
der Bundesärztekammer (2),<br />
wonach zu den wichtigen Bildmerkmalen<br />
die Wiedergabe von Mikroverkalkungen<br />
einer Größe von ≤ 0,2 mm<br />
gehört, von den gegenwärtig betriebenen<br />
Mammographie-Einrichtungen<br />
zweifelsfrei erfüllt wird.<br />
Von den insgesamt je 130 Arealen mit<br />
120-µm-Partikeln wurden mit dem digitalen<br />
System 128 und mit dem konventionellen<br />
System 117 detektiert,<br />
und von den je 60 Arealen mit 80-µm-<br />
Partikeln wurden noch zehn mit dem<br />
digitalen und sieben mit dem konventionellen<br />
System aufgefunden (s. Tab.<br />
1), wobei die relativ geringe Anzahl<br />
von Einzelentscheidungen weder eine<br />
Abhängigkeit der Detektionsrate von<br />
der Position noch von der Orientierung<br />
der Partikelgruppen erkennen ließ.<br />
Naturgemäß ziehen die einzelnen<br />
Testpersonen die Grenze zwischen einer<br />
positiven oder negativen Entscheidung<br />
bei verschiedenen Signal-Rausch-Verhältnissen,<br />
und damit<br />
schwankt auch die Summe der von jeder<br />
Testperson markierten Areale.<br />
Insgesamt versetzte jedoch das digitale<br />
System bereits ohne weitere spezielle<br />
Nachbearbeitung der Aufnahmen<br />
acht der zehn Ärzte in die Lage,<br />
ein bis drei Partikelgruppen mehr als<br />
mit dem konventionellen System zu<br />
detektieren. Aufgrund des realitätsnahen<br />
Testdesigns kann folglich davon<br />
ausgegangen werden, dass das<br />
digitale System des Senographe DMR<br />
2000 auch im Routinebetrieb Mammographien<br />
liefert, auf denen Mikrokalzifikationen<br />
eher oder besser als<br />
auf konventionellen Aufnahmen zu<br />
detektieren sind.<br />
Diskussion<br />
In einer nach Abschluss der vorliegenden<br />
Untersuchungen erschienenen<br />
Arbeit testeten Obenauer et al.<br />
(4) ebenfalls die Detektierbarkeit von<br />
mittels zerstoßener Eierschalen simulierten<br />
Mikrokalzifikationen vor<br />
antropomorphem Hintergrund. In<br />
grober Näherung verhalten sich einerseits<br />
die auf gleichen Querschnitt<br />
normierten Dicken der hier untersuchten<br />
80-µm-Goldpartikel und der<br />
von Obenauer et al. verwendeten<br />
150-µm-Kalkpartikel und andererseits<br />
die Schwächungskoeffizienten von<br />
Kalk und Gold wie 1:50, sodass das<br />
Produkt beider Größen und damit die<br />
Schwächung der Röntgenstrahlung<br />
durch das einzelne Partikel in beiden<br />
Fällen zumindest von gleicher Größenordnung<br />
sind. Unter diesen Voraussetzungen<br />
muss eine Detektionsrate<br />
für konventionelle und digitale<br />
Systeme von rund 17 bzw. 12 % für<br />
die 80-µm-Goldpartikel in dieser Arbeit<br />
und von rund 25 bzw. 15 % für<br />
die 150-µm-Kalkpartikel in der Arbeit<br />
von Obenauer et al. als ausgezeichnete<br />
Übereinstimmung für die Ermittlung<br />
einer Grenze der Detektierbarkeit<br />
vor inhomogenem Hintergrund<br />
angesehen werden.<br />
Diese hier gewonnenen Ergebnisse<br />
unterstützen ebenfalls die Kernaussage<br />
einer weiteren Arbeit von Obenauer<br />
und Mitarbeitern (2), auch wenn<br />
diese zum einen über eine Auswertung<br />
am Monitor die Vorteile der<br />
digitalen Mammographie deutlich<br />
weitergehender als in der hier vorliegenden<br />
Arbeit nutzen und zum anderen<br />
mit der Wiedergabe der Partikel<br />
an einem von vier genau bekannten<br />
Orten und vor homogenem Hintergrund<br />
letztendlich nur eine relative<br />
Bewertung kleiner Signal-Rausch-Verhältnisse<br />
vornehmen lassen und so<br />
insgesamt Partikel in einer Größenordnung<br />
bis herab zu 1 µm Dicke und<br />
100 µm Durchmesser detektieren.<br />
Partikel dieser Größe werden jedoch<br />
– wie vorliegende Arbeit zeigen<br />
soll – nur mit derart geringen Signal-<br />
Rausch-Verhältnissen abgebildet,<br />
dass ihre Detektion an unbekannten<br />
Orten und vor Mamma-äquivalentem<br />
Hintergrund praktisch unmöglich ist<br />
und ihnen folglich jegliche Relevanz<br />
für die primäre mammographische<br />
DIAGNOSTIK + THERAPIE<br />
FRAUENARZT ■ 43 (2002) ■ Nr. 1 53
DIAGNOSTIK + THERAPIE<br />
54<br />
Diagnostik von Mikroverkalkungen<br />
abgesprochen werden muss.<br />
Schlussfolgerungen<br />
Die bisher genutzte Bestimmung des<br />
Ortsauflösungsvermögens sowohl über<br />
einen Hochkontrast- als auch über einen<br />
Niedrigkontrast-Auflösungstest ist<br />
nicht geeignet, die Fähigkeit einer<br />
Mammographie-Einrichtung zur Abbildung<br />
von Mikrokalk zu beschreiben.<br />
Insbesondere wirkt bereits das hier<br />
untersuchte digitale System mit einem<br />
Auflösungsvermögen von etwa 4 Lp/<br />
mm nicht mehr limitierend bei der Detektion<br />
kleinster Mikrokalzifikationen,<br />
da diese bei genauer Kenntnis ihrer<br />
Position zwar auf der Aufnahme noch<br />
nachgewiesen werden können (s. Abb.<br />
2 unten), vor inhomogenem Hintergrund<br />
aber im Allgemeinen der Aufmerksamkeit<br />
entgehen.<br />
Unter dieser Voraussetzung fehlt<br />
auch die Bestätigung, dass die Erhöhung<br />
der Anforderungen an das<br />
Hochkontrast-Ortsauflösungsvermögen<br />
in den letzten Jahren zu einer<br />
verbesserten Erkennbarkeit kleiner<br />
Niedrigkontrast-Objekte und damit<br />
von Mikrokalk führte. Die Festlegung<br />
eines diesbezüglichen Grenzwertes<br />
ist unabhängig von den speziellen<br />
Problemen der digitalen Mammographie<br />
neu zu diskutieren.<br />
Die bisher verbreiteten Testmethoden,<br />
welche die Erkennbarkeit Mikrokalk-ähnlicher<br />
Partikel vor homogenem<br />
Hintergrund mittlerer optischer<br />
Dichte prüfen und damit insgesamt<br />
eine sehr kontrastreiche Wiedergabe<br />
in diesem Dichtebereich favorisieren,<br />
testen gleichzeitig eine Größenordnung<br />
von Partikeln, die praktisch<br />
nicht mehr relevant ist. Hier muss geprüft<br />
werden, ob die dadurch induzierten<br />
Modifikationen an Mammographie-Einrichtungen<br />
in der Regel<br />
auch zu einer generell verbesserten<br />
Detektion von Mikrokalk führen oder<br />
ob im Gegenteil durch die Steigerung<br />
des Kontrastes im mittleren Schwärzungsbereich<br />
immer größere Areale<br />
im real angefertigten Mammogramm<br />
FRAUENARZT ■ 43 (2002) ■ Nr. 1<br />
mit optischen Dichten weit oberhalb<br />
oder unterhalb des Optimums wiedergegeben<br />
werden, sodass sich dort<br />
eventuell vorhandener Mikrokalk bereits<br />
aufgrund des dann naturgemäß<br />
deutlich niedrigeren Kontrastes kaum<br />
noch vom Hintergrund abhebt. Vor<br />
einer weiteren physikalisch-technischen<br />
Optimierung der Mammographie-Einrichtungen<br />
bzw. vor der Festlegung<br />
neuer Grenzwerte erscheint es<br />
daher notwendig, ein allgemein anwendbares<br />
Prüfverfahren zu entwickeln,<br />
welches konkrete Aussagen<br />
über die Detektierbarkeit von Mikrokalzifikationen<br />
unter praxisnahen Bedingungen<br />
erlaubt.<br />
Erst wenn überhaupt Anhaltspunkte<br />
für das Vorhandensein von Mikrokalk<br />
vorliegen, stellt sich die Frage nach<br />
der Beurteilbarkeit der Form der einzelnen<br />
Partikel. Vor weiteren Überlegungen<br />
wird dann immer eine konventionelle<br />
oder digitale Vergrößerungsaufnahme<br />
indiziert sein, sodass<br />
mögliche Nachteile der Formerkennbarkeit<br />
bei Routineaufnahmen mit<br />
digitalen Systemen in diesem Zusammenhang<br />
als grundsätzlich nicht<br />
relevant angesehen werden können.<br />
Wenn die Auswertung zeigt, dass<br />
auch objektiv auf den Aufnahmen erkennbarer<br />
Mikrokalk vor dem Hintergrund<br />
normalen Mammagewebes<br />
unterhalb einer bestimmten Größe<br />
nicht mehr wahrgenommen wird, ergeben<br />
sich interessante Ansatzpunkte<br />
für eine nachträgliche computerunterstützte<br />
Suche nach diesbezüglichen<br />
Auffälligkeiten auf digital gewonnenen<br />
Aufnahmen.<br />
Insgesamt bietet das digitale System<br />
des Senograph DMR 2000 zumindest<br />
tendenziell bereits bessere Voraussetzungen<br />
für die Erkennbarkeit von<br />
Mikrokalk als konventionelle Systeme.<br />
Dazu kommen die herausragenden<br />
Möglichkeiten bei der Modifikation<br />
der Kontastwiedergabe sowie<br />
anderer Formen der Bildbearbeitung.<br />
Vor diesem Hintergrund ist die Genehmigung<br />
des Betriebs einer derartigen<br />
Mammographie-Einrichtung<br />
trotz des nominell nicht ausreichenden<br />
Ortsauflösungsvermögens durch<br />
das Bayerische Staatsministerium für<br />
Arbeit und Sozialordnung, Familie,<br />
Frauen und Gesundheit sowie durch<br />
die Kassenärztliche Vereinigung Bayerns<br />
gerechtfertigt und als ein positives<br />
Signal zur Weiterentwicklung<br />
der diagnostischen Möglichkeiten in<br />
der Mammographie zu werten.<br />
Danksagung<br />
Frau Krus von der Fa. Gammex-RMI,<br />
Bad Münstereifel, ist für die Beschaffung<br />
des „Antropomorphic Breast<br />
Phantom“ und Herrn Schmidtke von<br />
der Fa. PEHA med. Geräte GmbH,<br />
Sulzbach, für die Bereitstellung des<br />
Niedrigkontrast-Auflösungstests und<br />
für die Unterstützung bei der Anfertigung<br />
der Gold-Absorber ebenso zu<br />
danken wie den Ärzten, die sich für<br />
die Auswertung der Testaufnahmen<br />
zur Verfügung stellten.<br />
Literatur<br />
1. Küchler M, Friedrich M: Fokusabmessung<br />
und geometrische Unschärfe bei Mammographiegeräten.<br />
Akt Radiol 4 (1992) 205–<br />
211.<br />
2. Obenauer S, Hermann K-P, Schorn C et al.:<br />
Digitale Vollfeldmammographie: Dosisabhängige<br />
Detektion von simlierten Herdbefunden<br />
und Mikrokalzifikationen. Fortschr<br />
Röntgenstr 172 (2000) 1052–1056.<br />
3. Leitlinien der Bundesärztekammer zur<br />
Qualitätssicherung in der Röntgen<strong>diagnostik</strong>.<br />
Dt Ärztebl 92 (1995) A-2272–<br />
2278.<br />
4. Obenauer S, Hermann K-P, Schorn C et al.:<br />
Digitale Vollfeldmammographie: Phantomstudie<br />
zur Detektion von Mikrokalk.<br />
Fortschr Röntgenstr 172 (2000) 646–650.<br />
Autor<br />
Dr. rer. nat. Matthias Küchler<br />
Medizin-Physiker<br />
Böhmerwaldstr. 50<br />
85560 Ebersberg<br />
Tel. + Fax (0 80 92) 2 41 48<br />
Tel. dienstl. (0 89) 920 96 341<br />
Ärztliche Stelle bei der KV<br />
Bayerns