for tbildung + kongress - Frauenarzt
for tbildung + kongress - Frauenarzt
for tbildung + kongress - Frauenarzt
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
OPERATIVE GYNÄKOLOGIE<br />
Die hysteroskopische Resektion<br />
submuköser Myome<br />
Percy Brandner, Klaus J. Neis<br />
Seit ihrer Einführung vor rund 25 Jahren wurden umfangreiche<br />
Erfahrungen mit der hysteroskopischen Resektion submuköser<br />
Myome gesammelt. Was im Hinblick auf Indikationen, die Klassifikation<br />
der Myome und die er<strong>for</strong>derliche präoperative Diagnostik,<br />
eine eventuelle medikamentöse Vorbehandlung sowie<br />
strukturelle Voraussetzungen für den Eingriff, das Vorgehen bei<br />
der Operation und die Vermeidung von Komplikationen beachtet<br />
werden sollte, ist auf den folgenden Seiten zusammengestellt.<br />
Seit Neuwirth (21) im Jahre 1978 die<br />
erste transzervikale Resektion eines<br />
submukösen Myoms mittels eines<br />
modifizierten urologischen Resektoskops<br />
beschrieb, sind fünfundzwanzig<br />
Jahre vergangen. In dieser<br />
Zeitspanne wurde das urologische Instrumentarium<br />
schrittweise der<br />
transzervikalen Verwendung in der<br />
Gynäkologie angepasst. Parallel dazu<br />
wurden Operationsstandards geschaffen:<br />
Experten und Fachgesellschaften<br />
schufen eine praxisorientierte<br />
Klassifikation submuköser Myome,<br />
legten die Indikationen zur hysteroskopischen<br />
Myomresektion fest<br />
und beschrieben die Operationstechnik.<br />
Der ursprüngliche Therapieansatz<br />
der Laparotomie wurde dadurch<br />
innerhalb weniger Jahre nahezu<br />
gänzlich verdrängt (17).<br />
Im Interesse der Patientin war es unabdingbar,<br />
die hysteroskopische Resektion<br />
von submukösen Myomen in<br />
Standards zu fassen und zu vereinheitlichen.<br />
Dennoch ist es im Einzelfall<br />
nötig, innerhalb des gegebenen<br />
Rahmens das für die Patientin individuell<br />
beste Vorgehen zu wählen.<br />
Dies ist weit mehr als eine rein operativ-technische<br />
Aufgabe. Um eine<br />
im Einzelfall optimale Therapie zu gewährleisten,<br />
muss der Operateur vielmehr<br />
folgende Fragenkomplexe berücksichtigen:<br />
■ Ist eine sinnvolle Indikation zur<br />
Operation gegeben?<br />
■ Nach welchen anatomischen Gegebenheiten<br />
werden submuköse<br />
Myome eingeteilt?<br />
■ Welche präoperative Diagnostik<br />
ist sinnvoll?<br />
■ Soll eine medikamentöse Vorbehandlung<br />
mit GnRH-Analoga<br />
durchgeführt werden?<br />
■ Welche räumlichen, apparativen<br />
und organisatorischen Strukturen<br />
sind notwendig?<br />
■ Wie ist das Vorgehen intraoperativ<br />
zu wählen?<br />
■ Wie können Komplikationen<br />
verhindert werden?<br />
Nur wenn jede der oben gestellten<br />
Fragen vom Operateur für die einzelne<br />
Patientin zuverlässig beantwortet<br />
werden kann, darf ein zufriedenstellendes<br />
Operationsergebnis erwartet<br />
werden.<br />
Operationsindikation<br />
Von einer hysteroskopischen Myomresektion<br />
sollen zwei Patientenkollektive<br />
profitieren: Zum einen sind es<br />
die Patientinnen mit einer Anamnese<br />
von Sterilität oder Infertilität,<br />
zum anderen solche mit Metrorrhagien.<br />
Oft weist eine Patientin beide<br />
Symptome auf, beklagt eine Fertilitätsproblematik<br />
und uterine Hypermenorrhoen.<br />
Dennoch sollten beide<br />
Symptomenkomplexe bei der Indikationsstellung<br />
gesondert betrachtet<br />
werden.<br />
■ Indikation:<br />
Sterilität und Infertilität<br />
Die Häufigkeit von submukösen Myomen,<br />
Polypen, Synechien und Uterusfehlbildungen<br />
in Infertilitätskollektiven<br />
wird in älteren (7, 19, 27) und<br />
neueren (6, 10) hysteroskopischen<br />
Studien mit ca. 30–60 % angegeben.<br />
Selbst in Studien mit niedriger Rate<br />
an intrauteriner Pathologie beträgt<br />
deren Häufigkeit immerhin 9 % (31).<br />
Unsere Arbeitsgruppe, die hysteroskopische<br />
Untersuchungen an Patientinnen<br />
mit Missed Abortion unmittelbar<br />
vor der Kürettage vorgenommen<br />
hat, konnte diese Häufigkeit allerdings<br />
nicht bestätigen. Wir vermuten<br />
daher, dass bei zweizeitigen Hysteroskopien<br />
nach stattgehabten Aborten<br />
bisher häufig Normalbefunde überinterpretiert<br />
wurden und die überwiegende<br />
Mehrheit der Frühaborte doch<br />
eher genetisch bedingt ist (2).<br />
Autoren, die sich mit der Inzidenz<br />
hysteroskopisch diagnostizierter Cavumanomalien<br />
vor geplanter IVF (8,<br />
26) bzw. nach fehlgeschlagenen IVF-<br />
Zyklen (18) beschäftigten, berichteten<br />
über pathologische Befunde bei<br />
30–40 % der Untersuchten. Zwar ist<br />
die ätiologische Relevanz der erhobenen<br />
Befunde oft ungewiss (s.o.), dennoch<br />
sollte spätestens vor einem geplanten<br />
Embryotransfer ein auffälliges<br />
Cavum normalisiert werden, sofern<br />
dies durch einen minimal invasiven<br />
Eingriff wie eine operative Hysteroskopie<br />
möglich ist.<br />
Obgleich gedanklich der Analogieschluss<br />
von einem intrakavitären<br />
Myom zu einer Intrauterinspirale nahe<br />
liegt, ist die Frage, auf welche Weise<br />
submuköse Myome eine Infertilität<br />
begründen, noch nicht abschließend<br />
FORTBILDUNG + KONGRESS<br />
FRAUENARZT ■ 44 (2003) ■ Nr. 10 1063
FORTBILDUNG + KONGRESS<br />
1064<br />
beantwortet. Auch sind die Daten, inwieweit<br />
Kollektive mit Infertilität von<br />
einer hysteroskopischen Myomresektion<br />
profitieren, uneinheitlich.<br />
Während in einigen Arbeiten berichtet<br />
wird, dass sich durch die Myomresektion,<br />
besonders bei großen Myomen,<br />
in Infertilitätskollektiven die<br />
Häufigkeit eingetretener und ausgetragener<br />
Schwangerschaften steigern<br />
ließ (13, 28) und einzelne Autoren<br />
Schwangerschaftsraten von 47 % und<br />
Geburtenraten von 40 % nach Myomresektion<br />
schilderten (14), bemerkte<br />
eine andere Arbeitsgruppe, die den Erfolg<br />
einer IVF-Therapie nach Myomresektionen<br />
untersuchte, keinen Anstieg<br />
in der Häufigkeit angegangener<br />
Schwangerschaften (25). Wiederum<br />
andere Autoren beschrieben zwar einen<br />
positiven Effekt der Myomresektion<br />
bei Patientinnen mit sekundärer,<br />
nicht aber bei solchen mit primärer<br />
Infertilität (16).<br />
Unsicher ist auch, ob ein submuköses<br />
Myom nur durch mechanische Einengung<br />
des uterinen Cavum die Fertilität<br />
beeinträchtigt oder ob hier auch andere<br />
Faktoren wirksam sind. So ließ<br />
sich die Schwangerschaften- und Geburtenrate<br />
durch die Entfernung auch<br />
solcher Myome steigern, die – intramural<br />
oder subserös gelegen – keinen<br />
de<strong>for</strong>mierenden Einfluss auf die Gebärmutterhöhle<br />
hatten (11). Auch<br />
wurden nach der hysteroskopischen<br />
Resektion von submukösen Myomen<br />
deutlich schlechtere Schwangerschaftsraten<br />
erzielt, wenn bei der Patientin<br />
gleichzeitig intramurale Myome<br />
belassen wurden (1).<br />
Der tatsächliche Benefit, der für die<br />
infertile Patientin durch eine hysteroskopische<br />
Myomresektion resultiert,<br />
lässt sich aufgrund des oben Gesagten<br />
nicht exakt abschätzen. Dies<br />
liegt an den uneinheitlichen Studiendesigns<br />
und Patientenkollektiven verschiedener<br />
Autoren. Auch war in mehreren<br />
Studien die Fertilitätsstörung<br />
wenigstens eines Teiles der Patientinnen<br />
multifaktoriell bedingt (männliche<br />
Faktoren, endokrinologische Probleme),<br />
was die isolierte Bewertung<br />
FRAUENARZT ■ 44 (2003) ■ Nr. 10<br />
des Stellenwertes eines submukösen<br />
Myoms zusätzlich erschwert.<br />
In Zusammenschau der Literatur profitieren<br />
im Kollektiv der Infertilen am<br />
ehesten diejenigen Patientinnen, bei<br />
denen mit Ausnahme eines singulären,<br />
submukösen Myoms größeren<br />
Durchmessers keine weiteren Infertilitätsursachen<br />
bekannt sind.<br />
■ Indikation: Metrorrhagie<br />
Bereits seit der Arbeit von Word (32),<br />
der 1958 die diagnostische Wertigkeit<br />
der Abrasio bei Blutungsstörungen am<br />
Hysterektomiepräparat untersuchte,<br />
ist bekannt, dass es vor allem submuköse<br />
Myome sind, die sich selbst bei<br />
einer sorgfältigen Kürettage der Diagnose<br />
entziehen. Auch Brooks (5), der<br />
1988 nach vorausgegangener D&C zur<br />
Abklärung abnormer uteriner Blutungen<br />
nicht am Hysterektomiepräparat,<br />
sondern nun hysteroskopisch nach<br />
übersehenen Cavumanomalien suchte,<br />
wies auf die „remarkably high incidence<br />
of apparently missed pathologic<br />
factors (mainly submucous myomata)“<br />
hin. Aus diesem Grund sollte<br />
heute die Abklärung uteriner Blutungsstörungen<br />
durch eine alleinige<br />
fraktionierte Abrasio ohne begleitende<br />
Hysteroskopie obsolet sein (20).<br />
Es gibt eine typische Kombination von<br />
Angaben, die bereits bei der<br />
Anamnese-Erhebung den Verdacht auf<br />
eine intrakavitäre Raum<strong>for</strong>derung lenken<br />
kann. Insbesondere die klinische<br />
Konstellation einer (a) jungen Patientin<br />
mit (b) rezidivierenden, (c)<br />
anämisierenden und (d) trotz mehrerer<br />
(blinder) Abrasiones persistierenden<br />
Blutungsstörungen sollte den<br />
Therapeuten an ein submuköses Myom<br />
denken lassen und zu einer Hysteroskopie<br />
veranlassen (4).<br />
Wird bei Patientinnen mit solch einer<br />
Anamnese bei sonst regelhaftem Uterus<br />
hysteroskopisch ein submuköses<br />
Myom gesichert, so ist die Resektion<br />
Erfolg versprechend. Statt solche Patientinnen<br />
– wie in der Vergangenheit<br />
oft üblich – einer Hysterektomie zu-
Einteilung submuköser Myome<br />
Myomtyp Typ 0 Typ I Typ II<br />
hysteroskopischer<br />
Aspekt<br />
intramurale<br />
Ausdehnung<br />
gestielt<br />
Tab. 1: Einteilung submuköser Myome gemäß ihrem hysteroskopischen Erscheinungsbild nach<br />
Wamsteker (30).<br />
zuführen, sollte eine resektoskopische<br />
Myomabtragung angestrebt werden.<br />
Da das Myom die Ursache der Hypermenorrhoe<br />
darstellt, wird die verstärkte<br />
Blutung durch die Resektion<br />
meistens auf ein normales Maß reduziert.<br />
Dabei ist es bemerkenswert,<br />
dass sich selbst nach der Entfernung<br />
einzelner, nur erbsengroßer Myome<br />
schwere Hypermenorrhoen normalisieren<br />
können. Blutungsrezidive sind<br />
dagegen gehäuft, wenn eine Vielzahl<br />
von submukösen Myomen, Myome<br />
großen Durchmessers oder insgesamt<br />
vergrößerte Uteri vorliegen (12, 29).<br />
Eine mit der Resektion des Myoms in<br />
gleicher Sitzung durchgeführte Endometriumablation<br />
ist gewöhnlich nicht<br />
indiziert, da die Myomresektion bereits<br />
die kausale Therapie der Hypermenorrhoe<br />
darstellt.<br />
Während der therapeutische Nutzen<br />
der hysteroskopischen Myomresektion<br />
Restdicke des Myometriums<br />
D1<br />
spitzer stumpfer<br />
Winkel Winkel<br />
keine < 50 % > 50 %<br />
D1<br />
{ }<br />
R1 R2<br />
bei infertilen Patientinnen aufgrund<br />
des oben Dargelegten durchaus mit<br />
Einschränkungen betrachtet werden<br />
muss, wird die Patientin mit Metrorrhagie<br />
bei isoliertem intrakavitärem<br />
Myom mit hoher Wahrscheinlichkeit<br />
von der Resektoskopie profitieren.<br />
Einteilung submuköser<br />
Myome und präoperative<br />
Diagnostik<br />
Um bei der intrauterinen Myomchirurgie<br />
die Nomenklatur zu vereinheitlichen<br />
und um bereits präoperativ<br />
die Schwierigkeit der Operation<br />
abschätzbar zu machen, schlugen<br />
Wamsteker et al. 1993 (30) eine Einteilung<br />
der Myome nach ihrem hysteroskopischen<br />
Aspekt vor. Diese<br />
Klassifikation, die auch von der European<br />
Society <strong>for</strong> Gynaecological<br />
Endoscopy (ESGE) übernommen wurde,<br />
unterscheidet abhängig vom Aus-<br />
Abb. 1: Schematische Darstellung der myometranen Restdicke (R) als Resultierende des<br />
Myomtyps nach Wamsteker und des Myomdurchmessers (D).<br />
D2<br />
maß des intramuralen Myomanteiles<br />
drei Myomtypen (Tab. 1):<br />
■ Gestielte Myome werden dem<br />
Typ 0 zugeteilt.<br />
■ Weist das Myom zur umgebenden<br />
Uteruswand einen spitzen Winkel<br />
auf, so liegt es überwiegend<br />
intrakavitär (Typ I).<br />
■ Bei stumpfem Winkel liegt das<br />
Myom zum größeren Teil intramural<br />
(Typ II).<br />
Während die Myome der Typen 0<br />
und I als meist gefahrlos in einer Sitzung<br />
resezierbar gelten, drohen bei<br />
den tiefer liegenden Myomen des<br />
Typs II Flüssigkeitseinschwemmung<br />
und Uterusper<strong>for</strong>ation.<br />
Wenngleich sich die ESGE-Klassifikation<br />
in der Praxis bewährt hat, so bleiben<br />
doch Mängel: Das Risiko, bei der<br />
Resektion zu per<strong>for</strong>ieren, hängt in hohem<br />
Maße von der Restdicke zwischen<br />
Myombett und Uterusserosa ab. Diese<br />
Restdicke wird aber, wie in Abbildung<br />
1 demonstriert, nicht nur durch den<br />
Myomtyp nach Wamsteker, sondern<br />
auch durch den Durchmesser des Myoms<br />
bestimmt. So kann ein größeres<br />
Typ-I-Myom, wie es in Abbildung 1<br />
rechts dargestellt ist, durchaus überwiegend<br />
in die Gebärmutterhöhle hineinentwickelt<br />
sein, aufgrund seines<br />
Durchmessers aber ebenso nahe an die<br />
Serosa heranreichen, wie ein Typ-II-<br />
Myom kleineren Durchmessers.<br />
Um die Distanz zwischen Myom und<br />
äußerer Uteruswand einfach und zuverlässig<br />
darzustellen, hat sich neben<br />
der konventionellen transvaginalen<br />
Sonographie die Hydrosonographie<br />
(auch: SIS = Saline Infusion Sonography)<br />
bewährt. Bei diesem Verfahren<br />
wird der Uterus während einer vaginosonographischen<br />
Untersuchung simultan<br />
durch einen Katheter mit NaCl-<br />
Lösung perfundiert. Durch die Aufweitung<br />
des Cavum und die intrauterine<br />
Wasservorlaufstrecke lassen sich<br />
das Myom und seine Grenzflächen oft<br />
besser visualisieren als bei der einfachen<br />
Vaginosonographie. Sowohl der<br />
Winkel des Myoms gegenüber der<br />
Wandung als auch der Durchmesser<br />
des Myoms und die kritische Restdi-<br />
FORTBILDUNG + KONGRESS<br />
FRAUENARZT ■ 44 (2003) ■ Nr. 10 1065
FORTBILDUNG + KONGRESS<br />
1066<br />
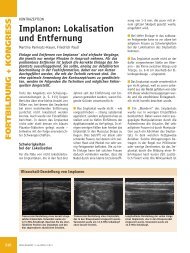
Abb. 2: Hydrosonographie: Erkennbar sind<br />
Myomtyp, Myomdurchmesser (D) und verbleibende<br />
Myometriumdicke (R).<br />
cke zur Außenwand des Uterus sind<br />
exakt erfassbar (Abb. 2). Die Untersuchung<br />
ist ohne großen Aufwand und<br />
meistens schmerzarm durchführbar.<br />
Zur differenzierten Operationsplanung<br />
submuköser Myome empfehlen wir,<br />
stets alle drei diagnostischen Methoden<br />
– Vaginosonographie, Hydrosonographie<br />
und diagnostische Hysteroskopie<br />
– zu kombinieren.<br />
Trotz exakter Diagnostik bleibt dem<br />
Operateur intraoperativ eine gewisse<br />
Restunsicherheit, da ein Teil der submukösen<br />
Myome keine konstante Beziehung<br />
zu der benachbarten Uteruswandung<br />
einnimmt. Vielmehr können<br />
vorwiegend intrakavitär gelegene Myome<br />
abhängig vom uterinen Distensionsdruck<br />
ihre Beziehung zum Myometrium<br />
ändern. Wir haben dieses<br />
in Abbildung 3 schematisch dargestellte,<br />
druckabhängige Versinken und<br />
Auftauchen submuköser Myome als<br />
„Myoma-Shift“-Phänomen bezeichnet.<br />
Durch die „Myoma Shift“ ist es möglich,<br />
dass ein Typ-I-Myom bei Erhö-<br />
FRAUENARZT ■ 44 (2003) ■ Nr. 10<br />
Das „Myoma-Shift“-Phänomen<br />
niedrig<br />
α < 90°<br />
Typ I<br />
hung des hysteroskopischen Distensionsdruckes<br />
nach intramural gedrängt<br />
und damit zum Typ-II-Myom wird.<br />
Wegen der gleichzeitig abnehmenden<br />
Restdicke der myometranen Deckschicht<br />
nimmt dabei die Per<strong>for</strong>ationsgefahr<br />
bei der Resektion zu. Da das<br />
Myom bei Absenken des Distensionsdruckes<br />
wieder hervortritt, empfiehlt<br />
es sich, die Resektion bei dem jeweils<br />
niedrigsten Druck vorzunehmen, der<br />
eine gute Übersicht über das Operationsfeld<br />
gewährleistet.<br />
Zur Frage der präoperativen<br />
Vorbehandlung mit GnRH-<br />
Analoga<br />
Die medikamentöse Vorbereitung einer<br />
hysteroskopischen Myomresektion<br />
durch die zweimalige Verabreichung<br />
eines GnRH-Analogons soll die Größe<br />
Was spricht für bzw. gegen den Einsatz von GnRH-Analoga?<br />
Einflussgröße pro Vorbehandlung kontra Vorbehandlung<br />
Anämie ausgeprägt wenig oder keine<br />
Myomtyp Typ II Typ 0 und I<br />
Durchmesser >3 cm
um 8 mm reduzierten Durchmesser<br />
von 3,2 cm aufweist.<br />
Auch in Hinblick auf die teilweise belastenden<br />
Nebenwirkungen und die erheblichen<br />
Kosten ist ein differenzierter<br />
und in jedem Falle abzuwägender<br />
Einsatz der GnRH-Analoga zu empfehlen.<br />
Wie in Tabelle 2 dargestellt, hängt<br />
die Entscheidung für oder gegen eine<br />
medikamentöse Vorbehandlung von<br />
mehreren Faktoren ab. Individuell<br />
muss unter anderem nach Lage, Größe,<br />
Myomtyp, Restdicke des Myometrium<br />
sowie nach Lokalisation und Anzahl<br />
der Myome, aber auch unter Berücksichtigung<br />
der Fähigkeiten des<br />
hysteroskopischen Operateurs der Einsatz<br />
der Analoga abgewogen werden.<br />
Dabei muss stets die gegebene Konstellation<br />
als Ganzes begriffen werden.<br />
Strukturelle Voraussetzungen<br />
und Sicherheitsaspekte<br />
Zweifelsohne stellt die Resektion submuköser<br />
Myome auf hysteroskopischem<br />
Wege eine minimal invasive<br />
Methode dar. Dies darf aber nicht darüber<br />
hinwegtäuschen, dass das Verfahren<br />
mit potenziell vital bedrohlichen<br />
Komplikationsmöglichkeiten<br />
vergesellschaftet ist. So kann eine<br />
Per<strong>for</strong>ation der Uteruswand und die<br />
Verbrennung des anliegenden Darmes<br />
mit der Hochfrequenzschlinge zu<br />
schwersten, kotigen Peritonitiden<br />
führen. Die übermäßige Intravasation<br />
des flüssigen Distensionsmediums<br />
kann durch eine hopotone Hyperhydratation<br />
(sog. TUR-Syndrom) intraoder<br />
postoperativ schwerste kardiozirkulatorische,<br />
renale und neurologische<br />
Störungen bis ad exitum nach<br />
sich ziehen. Diese können intra- und<br />
unmittelbar postoperativ, aber auch<br />
mit einer Latenz von mehreren Stunden<br />
auftreten (Hirnödem im Aufwachraum!).<br />
Aus diesem Grunde und insbesondere<br />
eingedenk der Tatsache, dass die Myomresektion<br />
meist einen elektiven<br />
Eingriff darstellt, muss der Operateur<br />
eine geeignete Infrastruktur vorhalten.<br />
Dieses bedingt, dass nur dort<br />
transzervikal operiert werden darf, wo<br />
eine Laparotomie, aber auch die situationsadäquate<br />
chirurgische Versorgung<br />
verletzter Organe (Blase, Darm)<br />
vorgenommen werden kann. Auch auf<br />
anästhesiologischer Seite müssen die<br />
personellen und apparativen Voraussetzungen<br />
so gewählt werden, dass<br />
die intra- und postoperative Überwachung<br />
der Patientin, aber auch das<br />
entsprechende Komplikationsmanagement<br />
gewährleistet ist.<br />
Durch Verwendung eines geeigneten<br />
Equipments kann der Operateur das<br />
Operationsrisiko minimieren. So sollte<br />
er nur spezielle gynäkologische Resektoskope<br />
verwenden. Auch sollte er<br />
bei den bis zu 45 Minuten dauernden<br />
Eingriffen aus Gründen der besseren<br />
Übersicht und der Dokumentation<br />
über eine Videokette arbeiten. Zur<br />
Vermeidung elektrischer Verbrennungen<br />
dürfen nur für die monopolare,<br />
transzervikale Hochfrequenzchirurgie<br />
zugelassene, elektolytfreie Distensionslösungen(Sorbit/Mannit-Gemisch,<br />
Glycin-Lösung) zum Einsatz<br />
kommen.<br />
Die Verwendung einer speziellen hysteroskopischen<br />
Pumpe ist ratsam.<br />
Durch solch eine Pumpe kann der<br />
Intrauterindruck auch bei großem Volumendurchsatz<br />
konstant gehalten<br />
werden, was die Übersicht verbessert.<br />
Auch der Einsatz eines modernen,<br />
chipgesteuerten Hochfrequenzgenerators<br />
ist zu empfehlen. Diese Geräte<br />
sind den älteren, ungeregelten Generatoren<br />
überlegen, da sie beim<br />
Schneiden automatisch die Stromabgabe<br />
auf das eben notwendige Minimum<br />
beschränken, welches benötigt<br />
wird, um an der Elektrode den für die<br />
Resektion notwendigen Lichtbogen<br />
entstehen zu lassen. Eine überflüssige<br />
Belastung der Patientin mit elektrischer<br />
und thermischer Energie wird<br />
so vermieden.<br />
Operationstechnik<br />
Standard ist heute die Resektion des<br />
Myoms mittels einer Schneideschlinge<br />
(„Cutting Loop“) und monopolarem<br />
Strom. Vor Beginn des Eingriffs wird<br />
der uterine Perfusionsdruck an der<br />
Pumpe auf 100±20 mmHg bei gleichzeitig<br />
hoher Spülleistung (ca. 400<br />
ml/min) vorgewählt. Die Leistung des<br />
Schneidestroms wird an dem chipgesteuerten<br />
HF-Generator auf ca. 80<br />
Watt begrenzt, der Koagulationsstrom<br />
auf ca. 60 Watt eingestellt. Es kann<br />
intraoperativ notwendig werden, diese<br />
Einstellungen zu ändern.<br />
Nachdem der Operateur das Cavum<br />
freigespült, Druck aufgebaut und<br />
Übersicht gewonnen hat, beginnt er<br />
mit der Resektion des Myoms. Dabei<br />
reseziert er senkrecht zur Myomoberfläche<br />
möglichst große Resektate<br />
(sog. Chips), die er versucht, kranial<br />
des Myoms im Fundus zu „parken“. Die<br />
Elektrode wird nur beim Zurückziehen<br />
aktiviert, um eine Per<strong>for</strong>ation zu vermeiden.<br />
Zum Abtransport des austretenden<br />
Blutes, aber auch zur Kühlung<br />
ist auf eine ausreichend hohe Spülrate<br />
zu achten.<br />
Die Resektion beginnt an der Apex des<br />
Myoms und schreitet in Richtung des<br />
intramuralen Myombettes <strong>for</strong>t (Abb. 4<br />
auf S. 1068). Mit der intermittierenden<br />
Kürettage der „Chips“ wird so lange<br />
wie möglich gewartet, da jedes<br />
Entfernen des Resektoskops zu einem<br />
Zusammenbrechen des Intrauterindruckes<br />
und damit zu Einblutungen<br />
führt. Andererseits darf die Kürettage<br />
nicht herausgezögert werden, wenn<br />
die Übersicht nachlässt. Die Resektion<br />
endet, wenn das native, an seiner zirkulär<br />
gefurchten Oberflächentextur erkennbare<br />
Myometrium erreicht ist<br />
(Abb. 5 auf S. 1068). Sind Myome<br />
vollständig intrakavitär gelegen und<br />
nur über einen Gewebestiel mit der<br />
Uteruswand verbunden (Typ-0-Myome),<br />
so ist der Operateur versucht, zunächst<br />
den Stiel zu durchtrennen. Dadurch<br />
wird aber der Stromfluss zur<br />
Neutralelektrode unterbrochen, was<br />
die weitere Zerkleinerung und die<br />
Extraktion des Myoms erschwert (3).<br />
Besonders schwierig ist die Resektion<br />
von Myomen mit großem intramuralen<br />
Anteil, also Typ-II- und großen<br />
FORTBILDUNG + KONGRESS<br />
FRAUENARZT ■ 44 (2003) ■ Nr. 10 1067
FORTBILDUNG + KONGRESS<br />
1068<br />
Abb. 4: Resektion eines Typ-0-Myoms mit der Schlingenelektrode. Abb. 5: Endzustand nach Myomresektion: zirkulär gefurchtes originäres<br />
Myometrium.<br />
Typ-I-Myomen. Zum einen besteht<br />
hier aufgrund der breiten Basis eine<br />
erhöhte Einschwemmungs- und Blutungsgefahr.<br />
Zum anderen ist wegen<br />
der geringen Restdistanz zwischen<br />
Myombett und Uterusserosa eine erhöhte<br />
Gefahr der Uterusper<strong>for</strong>ation<br />
gegeben.<br />
In diesen Fällen reseziert der Operateur<br />
das Myom zunächst eine „Loop-<br />
Breite“ in das umgebende Myometrium<br />
hinein. Damit ist eine Resektionstiefe<br />
analog der Endometriumablation<br />
erreicht. Oft prolabieren<br />
während der intermittierenden Kürettage<br />
intramurale Anteile des Myoms in<br />
das Cavum, sodass eine weitere Resektion<br />
möglich ist. Dieser Vorgang ist<br />
mehrfach wiederholbar und kann<br />
durch die intravenöse Verabreichung<br />
des Uterotonikums Methylergometrin<br />
(Methergin®) verstärkt werden. Da<br />
sich simultan mit der „Geburt“ des<br />
Myoms die bedeckende myometrane<br />
Außenwand <strong>for</strong>miert, lassen sich so<br />
auch intramurale Myomteile entfernen.<br />
Unter Umständen kann eine simultane,<br />
transabdominale Ultraschallkontrolle<br />
hilfreich sein.<br />
Vermeidung<br />
von Komplikationen<br />
Wie viel Distensionslösung in den<br />
Kreislauf eingeschwemmt wird, hängt<br />
vom eröffneten Gefäßquerschnitt,<br />
aber auch von der Dauer des Eingriffs<br />
FRAUENARZT ■ 44 (2003) ■ Nr. 10<br />
und dem Druckgefälle zum Gefäßsystem<br />
der Patientin ab. Aus diesem<br />
Grunde sollte der Operateur zügig,<br />
wenn auch nicht hastig vorgehen. Der<br />
Intrauterindruck sollte – auch mit<br />
Hinblick auf das „Myoma-Shift-Phänomen“<br />
– nur so hoch vorgewählt<br />
werden, wie für die Übersicht er<strong>for</strong>derlich.<br />
Gleichzeitig ist auf einen hohen<br />
Flüssigkeitsdurchsatz durch das<br />
Cavum zu achten, um Blut und Gasblasen<br />
sowie thermische Energie abzutransportieren.<br />
Stets muss zur Vermeidung<br />
einer Per<strong>for</strong>ation die Übersicht<br />
gewahrt bleiben. Auch darf die<br />
Elektrode nur beim Zurückziehen aktiviert<br />
werden, um die Per<strong>for</strong>ationsgefahr<br />
zu verringern.<br />
Ein wesentliches Sicherheitsprinzip<br />
ist es, die Operation lieber unvollendet<br />
abzubrechen, als eine Komplikation<br />
hervorzurufen. Überschreitet die<br />
eingeschwemmte Flüssigkeitsmenge<br />
1.000 ml (regelmäßige Bilanzierung!)<br />
oder treten erste klinische<br />
Symptome des TUR-Syndromes auf,<br />
so ist der Eingriff zu beenden, auch<br />
wenn den Operateur vermeintlich nur<br />
noch wenige Minuten von seinem Ziel<br />
trennen. Das Gleiche gilt für nachlassende<br />
Übersicht und die Befürchtung,<br />
zu tief in die Uteruswandung hineinzugeraten.<br />
Bei nachlassender Übersicht und<br />
grenzwertiger Flüssigkeitseinschwemmung<br />
hat sich ein zweizeitiges Vor-<br />
gehen bewährt, d.h. eine Re-Hysteroskopie<br />
und gegebenenfalls Nachresektion<br />
nach einigen Wochen (22).<br />
Bereits Stunden bis Tage nach der<br />
Erstresektion haben sich durch Nachlassen<br />
des Binnendruckes intramurale<br />
Myomteile in das Cavum verlagert.<br />
Auch hat sich dann meist die äußere<br />
Schicht der Uteruswand re<strong>for</strong>miert,<br />
wie wir durch hydrosonographische<br />
Untersuchungen zeigen konnten.<br />
Es empfiehlt sich, die Patientin bereits<br />
bei der Operationsaufklärung über die<br />
mögliche Notwendigkeit einer zweizeitigen<br />
Operation zu in<strong>for</strong>mieren. Ist<br />
dies geschehen, so wird sie eine eventuell<br />
notwendige Re-Hysteroskopie<br />
nicht als Ergebnis einer unzureichenden<br />
Operation, sondern als sinnvolle<br />
Maßnahme im Interesse der eigenen<br />
Sicherheit verstehen.<br />
Besonders in Infertilitätskollektiven<br />
sollte perioperativ und eventuell auch<br />
postoperativ eine Antbiotikagabe erfolgen,<br />
um einer Endometritis und<br />
intrauterinen Adhäsionen vorzubeugen.<br />
Der Wert einer zusätzlichen Östrogengabe<br />
zur schnelleren Abheilung<br />
des Endometriumdefekts ist bei endokrinologisch<br />
gesunden Frauen nicht<br />
belegt. Zwar werden auch größere Gewebeläsionen<br />
meist problemlos innerhalb<br />
weniger Wochen von Endometrium<br />
gedeckt, sicherheitshalber<br />
sollte man der Patientin aber zu Beginn<br />
eines der folgenden Zyklen eine
diagnostische Kontrollhysteroskopie<br />
zum Ausschluss von Adhäsionen anbieten.<br />
Literatur<br />
1. Bernard G, Darai E, Poncelet C et al.:<br />
Fertility after hysteroscopic myomectomy:<br />
effect of intramural myomas associated. Eur<br />
J Obstet Reprod Biol 88 (2000) 85–90.<br />
2. Brandner P, Neis KJ, Wagner S et al.:<br />
Uterine and fetal findings at hysteroscopic<br />
evaluation of spontaneous abortions be<strong>for</strong>e<br />
D&C. J Am Assoc Gynecol Laparosc 8 (2001)<br />
552–557.<br />
3. Brandner P, Neis KJ: Indikationen und<br />
Technik der transzervikalen Hochfrequenzchirurgie.<br />
frauenheilkunde plus 1 (1998)<br />
73–77.<br />
4. Brandner P, Neis KJ: Possibilities and limits<br />
of operative hysteroscopy: An update on<br />
transcervical resectoscopic uterine surgery.<br />
Int Surg 81 (1996) 259–265.<br />
5. Brooks PG, Serden SP: Hysteroscopic<br />
findings after unsuccessful dilatation and<br />
curettage after abnormal uterine bleeding.<br />
Am J Obstet Gynecol 158 (1988) 1354–<br />
1357.<br />
6. Campo R, Van Belle Y, Rombauts L et al.:<br />
Office mini-hysteroscopy. Hum Reprod<br />
Update 5 (1999) 73–81.<br />
7. Cohen MR, Dmowski WP: Modern hysteroscopy<br />
– diagnostic and therapeutical<br />
potential. Fertil Steril 24 (1973) 905–911.<br />
8. Dicker D, Goldman JA, Ashkenazi J et al.:<br />
The value of hysteroscopy in elderly<br />
women prior to in vitro fertilizationembryo<br />
transfer (IVF-ET): a comparative<br />
study. J In Vitro Fert Embryo Transf 7<br />
(1990) 267–270.<br />
9. Donnez J, Nisolle M, Clerckx F et al.:<br />
Advanced endoscopic techniques used in<br />
dysfunctional bleeding, fibroids and endometriosis,<br />
and the role of gonadotropinreleasing<br />
hormone agonist treatment. Br J<br />
Obstet Gynecol 101 (1994), Suppl 10, 2–9.<br />
10. Fabres C, Alam V, Balmaceda J et al:<br />
Comparison of ultrasonography and<br />
hysteroscopy in the diagnosis of intrauterine<br />
lesions in infertile women. J Am<br />
Assoc Gynecol Laparosc 5 (1998) 375–378.<br />
11. Fauconnier A, Dubuisson JB, Ancel PY<br />
et al.: Prognostic factors of reproductive<br />
outcome after myomectomy in infertile<br />
patients. Hum Reprod 15 (2000) 1751–<br />
1757.<br />
12. Fernandez H, Kadoch O, Kapella-Allouc S et<br />
al.: Résection hystéroscopique des myomes<br />
sous muqueux: résultats à long terme/<br />
Transcervical hysteroscopic resection of<br />
submucous leiomymas: long-term results.<br />
Ann Chir 126 (2001) 58–64.<br />
13. Fernandez H, Sefrioui O, Virelizier C et al.:<br />
Hysteroscopic resection of submucosal<br />
myomas in patients with infertility. Hum<br />
Reprod 16 (2001) 1489–1492.<br />
14. Goldenberg M, Sivan E, Sharabi Z et al:<br />
Outcome of hysteroscopic resection of<br />
submucous myomas <strong>for</strong> infertility. Fertil<br />
Steril 64 (1995) 714–716.<br />
15. Hackenberg R, Gesenhues T, Deichert U<br />
et al.: The response of uterine fibroids to<br />
GnRH-agonist treatment can be predicted<br />
in most cases after one month. Eur J Obstet<br />
Gynecol 45 (1992) 125–129.<br />
16. Hallez JP: Single-stage total hysteroscopic<br />
myomectomies: indications, techniques,<br />
and results. Fertil Steril 63 (1995) 703–708.<br />
17. Hucke J, Campo RL, de Bruyne F et al.: Die<br />
hysteroskopische Resektion submuköser<br />
Myome. Geburtsh Frauenheilk 52 (1992)<br />
214–218.<br />
18. Kirsop R, Porter R, Torode H et al: The role<br />
of hysteroscopy in patients having failed<br />
IVF/ET transfer cycles. Aust NZ J Obstet<br />
Gynecol 31 (1991) 263–264.<br />
19. Mohr J, Lindemann HJ: Hysteroscopy in the<br />
infertile patient. J Reprod Med 19 (1977)<br />
161–162.<br />
20. Neis KJ, Brandner P, Hepp H: Hysteroscopy<br />
– textbook and atlas. Thieme, Stuttgart,<br />
1994.<br />
21. Neuwirth RS: A new technique <strong>for</strong> and<br />
additional experience with hysteroscopic<br />
resection of submucous fibroids. Am J<br />
Obstet Gynecol 131 (1978) 91–94.<br />
22. Römer T: Hysteroscopic myoma resection of<br />
submucous myomas with largely intramural<br />
components. Zentralbl Gynakol 119 (1997)<br />
374–377.<br />
23. Römer T: Value of premedication with<br />
gonadotropin releasing hormone agonists<br />
be<strong>for</strong>e transcervical resection of solitary<br />
submucous myoma. Gynäkol Geburtshilfliche<br />
Rundschau 36 (1996) 194–196.<br />
24. Schweppe KW: Vergleichende Untersuchung<br />
zur medikamentösen Behandlung von<br />
Uterusmyomen mit GnRH-Agonisten.<br />
Fertilität 8 (1992) 183–187.<br />
25. Seoud MA, Patterson R, Muasher SJ et al.:<br />
Effects of prior myomectomy on in vitro<br />
fertilisation (IVF) per<strong>for</strong>mance. J Assist<br />
Reprod Genet 9 (1992) 217–221.<br />
26. Shamma FN, Lee G, Gutmann JN et al.:<br />
The role of office hysteroscopy in IVF. Fertil<br />
Steril 58 (1992) 1237–1239.<br />
27. Valle RF: Hysteroscopy in the evaluation of<br />
female infertility. Am J Obstet Gynecol 137<br />
(1980) 425–431.<br />
28. Varasteh NN, Neuwirth RS, Levin B et al.:<br />
Pregnancy rates after hysteroscopic<br />
polypectomy and myomectomy in infertile<br />
women. Obstet Gynecol 94 (1999) 168–171.<br />
29. Vercellini P, Zaina B, Yaylayan L et al:<br />
Hysteroscopic myomectomy: long-term<br />
effects on menstrual pattern and fertility.<br />
Obstet Gynecol 94 (1999) 341–347.<br />
30. Wamsteker K, Emanuel MH, de Kruif JH:<br />
Transcervical hysteroscopic resection of<br />
submucous fibroids <strong>for</strong> abnormal uterine<br />
bleeding: results regarding the degree of<br />
intramural extension. Obstet Gynecol 82<br />
(1993) 736–740.<br />
31. Woolcott R, Petchpud A: The efficacy of<br />
hysteroscopy: a comparison of women<br />
presenting with infertility versus other<br />
gynaecological symptoms. Aust NZ J Obstet<br />
Gynaecol 35 (1995) 310–313.<br />
32. Word B, Gravlee LC, Wideman GL: The<br />
fallacy of simple uterine curettage. Obstet<br />
Gynecol 12 (1958) 642–648.<br />
Für die Autoren<br />
Dr. med.<br />
Percy Brandner<br />
Stv. Chefarzt<br />
Frauenklinik<br />
Klinikum Saarbrücken<br />
Winterberg 1<br />
D-66119 Saarbrücken<br />
Tel. + 49 (0) 6 81 / 9 63 22 31<br />
Fax + 49 (0) 6 81 / 9 63 27 16<br />
E-Mail pbrandner@<br />
klinikum-saarbruecken.de<br />
FORTBILDUNG + KONGRESS<br />
FRAUENARZT ■ 44 (2003) ■ Nr. 10 1069