Vidrios del sistema LÍ2O-SÍO2 preparados por la técnica sol-gel
Vidrios del sistema LÍ2O-SÍO2 preparados por la técnica sol-gel
Vidrios del sistema LÍ2O-SÍO2 preparados por la técnica sol-gel
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Vidrios</strong> <strong>del</strong> <strong>sistema</strong> <strong>LÍ2O</strong>-<strong>SÍO2</strong> <strong>preparados</strong> <strong>por</strong> <strong>la</strong> <strong>técnica</strong> <strong>sol</strong>-<strong>gel</strong><br />
5.4<br />
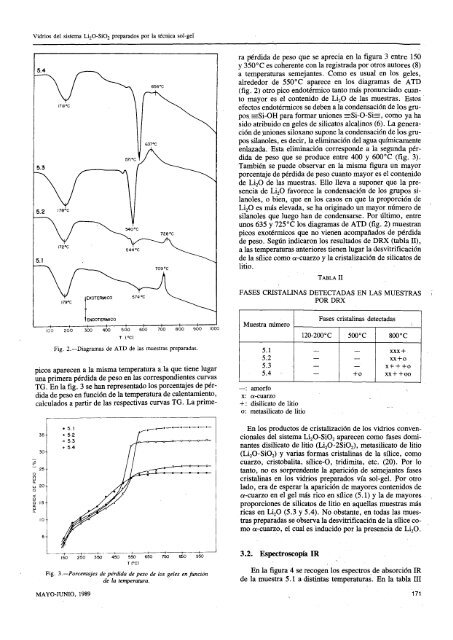
Fig. 2.—Diagramas de ATD de <strong>la</strong>s muestras preparadas.<br />
picos aparecen a <strong>la</strong> misma temperatura a <strong>la</strong> que tiene lugar<br />
una primera pérdida de peso en <strong>la</strong>s correspondientes curvas<br />
TG. En <strong>la</strong> fig. 3 se han representado los <strong>por</strong>centajes de pérdida<br />
de peso en función de <strong>la</strong> temperatura de calentamiento,<br />
calcu<strong>la</strong>dos a partir de <strong>la</strong>s respectivas curvas TG. La prime<br />
Fig. 3.—Porcentajes de pérdida de peso de los <strong>gel</strong>es en función<br />
de <strong>la</strong> temperatura.<br />
ra pérdida de peso que se aprecia en <strong>la</strong> figura 3 entre 150<br />
y 350°C es coherente con <strong>la</strong> registrada <strong>por</strong> otros autores (8)<br />
a temperaturas semejantes. Como es usual en los <strong>gel</strong>es,<br />
alrededor de 550°C aparece en los diagramas de ATD<br />
(fig. 2) otro pico endotérmico tanto más pronunciado cuanto<br />
mayor es el contenido de <strong>LÍ2O</strong> de <strong>la</strong>s muestras. Estos<br />
efectos endotérmicos se deben a <strong>la</strong> condensación de los grupos<br />
=Si-OH para formar uniones =Si-0-Si=, como ya ha<br />
sido atribuido en <strong>gel</strong>es de silicatos alcalinos (6). La generación<br />
de uniones siloxano supone <strong>la</strong> condensación de los grupos<br />
si<strong>la</strong>noles, es decir, <strong>la</strong> eliminación <strong>del</strong> agua químicamente<br />
en<strong>la</strong>zada. Esta eliminación corresponde a <strong>la</strong> segunda pérdida<br />
de peso que se produce entre 400 y 600°C (fig. 3).<br />
También se puede observar en <strong>la</strong> misma figura un mayor<br />
<strong>por</strong>centaje de pérdida de peso cuanto mayor es el contenido<br />
de <strong>LÍ2O</strong> de <strong>la</strong>s muestras. Ello lleva a suponer que <strong>la</strong> presencia<br />
de LÍ2Q favorece <strong>la</strong> condensación de los grupos si<strong>la</strong>noles,<br />
o bien, que en los casos en que <strong>la</strong> pro<strong>por</strong>ción de<br />
<strong>LÍ2O</strong> es más elevada, se ha originado un mayor número de<br />
si<strong>la</strong>noles que luego han de condensarse. Por último, entre<br />
unos 635 y 725°C los diagramas de ATD (fig. 2) muestran<br />
picos exotérmicos que no vienen acompañados de pérdida<br />
de peso. Según indicaron los resultados de DRX (tab<strong>la</strong> II),<br />
a <strong>la</strong>s temperaturas anteriores tienen lugar <strong>la</strong> desvitrificación<br />
de <strong>la</strong> sflice como a-cuarzo y <strong>la</strong> cristalización de silicatos de<br />
litio.<br />
TABLA II<br />
FASES CRISTALINAS DETECTADAS EN LAS MUESTRAS<br />
POR DRX<br />
Muestra número<br />
5.1<br />
5.2<br />
5.3<br />
5.4 -<br />
Fases cristalinas detectadas<br />
120-200°C 500°C 800°C j<br />
—<br />
+0<br />
XXX + .<br />
xx+o<br />
X+-H-I-0<br />
XX+-I-00<br />
—: amorfo ,<br />
x: a-cuarzo<br />
+ : disilicato de litio<br />
o: metasilicato de litio<br />
En los productos de cristalización de los vidrios convencionales<br />
<strong>del</strong> <strong>sistema</strong> <strong>LÍ2O</strong>-<strong>SÍO2</strong> aparecen como fases dominantes<br />
disilicato de litio (<strong>LÍ2O</strong>-251102), metasilicato de litio<br />
(LÍ20-SÍ02) y varias formas cristalinas de <strong>la</strong> sílice, como<br />
cuarzo, cristobalita, sflice-0, tridimita, etc. (20). Por lo<br />
tanto, no es sorprendente <strong>la</strong> aparición de semejantes fases<br />
cristalinas en los vidrios <strong>preparados</strong> vía <strong>sol</strong>-<strong>gel</strong>. Por otro<br />
<strong>la</strong>do, era de esperar <strong>la</strong> aparición de mayores contenidos de<br />
a-cuarzo en el <strong>gel</strong> más rico en sííice (5.1) y <strong>la</strong> de mayores<br />
pro<strong>por</strong>ciones de silicatos de litio en aquel<strong>la</strong>s muestras más<br />
ricas en LijO (5.3 y 5.4). No obstante, en todas <strong>la</strong>s muestras<br />
preparadas se observa <strong>la</strong> desvitrificación de <strong>la</strong> sflice como<br />
a-cuarzo, el cual es inducido <strong>por</strong> <strong>la</strong> presencia de <strong>LÍ2O</strong>.<br />
3.2. Espectroscopia IR<br />
En <strong>la</strong> figura 4 se recogen los espectros de absorción IR<br />
de <strong>la</strong> muestra 5.1 a distintas temperaturas. En <strong>la</strong> tab<strong>la</strong> III<br />
MAYO-JUNIO, 1989 171