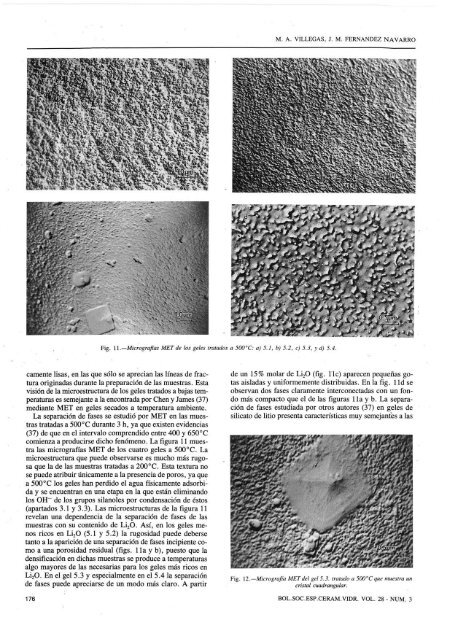
fet^"-':-;•••.• • Ssi. Fig. II.—Micrograf<strong>la</strong>s MET de los <strong>gel</strong>es tratados a 500°C: a) 5.1, b) 5.2, c) 5.3, y d) 5.4. camente lisas, en <strong>la</strong>s que sólo se aprecian <strong>la</strong>s líneas de fi'actura originadas durante <strong>la</strong> preparación de <strong>la</strong>s muestras. Esta visión de <strong>la</strong> microestructura de los <strong>gel</strong>es tratados a bajas temperaturas es semejante a <strong>la</strong> encontrada <strong>por</strong> Chen y James (37) mediante MET en <strong>gel</strong>es secados a temperatura ambiente. La separación de fases se estudió <strong>por</strong> MET en <strong>la</strong>s muestras tratadas a 500°C durante 3 h, ya que existen evidencias (37) de que en el intervalo comprendido entre 400 y 650°C comienza a producirse dicho fenómeno. La figura 11 muestra <strong>la</strong>s micrografías MET de los cuatro <strong>gel</strong>es a 500°C. La microestructura que puede observarse es mucho más rugosa que <strong>la</strong> de <strong>la</strong>s muestras tratadas a 200°C. Esta textura no se puede atribuir únicamente a <strong>la</strong> presencia de <strong>por</strong>os, ya que a 500 °C los <strong>gel</strong>es han perdido el agua físicamente adsorbida y se encuentran en una etapa en <strong>la</strong> que están eliminando los OH~ de los grupos si<strong>la</strong>noles <strong>por</strong> condensación de éstos (apartados 3.1 y 3.3). Las microestructuras de <strong>la</strong> figura 11 reve<strong>la</strong>n una dependencia de <strong>la</strong> separación de fases de <strong>la</strong>s muestras con su contenido de <strong>LÍ2O</strong>. Así, en los <strong>gel</strong>es menos ricos en <strong>LÍ2O</strong> (5.1 y 5.2) <strong>la</strong> rugosidad puede deberse tanto a <strong>la</strong> aparición de una separación de fases incipiente como a una <strong>por</strong>osidad residual (figs, lia y b), puesto que <strong>la</strong> densificación en dichas muestras se produce a temperaturas algo mayores de <strong>la</strong>s necesarias para los <strong>gel</strong>es más ricos en <strong>LÍ2O</strong>. En el <strong>gel</strong> 5.3 y especialmente en el 5.4 <strong>la</strong> separación de fases puede apreciarse de un modo más c<strong>la</strong>ro. A partir M. A. VILLEGAS, J. M. FERNANDEZ NAVARRO de un 15% mo<strong>la</strong>r de <strong>LÍ2O</strong> (fig. 11c) aparecen pequeñas gotas ais<strong>la</strong>das y uniformemente distribuidas. En <strong>la</strong> fig. lid se observan dos fases c<strong>la</strong>ramente interconectadas con un fondo más compacto que el de <strong>la</strong>s figuras lia y b. La separación de fases estudiada <strong>por</strong> otros autores (37) en <strong>gel</strong>es de silicato de litio presenta características muy semejantes a <strong>la</strong>s Fig. \2.—Micrografia MET <strong>del</strong> <strong>gel</strong> 5.3. tratado a 500°C que muestra un cristal cuadrangu<strong>la</strong>r. 176 BOL.SOC.ESP.CERAM.VIDR. VOL. 28 - NUM. 3
<strong>Vidrios</strong> <strong>del</strong> <strong>sistema</strong> <strong>LÍ2O</strong>-<strong>SÍO2</strong> <strong>preparados</strong> <strong>por</strong> <strong>la</strong> <strong>técnica</strong> <strong>sol</strong>-<strong>gel</strong> obtenidas aquí. El hecho de que en los vidrios <strong>preparados</strong> a partir de <strong>gel</strong>es <strong>la</strong> separación de fases se produzca a temperaturas menores que en los correspondientes vidrios <strong>preparados</strong> <strong>por</strong> fusión convencional, ha sido atribuido (22, 37, 38) a <strong>la</strong> presencia de agua químicamente en<strong>la</strong>zada en los <strong>gel</strong>es así como a <strong>la</strong>s diferentes historias térmicas de ambos vidrios y a <strong>la</strong> existencia de una fina <strong>por</strong>osidad en los <strong>gel</strong>es que influye directamente en el mecanismo de nucleación. La figura Uc muestra <strong>la</strong> presencia de núcleos cristalinos en los <strong>gel</strong>es, y en <strong>la</strong> figura 12 puede observarse un cristal cuadrangu<strong>la</strong>r inmerso en una microestructura separada e interconectada. Debido a que el disilicato de litio aparece, en general, en forma de cristales esferolíticos, cabe atribuir al metasilicato de litio los cristales de <strong>la</strong>s figuras 11c y 12. 4. CONCLUSIONES Se pueden preparar vidrios <strong>del</strong> <strong>sistema</strong> <strong>LÍ2O</strong>-<strong>SÍO2</strong> con hasta un 20% mo<strong>la</strong>r de <strong>LÍ2O</strong> <strong>por</strong> el procedimiento <strong>sol</strong>-<strong>gel</strong>, a temperaturas más bajas que <strong>la</strong>s requeridas para su obtención <strong>por</strong> <strong>técnica</strong>s usuales de fusión. Los vidrios <strong>preparados</strong> desvitrifican <strong>por</strong> encima de 500 °C dando lugar a a-cuarzo y silicatos de litio, en pro<strong>por</strong>ciones variables según su composición. La evolución térmica de los <strong>gel</strong>es se lleva a cabo <strong>por</strong> una pérdida a bajas temperaturas <strong>del</strong> agua asorbida y <strong>por</strong> <strong>la</strong> condensación de los grupos si<strong>la</strong>noles, con eliminación <strong>del</strong> agua químicamente en<strong>la</strong>zada, a temperaturas superiores a 500°C. La concentración de iones Li^ en <strong>la</strong>s muestras no sólo determina <strong>la</strong> formación de redes de sflice más o menos abiertas o discontinuas, debido a <strong>la</strong> presencia de oxígenos no puente; sino que influye directamente en el modo de eliminación <strong>del</strong> agua y en el proceso de densificación. A mayores contenidos de <strong>LÍ2O</strong> el agua se pierde con mayor facilidad o a temperaturas algo menores. Los materiales <strong>preparados</strong> presentan una separación de fases parecida a <strong>la</strong> de los correspondientes vidrios <strong>preparados</strong> <strong>por</strong> fusión, aunque el fenómeno en este caso se produce a temperaturas mucho menores (a partir de unos 500 °C), como consecuencia <strong>del</strong> elevado contenido de agua residual de los <strong>gel</strong>es que induce <strong>la</strong> inmiscibilidad. 5. BIBLIOGRAFÍA 1. GLASER, F. P.: Crystallization of lithium disilicate from <strong>LÍ2O</strong>-<strong>SÍO2</strong> g<strong>la</strong>sses. Phys. Chem. G<strong>la</strong>sses, 8 (1967), 224-232. 2. FREIMAN, S. W. y HENCH, L. L. : Kinetics of crystallization in <strong>LÍ2O</strong>-<strong>SÍO2</strong> g<strong>la</strong>sses. /. Am. Ceram. Soc, 51 (1968), 382-387. 3. JAMES, P. F.: Kinetics of crystal nucleation in lithium silicate g<strong>la</strong>sses. Phys. Chem. G<strong>la</strong>sses, 15 (1974), 95-105. 4. WoiGNiER, T., PHALIPPOU, J. y ZARZYCKI, J.: Evolution thermique des <strong>gel</strong>s d'alumino silicate alcalin. J. Phys. Coll. C9, sup. n°12, 43 (1982), 261-264. 5. PHALIPPOU, J., PRASSAS, M. y ZARZYCKI, J.: Crystallization of <strong>gel</strong>s and g<strong>la</strong>sses made from hot-pressed <strong>gel</strong>s. /. Non-Cryst. Solids, 48 (1982) 17-30. 6. VILLEGAS, M. A. y FERNÁNDEZ NAVARRO, J. M.: Alkaline silicate g<strong>la</strong>sses prepared via <strong>sol</strong>-<strong>gel</strong>. En Proc. 1st Int. Workshop on Non-Cryst. Solids. SanFeliú. Ed. M. D. Baró y N. C<strong>la</strong>vaguera. World Scientific, Phi<strong>la</strong><strong>del</strong>phia (1986), págs. 433-440. 7. ORCEL, G., PHALIPPOU, J. y HENCH, L. L.: Processing and structural evolution of (xLÍ20-(l-x)Na20)- •A1203-2SÍ02 <strong>gel</strong>s. /. Non-Cryst. Solids, 82 (1986), 301-306. 8. CoNGSHAN, Z., PHALIPPOU, y ZARZYCKI, J.: Influence of trace alkali ions on the crystallization behaviour of silica <strong>gel</strong>s. /. Non-Cryst. Solids, 82 (1986), 321-328. 9. SCHWARTZ, I., ANDERSON, P., DELAMBILLY, H. y KLEIN, L. C: Stability of lithium silicate <strong>gel</strong>s. /. Non- Cryst. Solids., 83 (1986), 391-399. 10. HAYRI, E. A. y GREENBLATT, M.: The preparation and ionic conductivity of <strong>sol</strong>-<strong>gel</strong>s in the <strong>LÍ2O</strong>- P2O3-<strong>SÍO2</strong> system. /. Non-Cryst. Solids, 94 (1987), 387-401. 11. BRANDA, F., ARONNE, A., MAROTTA, A. y BURI, A. : LÍ20-2SÍ02 <strong>sol</strong>-<strong>gel</strong> g<strong>la</strong>ss. /. Mat. Sei. Lett., 6 (1987), 203-206. 12. SAKKA, S.: G<strong>la</strong>sses and g<strong>la</strong>ss-ceramics from <strong>gel</strong>s. J. Non-Cryst. Solids, 73 (1985), 651-660. 13. BOILOT, J. P. y C0LOMBAN, Ph.: Sodium and lithium superionic <strong>gel</strong>s and g<strong>la</strong>sses. /. Mat. Sei. Lett., 4 (1985), 22-24. 14. RAY AINE, D., SEMINEL, A., CHARBOUILLOT, Y. y ViNCENS, M.: A new family of organically modified silicates prepared from <strong>gel</strong>s. /. Non-Cryst. Solids, 82 (1986), 210-219. 15. VILLEGAS, M. A. y FERNÁNDEZ NAVARRO, J. M.: Caracterización de <strong>gel</strong>es 5R20-95SÍ02 mediante medidas de conductividad eléctrica y espectroscopia de infrarrojo próximo. Bol. Soc. Esp. Cerám. Vidr., 26 (1987), 235-242. 16. VILLEGAS, M. A., JURADO, J. R. y FERNÁNDEZ NA VARRO, J. M.: Dielectric properties of g<strong>la</strong>sses prepared via <strong>sol</strong>-<strong>gel</strong>. /. Mat. Sei. (Aceptado, en prensa.) 17. KRACEK, F. C: Binary system <strong>LÍ2O</strong>-<strong>SÍO2</strong>. /. Phys. Chem., 34 (1930), 2.641-2.650. 18. RINCÓN, J. M.: Estudio de nuevos vidrios y materiales vitrocristalinos <strong>del</strong> <strong>sistema</strong> LÍ20-CdO-Si02 con posible utilidad en <strong>la</strong> industria nuclear. Tesis doctoral, Madrid (1982). Págs. 27-30. 19. VILLEGAS, M. A. y FERNÁNDEZ NAVARRO, J. M.: Preparación de vidrios de silicatos alcalinos <strong>por</strong> el método <strong>sol</strong>-<strong>gel</strong>. Bol. Soc. Esp. Cerám. Vidr., 26 (1987), 99-108. 20. AUSTIN, A. E.: X-ray diffraction data for compounds in systems <strong>LÍ2O</strong>-<strong>SÍO2</strong> and BaO-Si02. J. Am. Ceram. Soc, 30 (1947), 218-220. 21. DECOTTIGNIES, M., PHALIPPOU, J. y ZARZYCKI, J.: Synthesis of g<strong>la</strong>sses by hot-pressing of <strong>gel</strong>s. /. Mat. Sei., 13 (1978), 2.605-2.618. 22. VILLEGAS, M. A. y FERNÁNDEZ NAVARRO, J. M.: Characterizacion and study of Na20-B203-Si02 g<strong>la</strong>sses^ prepared by the <strong>sol</strong>-<strong>gel</strong> method. J. Mat. ScL, 23 (1988), 2.142-2.152. 23. HAALAND, D. M. y BRINKER, C. J.: In situ FT-IR studies of oxide and oxynitride <strong>sol</strong>-<strong>gel</strong> derived thin films. Mat. Res. Soc. Symp. Proc, 32 (1984), 261-213. 24. PRASAS, M. y HENCH, L. L.: Physical chemical factors in <strong>sol</strong>-<strong>gel</strong> processing. Processing of Ceramics, G<strong>la</strong>sses and Composites. Edit. J. Wiley and Sons, New York (1984). Págs. 100-125, MAYO-JUNIO, 1989 177