Les électrons dans un potentiel périodique. Structure de bande - EPFL
Les électrons dans un potentiel périodique. Structure de bande - EPFL
Les électrons dans un potentiel périodique. Structure de bande - EPFL
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
22 CHAPITRE 5. STRUCTURE DE BANDE<br />
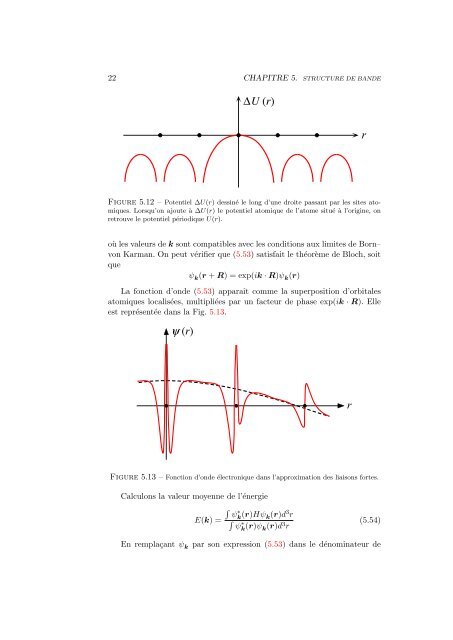
Figure 5.12 – Potentiel ∆U(r) <strong>de</strong>ssiné le long d’<strong>un</strong>e droite passant par les sites atomiques.<br />
Lorsqu’on ajoute à ∆U(r) le <strong>potentiel</strong> atomique <strong>de</strong> l’atome situé à l’origine, on<br />
retrouve le <strong>potentiel</strong> <strong>périodique</strong> U(r).<br />
où les valeurs <strong>de</strong> k sont compatibles avec les conditions aux limites <strong>de</strong> Born–<br />
von Karman. On peut vérifier que (5.53) satisfait le théorème <strong>de</strong> Bloch, soit<br />
que<br />
ψ k(r + R) = exp(ik · R)ψ k(r)<br />
La fonction d’on<strong>de</strong> (5.53) apparaît comme la superposition d’orbitales<br />
atomiques localisées, multipliées par <strong>un</strong> facteur <strong>de</strong> phase exp(ik · R). Elle<br />
est représentée <strong>dans</strong> la Fig. 5.13.<br />
Figure 5.13 – Fonction d’on<strong>de</strong> électronique <strong>dans</strong> l’approximation <strong>de</strong>s liaisons fortes.<br />
Calculons la valeur moyenne <strong>de</strong> l’énergie<br />
E(k) =<br />
ψ ∗ k (r)Hψ k(r)d 3 r<br />
ψ ∗ k (r)ψ k(r)d 3 r<br />
r<br />
r<br />
(5.54)<br />
En remplaçant ψ k par son expression (5.53) <strong>dans</strong> le dénominateur <strong>de</strong>