Methodes d'évaluation de la biomasse
Methodes d'évaluation de la biomasse
Methodes d'évaluation de la biomasse
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Métho<strong>de</strong>s <strong>de</strong> mesure <strong>de</strong> <strong>la</strong> Croissance
Constitution <strong>de</strong>s Microorganismes<br />
Protéines 52.4%<br />
Polysacchari<strong>de</strong>s 16.6%<br />
Lipi<strong>de</strong>s 9.4%<br />
ARN 15.4%<br />
ADN 3.2%
Composition Elémentaire<br />
95% du poids sec d’une cellule sont composés d’ éléments<br />
majeurs : C, O, H, N, S, P, K + , Ca 2+ , Mg 2+ et Fe 2+ …<br />
C (50%)<br />
O (20%)<br />
N (14%)<br />
H (8%)<br />
P (3%)<br />
S, (9%)<br />
Na et K (1% chacun)<br />
Ca , Mg (0,5% chacun)<br />
Fe (0,2%)<br />
les oligoéléments (0,2% cumulé)<br />
(éléments traces : Co, Zn, Mo, Cu, Mn, Ni, W, Se..)
Élémént<br />
C<br />
O<br />
N<br />
H<br />
P<br />
S<br />
Teneur pour 100g <strong>de</strong> cellules<br />
m(g)<br />
50%<br />
20%<br />
14%<br />
8%<br />
3%<br />
9%<br />
MA<br />
0,28<br />
Formu<strong>la</strong>tion pour un microorganisme<br />
CH 1,92 O 0,3 N 0,24<br />
12<br />
16<br />
14<br />
1<br />
31<br />
32<br />
Nbre m/MA<br />
4,16<br />
1,25<br />
1<br />
8<br />
0,1<br />
Pour 1C<br />
1<br />
0,3<br />
0,24<br />
1,92<br />
0,02<br />
0,067
CO 2 + H 2 O +<br />
CH 3 COOH + C 2 H 5 OH<br />
C 6 H 12 O 6 + NH 4 CL + O 2 +<br />
CH 1,92 O 0,3 N 0,24<br />
ADP + Pi<br />
ATP<br />
CH 1,92 O 0,3 N 0,24<br />
CH 1,92 O 0,3 N 0,24 : 50% <strong>de</strong> protéines<br />
CHALEUR
Mesure du nombre : comptage total<br />
<strong>de</strong>s particules<br />
-Chambre <strong>de</strong> comptage <strong>de</strong> Petroff-Hausser, hémocytomètres, hématimètre<br />
- rapi<strong>de</strong>, peu sensible, pas <strong>de</strong> distinction vivante/morte (sauf si coloration)<br />
-plus facile si coloration<br />
- besoin <strong>de</strong> concentration importante (>10 7 cellules /ml)
Cellule <strong>de</strong> Ma<strong>la</strong>ssez
Cellule <strong>de</strong> Petroff-Hausser<br />
25 carrés couvrent une surface <strong>de</strong><br />
1mm2.<br />
On compte les bactéries (x) dans<br />
quelques carrés pris au hasard (n).<br />
Nbre total <strong>de</strong> bactéries dans 1mm2<br />
X = (x/n) 25<br />
La chambre a une profon<strong>de</strong>ur <strong>de</strong><br />
0,02mm ( Volume: 0,02mm3)<br />
Bactérie/mm3 = (x/n) 25 . 1/0,02<br />
1mm3 = 1µl
-marquage fluorescence (épifluorescence – ex : acridine orange<br />
ou DAPI – ADN – avec orangé d’acridine, on peut en théorie<br />
distinguer les bactéries vivantes qui sont vertes, et les bactéries<br />
mortes qui sont rouges en fonction du <strong>de</strong>gré d’ouverture <strong>de</strong> <strong>la</strong><br />
chaîne d’ADN)
-Obtention d'une son<strong>de</strong> marquée par NickTrans<strong>la</strong>tion.<br />
-Hybridation in situ avec l'ADN dénaturé.<br />
-Traitement avec <strong>de</strong>s anticorps fluorescents pour localiser<br />
le gène d'intérêt au microscope à épifluorescence
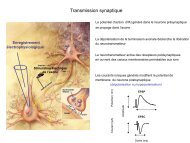
Evaluation of the physiological state of<br />
Lactobacillus helveticus CNRZ32<br />
in different conditions using in situ<br />
hybridization.<br />
(a) Cells at the beginning of the exponential<br />
growth phase, incubated in MRS broth for 1 h<br />
at 42 °C.<br />
(b) Cells in exponential growth phase,<br />
incubated in MRS broth for 3 h at 42 °C<br />
(control).<br />
(c) Cells submitted to a stress treatment in<br />
acid MRS broth (pH 3.5–3.6) for 2 h at 42 °C<br />
after growth in optimal conditions for 1 h at<br />
42 °C.<br />
(d) Cells incubated for 24 h in MRS broth at<br />
42 °C.
Coulter Counter<br />
Cytomètre <strong>de</strong> flux<br />
COMPTAGE AUTOMATIQUE
Compteurs électriques <strong>de</strong> particules <strong>de</strong> type Coulter<br />
pour grands microorganismes (levures non fi<strong>la</strong>menteuses, protozoaires, algues)
La P<strong>la</strong>ge <strong>de</strong> mesure varie entre 1 et<br />
360µm<br />
Principe du Coulter Counter<br />
Basé sur <strong>la</strong> variation <strong>de</strong> résistance<br />
provoquée par les particules p<strong>la</strong>cées dans un<br />
champ électrique.<br />
Résistance mesurée entre 2<br />
électro<strong>de</strong>s <strong>de</strong> part et d’autre d’un orifice<br />
calibré à travers lequel les particules sont<br />
aspirées.<br />
Chaque fois qu’une particule<br />
traverse l’orifice, elle dép<strong>la</strong>ce son propre<br />
volume d’électrolyte et génère un signal<br />
proportionnel au volume <strong>de</strong> liqui<strong>de</strong> dép<strong>la</strong>cé.<br />
Un dispositif manométrique permet<br />
<strong>de</strong> mesure le volume <strong>de</strong> liqui<strong>de</strong> aspiré et<br />
connaître <strong>la</strong> concentration <strong>de</strong> particule
La Cytométrie <strong>de</strong> Flux
Un système complexe <strong>de</strong> filtres et <strong>de</strong> détecteurs permet <strong>de</strong><br />
faire plusieurs mesures simultanées<br />
(2 mesures <strong>de</strong> diffraction et <strong>de</strong>s mesures <strong>de</strong> fluorescence).
MESURES INDIRECTES DU NOMBRE DE<br />
CELLULES
Dénombrement <strong>de</strong>s bactéries cultivables<br />
Dénombrement <strong>de</strong>s CFU (unités formant colonies) sur un milieu soli<strong>de</strong> le plus souvent<br />
métho<strong>de</strong> précise mais longue et problème si les amas <strong>de</strong> cellules ne sont pas dissociés<br />
Dilutions en série suivies du dépôt d’un volume connu sur boîte :
Filtration sur Membrane
Mesures visuelles d’un trouble<br />
il faut que <strong>la</strong> concentration en bactéries atteigne au moins 10 7 /ml afin<br />
que le milieu commence à apparaître trouble.
-turbidimétrie :estimation d'une concentration particu<strong>la</strong>ire par l'évaluation<br />
(macroscopique, à l'oeil) d'un trouble et par comparaison avec une gamme étalon<br />
ex: étalon <strong>de</strong> Mac Far<strong>la</strong>nd<br />
-peu précise<br />
- donne un ordre <strong>de</strong> gran<strong>de</strong>ur :<br />
détermination visuelle <strong>de</strong> <strong>la</strong> turbidité :<br />
Pas <strong>de</strong> trouble = moins <strong>de</strong> 10 7 bactéries/ml<br />
Trouble léger = 10 7 –10 8 /ml<br />
Trouble important = 10 8 –10 9 /ml<br />
Trouble très important = plus <strong>de</strong> 10 9 /ml (les cultures<br />
atteignent rarement plus <strong>de</strong> 10 10 /ml)<br />
Utilisation éventuelle d’une gamme standard <strong>de</strong> McFar<strong>la</strong>nd :<br />
0,5Mc far<strong>la</strong>nd = 10 7 –10 8 CFU/ml -
Technique du Nombre le plus probable
Mesure <strong>de</strong> <strong>la</strong> masse<br />
-directe : détermination du poids sec <strong>de</strong>s organismes -<br />
culture/centrifugation/<strong>la</strong>vage/séchage à 100-110°C dans un four<br />
-/pesées –<br />
- métho<strong>de</strong> longue et peu sensible/précise, pas <strong>de</strong> distinction entre les vivantes<br />
et les mortes.
Mesure <strong>de</strong> l’absorbance<br />
Dédié à <strong>la</strong> mesure <strong>de</strong> particules d’une taille typiquement comprise entre 0.05<br />
µm et 5 µm.<br />
l’importance <strong>de</strong> <strong>la</strong> diffraction <strong>de</strong> <strong>la</strong> lumière est mesurée par un<br />
spectrophotomètre à <strong>de</strong>s longueurs d’on<strong>de</strong>s autour <strong>de</strong> 600 nm (pour minimiser<br />
absorbance du milieu).<br />
-Métho<strong>de</strong> précise, simple, rapi<strong>de</strong> mais ne distingue pas cellules vivantes et<br />
mortes, peu sensible (il faut plus <strong>de</strong> 10 6 bactéries/ml)<br />
-problème <strong>de</strong>s milieux très colorés ou très troubles<br />
– Nécessité d’être dans <strong>la</strong> gamme <strong>de</strong> linéarité ou diluer <strong>la</strong> solution.
Io I lumière diffractée (mesurée<br />
par néphélomètre)<br />
lumière transmise (mesurée<br />
par spectrophomtomètre)
DO à<br />
600nm<br />
DO = f (C)<br />
Mg/ml<br />
Courbe poids sec<br />
-Dans <strong>la</strong> partie linéaire, l’intensité transmise peut être déterminée par <strong>la</strong> loi<br />
<strong>de</strong> Beer-Lambert<br />
.<br />
Loi <strong>de</strong> Beer-Lambert : A = D.O = log (I 0 / I) = ε l C<br />
où A:: l'absorbance, D.O: <strong>la</strong> <strong>de</strong>nsité optique<br />
Ιο l'intensité lumineuse inci<strong>de</strong>nte, Ι: l'intensité lumineuse<br />
transmise,<br />
ε: le coefficient d'extinction mo<strong>la</strong>ire caractéristique <strong>de</strong> <strong>la</strong> substance<br />
étudiée à une longueur d'on<strong>de</strong> donnée en L mol -1 cm -1 ,<br />
L: l'épaisseur traversée en cm et C: <strong>la</strong> concentration en mol.L -1 .
Centrifugation<br />
Surnageant<br />
Culot repris dans l’eau/<strong>la</strong>vage<br />
Centrifugation<br />
Surnageant<br />
Solution <strong>de</strong> Travail: DO=1<br />
2/10 4/10 6/10 8/10 1<br />
DO(600nm)<br />
Confection <strong>de</strong> <strong>la</strong> courbe Poids sec<br />
Culot repris dans un volume 20 ml<br />
Solution mère DO = 50 : x mg/ml<br />
Db: mg/ml<br />
10ml mis à sécher<br />
Les cellules sont pesées<br />
Densité bactérienne: mg/ml
Mesure du Volume Cellu<strong>la</strong>ire global<br />
Fast, reproducible and reliable <strong>de</strong>termination of biomass in suspension cell cultures<br />
with VoluPAC tubes<br />
Joachim Luecke Nature Methods - 3, (2006)<br />
For PCV measurements, aliquots of a<br />
well-mixed suspension culture (CHO<br />
cells) (100–1,000µl in multiples of<br />
100µl) were transferred into VoluPAC<br />
tubes.<br />
The tubes were centrifuged in a<br />
microcentrifuge equipped with a<br />
swinging bucket rotor for 1 min at<br />
2,500g (5,000 r.p.m.).<br />
The height of the cell pellet was<br />
visually <strong>de</strong>termined by taking a reading<br />
from the capil<strong>la</strong>ry graduation;<br />
alternatively, an image analysis <strong>de</strong>vice<br />
was used.
Mesure <strong>de</strong> l’activité<br />
- consommation <strong>de</strong> substrat<br />
- mesure <strong>de</strong> constituants cellu<strong>la</strong>ires<br />
-dosage <strong>de</strong>s protéines<br />
- dosage <strong>de</strong> l’azote cellu<strong>la</strong>ire (Kjeldal)<br />
- nucléoti<strong>de</strong>s tels ATP, FAD, FMN (ex : ATP par luciférase <strong>de</strong><br />
luciole dépendante <strong>de</strong> l’ATP. On peut détecter 10 4 bactéries/ml)<br />
- mesure <strong>de</strong>s produits d’excrétions<br />
(ex : 14 CO 2 )<br />
- mesure <strong>de</strong>s variations physico-chimiques du milieu<br />
(ex :pH, potentiel redox, conductivité/impédance, chaleur)
Très sensible: détecte 10 -10 mg d’ATP soit 10 -16 moles (1O -10 µmoles)<br />
Pool d’ATP chez E. coli: 4,5-7,5µmoles/g<br />
Turn over: 4-8/s<br />
luciferase