Téléchargez
Téléchargez
Téléchargez
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
16<br />
La thermodynamique chimique<br />
L’INFLUENCE DE LA TEMPÉRATURE<br />
SUR LA FONCTION DE GIBBS<br />
Comme les ∆H et les ∆S varient peu avec la température, les variations de la fonction<br />
de Gibbs selon la température dépendent essentiellement du terme -T∆S. Aux<br />
températures relativement basses, le signe de ∆G est généralement déterminé par<br />
le signe de ∆H; à mesure que la température augmente, la contribution du terme -<br />
T∆S devient de plus en plus importante et plusieurs situations peuvent se produire<br />
selon les signes respectifs de ∆H et de ∆S, comme l’indique la figure suivante.<br />
4<br />
∆G0<br />
∆H0<br />
B<br />
∆S négatif<br />
–T ∆S0<br />
Réaction favorisant les<br />
réactifs (réaction inverse)<br />
∆G∆HT ∆S0<br />
∆S positif<br />
–T ∆S0<br />
2<br />
0<br />
∆H0<br />
A<br />
∆S positif<br />
–T ∆S0<br />
∆S négatif<br />
–T ∆S0<br />
3<br />
Réaction favorisant les<br />
produits (réaction directe)<br />
∆G∆HT ∆S0<br />
∆G0<br />
∆H prépondérant<br />
1<br />
T ∆S prépondérant<br />
supérieur à ∆H<br />
T<br />
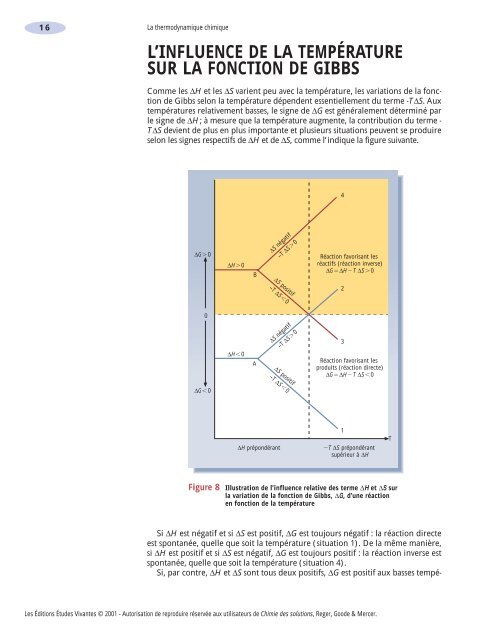
Figure 8 Illustration de l’influence relative des terme ∆H et ∆S sur<br />
la variation de la fonction de Gibbs, ∆G, d’une réaction<br />
en fonction de la température<br />
Si ∆H est négatif et si ∆S est positif, ∆G est toujours négatif : la réaction directe<br />
est spontanée, quelle que soit la température (situation 1). De la même manière,<br />
si ∆H est positif et si ∆S est négatif, ∆G est toujours positif : la réaction inverse est<br />
spontanée, quelle que soit la température (situation 4).<br />
Si, par contre, ∆H et ∆S sont tous deux positifs, ∆G est positif aux basses tempé-<br />
Les Éditions Études Vivantes © 2001 - Autorisation de reproduire réservée aux utilisateurs de Chimie des solutions, Reger, Goode & Mercer.