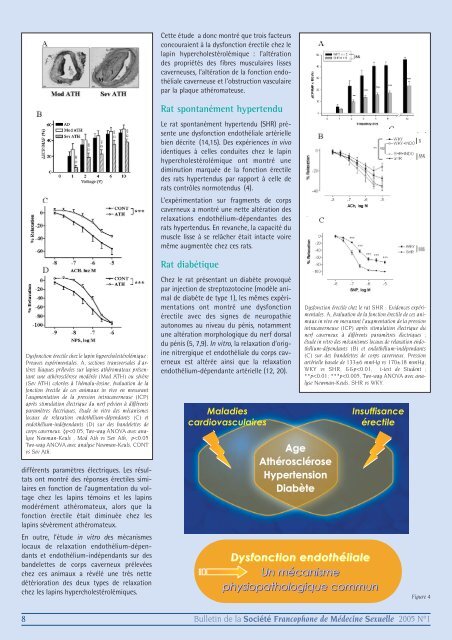
Cette étude a donc montré que trois facteursconcouraient à la dysfonction érectile chez lelapin hypercholestérolémique : l’altérationdes propriétés des fibres musculaires lissescaverneuses, l’altération de la fonction endothélialecaverneuse et l’obstruction vasculairepar la plaque athéromateuse.Rat spontanément hypertenduLe rat spontanément hypertendu (SHR) présenteune dysfonction endothéliale artériellebien décrite (14,15). Des expériences in vivoidentiques à celles conduites chez le lapinhypercholestérolémique ont montré unediminution marquée de la fonction érectiledes rats hypertendus par rapport à celle derats contrôles normotendus (4).L’expérimentation sur fragments de corpscaverneux a montré une nette altération desrelaxations endothélium-dépendantes desrats hypertendus. En revanche, la capacité dumuscle lisse à se relâcher était intacte voiremême augmentée chez ces rats.Dysfonction érectile chez le lapin hypercholestérolémique :Preuves expérimentales. A, sections transversales d’artèresiliaques prélevées sur lapins athéromateux présentantune athérosclérose modérée (Mod ATH) ou sévère(Sev ATH) colorées à l’hémalu-éosine, évaluation de lafonction érectile de ces animaux in vivo en mesurantl’augmentation de la pression intracaverneuse (ICP)après stimulation électrique du nerf pelvien à différentsparamètres électriques, étude in vitro des mécanismeslocaux de relaxation endothélium-dépendants (C) etendothélium-indépendants (D) sur des bandelettes decorps caverneux. §p
ConclusionLa dysfonction endothéliale semble être unmécanisme physiopathologique communassocié à l’insuffisance érectile et au diabète, àl’hypertension et à l’athérosclérose (figure 4).Cette dysfonction endothéliale pourrait alorsêtre une cible thérapeutique idéale notammentpour traiter l’IE d’origine vasculaire.Les stratégies thérapeutiques potentiellessont nombreuses. Le traitement peut visersoit la cellule endothéliale en augmentant labiodisponibilité du NO (inhibiteurs de l’enzymede conversion, antagonistes des récepteursà l’angiotensine II, Antagonistes calciques,antioxydants, supplémentation enarginine/tétrahydrobioptérine, antagonistesTxA2/PGH2, …), soit la cellule musculaire lisseen augmentant la réponse au NO, notammenten inhibant les phosphodiestérases de type 5.L’apport de NO exogène (donneurs de NO) oula stimulation de la relaxation NO-indépendante(activateurs de guanylate cyclase)représentent d’autres possibilités.Références1. Andersson K.E. & Wagner G. Physiology of penileerection. Physiol Rev., 1995, 75 : 191-236.2. Bacon C.G., Hu F.B., Giovannucci E., Glasser D.B.,Mittleman M.A., & Rimm, E.B. Association of type andduration of diabetes with erectile dysfunction in a largecohort of men. Diabetes Care, 2002, 25 : 1458-1463.3. Behr-Roussel D., Bernabé J., Compagnie S., RupinA., Verbeuren T.J., Alexandre L., & Giuliano F. Distinctmechanisms implicated in atherosclerosis-inducederectile dysfunction in rabbits. Atherosclerosis, 2002,162 : 355-362.4. Behr-Roussel D., Chamiot-Clerc P., Bernabe J.,Mevel K., Alexandre L., & Giuliano F. Erectile dysfunctionin spontaneously hypertensive rats: pathophysiologicalmechanisms. Am J Physiol Regul Integr CompPhysiol, 2003, 284 : R682-R688.5. Cellek S., Rodrigo J., Lobos E., Fernandez P., SerranoJ., & Moncada S. Selective nitrergic neurodegenerationin diabetes mellitus. Br.J.Pharmacol., 1999, 128 :1804-1812.6. Christ G.J. The penis as a vascular organ. Theimportance of corporal smooth muscle tone in thecontrol of erection. Urol.Clin.North Am., 1995, 22 :727-745.7. Escrig A., Marin R., Abreu P., Gonzalez-Mora J.L., &Mas M. Changes in mating behavior, erectile function,and nitric oxide levels in penile corpora cavernosain streptozotocin-diabetic rats. Biol.Reprod.,2002, 66 : 185-189.8. Feldman H.A., Goldstein I., Hatzichristou D.G., KraneR.J., & McKinlay J.BImpotence and its medical andpsychosocial correlates: results of the MassachusettsMale Aging Study. J Urol, . 1994, 151 : 54-61.9. Felten D.L., Felten S.Y., & Melman A. Noradrenergicinnervation of the penis in control and streptozotocin-diabeticrats: evidence of autonomic neuropathy.Anat.Rec., 1983, 206 : 49-59.10. Giuliano F., Chevret-Measson M., Tsatsaris A.,Reitz C., Murino M., & Thonneau P. Prevalence oferectile dysfunction in France: results of an epidemiologicalsurvey of a representative sample of 1004men. Eur.Urol., 2002, 42 :382-389.11. Jensen J., Lendorf A., Stimpel H., Frost J., Ibsen H.,& Rosenkilde P. The prevalence and etiology of impotencein 101 male hypertensive outpatients. Am.JHypertens., 1999, 12 : 271-275.12. Keegan A., Cotter M.A., & Cameron N.E. Effects ofdiabetes and treatment with the antioxidant alphalipoicacid on endothelial and neurogenic responses ofcorpus cavernosum in rats. Diabetologia, 1999, 42 :343-350.13. Klein R., Klein B., & Lee K. Prevalence of selfreportederectile dysfunction in people with longtermIDDM. Diabetes Care, 1996, 19 : 135-141.14. Koga T., Takata Y., Kobayashi K., Takishita S.,Yamashita Y., & Fujishima M. Age and hypertensionpromote endothelium-dependent contractions toacetylcholine in the aorta of the rat. Hypertension,1989, 14 : 542-548.15. Kung C.F. & Luscher T.F. Different mechanisms ofendothelial dysfunction with aging and hypertensionin rat aorta. Hypertension, 1995, 25 : 194-200.16. Lewis R.W., Hatzichristou D.G., Laumann E., &McKinlay J.B. Epidemiology and natural history oferectile dysfunction; risk factors including iatrogenicand aging. Proceedings of the First InternationalConsultationn on Erectile Dysfunction (ed. by A.jardin, A. H. Wagner, S. Khoury, F. Giuliano, H. Padma-Nathan, & M. Rosen), 2000, 21-51. Health PublicationLtd, Plymouth.17. Melman A. & Gingell J.C. The epidemiology andpathophysiology of erectile dysfunction. J.Urol.,1999, 161 : 5-11.18. Ruben A. & Babbott D. Impotence in diabetesmellitus. JAMA, 1958, 168 : 498.19. Solomon H., Man J.W., & Jackson G. Erectile dysfunctionand the cardiovascular patient: 20.endothelial dysfunction is the common denominator.Heart, 2003, 89 : 251-253.20. Taylor P.D. & Poston L. The effect of hyperglycaemiaon function of rat isolated mesenteric resistanceartery. Br.J.Pharmacol., 1994, 113 : 801-808.21. Wei M., Macera C.A., Davis D.R., Hornung C.A.,Nankin H.R., & Blair S.N. Total cholesterol and highdensity lipoprotein cholesterol as important predictorsof erectile dysfunction. Am J Epidemiol, 1994,140 : 930-937.Les troubles mictionnels (LUTS) en rapportavec une hypertrophie bénigne dela prostate (HBP) et la dysfonctionérectile (DE) ont souvent été considéréscomme étant essentiellement associésavec l’âge et le vieillissement. Cependant, destravaux récents suggèrent une étiologie enpartie commune de ces deux affections, indépendammentde l’âge (1).EpidémiologieHYPERTROPHIE BÉNIGNE DE LA PROSTATEET DYSFONCTION ÉRECTILE : PLUS QU’UNE SIMPLE COINCIDENCERécemment, une large étude internationale(MSAM-7 – Multinational Survey of theAging Male) (2) a mis en évidence, chez 14000 hommes entre 50 et 79 ans, que lestroubles urinaires (LUTS) en rapport avecl’HBP sont un facteur de risque pour la dysfonctionérectile, indépendamment de l’âgeet d’autres facteurs de risques importants.De plus, cette même étude (MSAM-7) a égalementdémontré que plus de 60% de ceshommes se plaignaient de troubles de l’éjaculationdont la prévalence était presque égaleà celle de la dysfonction érectile. Il existait,après stratification pour l’âge, une relationlinéaire entre l’importance des troubles urinaires(score IPSS) et l’importance de la dysfonctionérectile (score IIEF) et des troubleséjaculatoires.PathophysiologieLe lien entre troubles mictionnels et dysfonctionérectile est soutenu par différentes théories :Théorie du NO (monoxyded’azote ou oxyde nitrique) :Une production diminuée de NO/NOS dans lepetit bassin atteint la prostate et les structurespéniennes (3). Le rôle du NO est bienClaude SchulmanCliniques Universitaires de Bruxelles,Service d’Urologie, Hôpital Erasme,route de Lennik 808, B-1070 Bruxelles,Belgique, Claude.Schulman@ulb.ac.beaccepté comme mécanisme moléculaire debase dans la dysfonction érectile. La productionde NO/NOS dans la prostate est diminuéedans la zone de transition correspondant àl’hypertrophie adénomateuse bénigne lorsqu’onla compare à des tissus prostatiquesnormaux. En effet, les isoenzymes phosphodiestérase(PDE) type 4 et 5 sont présentesdans la prostate, ainsi que l’enzyme PDE11A.Cette théorie unifiée par le NO peut expliquerle lien entre les deux affections (4, 5, 6).Système nerveux autonome :Une hyperactivité du système nerveux autonomesympathique est associée aux troublesBulletin de la Société Francophone de Médecine Sexuelle 2005 N°1 9