28Secti<strong>un</strong>ea 2. Protectia si inginerie mediuluiCom<strong>un</strong>icari orale1. RECUPERAREA VANADIULUI DIN CENUŞI PETROLIERE UTILIZÂNDTEHNICI SOL-GELAlexandrescu LygiaUniversitatea Spiru Haret, Str. Ion Ghica nr. 13, Sector 3, BucureştiPrincipalul scop al prezentului studiu <strong>este</strong> de a evalua fezabilitatea practică a recuperăriivanadiului din cenuşi de origine petrolieră, utilizând o metodă nouă. Această cale derecuperare a <strong>un</strong>ui metal greu din cenuşa rezultată prin combustia reziduurilor petroliere, a foststudiată printr-o metodă alcătuită din două etape: tratamentul hidrometalurgic al cenuşei învederea aducerii în soluţie a ionilor de vanadiu existenţi în materialul de analizat, urmat de <strong>un</strong>proces de chelare a acestora cu o serie de liganzi imobilizaţi în matricea <strong>un</strong>ui sol-gel.Au fost preparate sol-gel-uri conţinând ca liganzi grupări de acid iminodiacetic,imidazol, acid etilendiaminotetracetic şi polietilen imină, <strong>care</strong> ulterior au fost folosite înstudierea adsorbţiei şi desorbţiei ionilor de vanadiu. Abilitatea acestor liganzi de a formacomplecşi prin intermediul ionilor de vanadiu a fost investigată atât prin procedura batch, cât şipe coloană, iar pentru analiza vanadiului din probe s-a folosit spectroscopia de absorbţieatomică.Adsorbţia vanadiului în ac<strong>este</strong> geluri siliconice modificate a fost analizată în f<strong>un</strong>cţie depH, de concentraţia ionilor de vanadiu şi de tăria ionică a soluţiilor apoase. A fost studiată deasemenea cinetica acestui proces de recuperare a vanadiului şi s-a constatat că aceastăadsorbţie urmăreşte modelul izotermei Langmuir.Capacităţile de adsorbţie ale sol-gel-urilor folosite au variat între 3,8 şi 6,5 mg V/g solgel,în f<strong>un</strong>cţie de ligandul folosit. Sol-gel-ul în <strong>care</strong> a fost imobilizat vanadiul a trecut apoiprintr-<strong>un</strong> proces cantitativ de desorbţie, în urma căruia s-a recuperat între 82 şi 100% vanadiu,făcând astfel posibilă refolosirea matricei de sol-gel.Bibliografie:-Alexander, J., Vanadium and Some of Its Industrial Applications, Chemistry and Industry 49, 871-887, 1992.-Nriagu, J., Vanadium in the Environment, pt.1: Chemistry and Biochemistry, Wiley Series, New York 1998.-Conway, M., Selecting and Using Chelating Ligands, Chemical Engineering, March, 86-90-, 1999.-Aelion, R., Loebel, A., Eirich, F., The Chemistry of the Silica, Wiley-New York, 1989.
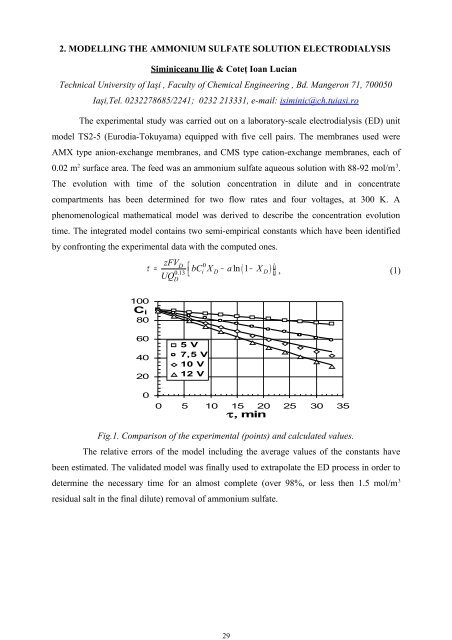
292. MODELLING THE AMMONIUM SULFATE SOLUTION ELECTRODIALYSISSiminiceanu Ilie & Coteţ Ioan LucianTechnical University of Iaşi , Faculty of Chemical Engineering , Bd. Mangeron 71, 700050Iaşi,Tel. 0232278685/2241; 0232 213331, e-mail: isiminic@ch.tuiasi.roThe experimental study was carried out on a laboratory-scale electrodialysis (ED) <strong>un</strong>itmodel TS2-5 (Eurodia-Tokuyama) equipped with five cell pairs. The membranes used wereAMX type anion-exchange membranes, and CMS type cation-exchange membranes, each of0.02 m 2 surface area. The feed was an ammonium sulfate aqueous solution with 88-92 mol/m 3 .The evolution with time of the solution concentration in dilute and in concentratecompartments has been determined for two flow rates and four voltages, at 300 K. Aphenomenological mathematical model was derived to describe the concentration evolutiontime. The integrated model contains two semi-empirical constants which have been identifiedby confronting the experimental data with the computed ones.τ zFVD0= ⎡ bC ln0.13 i X D − a ( 1 − X D ) ůUQ ⎣ű , (1)D100C i8060402005 V7,5 V10 V12 V0 5 10 15 20 25 30 35τ, minFig.1. Comparison of the experimental (points) and calculated values.The relative errors of the model including the average values of the constants havebeen estimated. The validated model was finally used to extrapolate the ED process in order todetermine the necessary time for an almost complete (over 98%, or less then 1.5 mol/m 3residual salt in the final dilute) removal of ammonium sulfate.