CHEMIE
CHEMIE
CHEMIE
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Chemie für Bauingenieure Block 1 ETHZ – BAUG – HS2011<br />
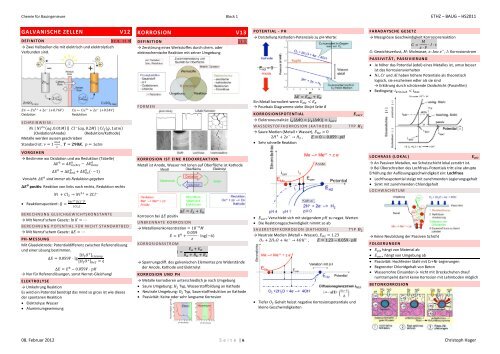
GALVANISCHE ZELLEN V12<br />
DEF IN IT O N 12. 8 , 12. 9<br />
→ Zwei Halbzellen die mit elektrisch und elektrolytisch<br />
Verbunden sind.<br />
( ) ( )<br />
Oxidation Reduktion<br />
SCHR EIBWEIS E:<br />
| ( ) ‖ ( ) | ( )<br />
(Oxidation/Anode) (Reduktion/Kathode)<br />
Metalle werden aussen geschrieben<br />
Standard ist:<br />
,<br />
VO RG EHEN<br />
→ Bestimme wo Oxidation und wo Reduktion (Tabelle)<br />
( )<br />
Vorsicht: sind immer als Reduktion gegeben<br />
positiv: Reaktion von links nach rechts, Reduktion rechts<br />
Reaktionsquotient:<br />
[ ][ ]<br />
[ ]<br />
BERECH NUNG G LEIC HG EW IC HTS K O NS TA NT E<br />
→ Mit Nernst’schem Gesetz:<br />
BERECH NUNG POT E NTIAL FÜR NIC HT STA NDARTB E D<br />
→ Mit Nernst’schem Gesetz:<br />
PH-MESSU NG<br />
Mit Glaselektrode: Potentialdifferenz zwischen Referenzlösung<br />
und einer Lösung bestimmen.<br />
[ ]<br />
[ ]<br />
→ Nur für Referenzlösungen, sonst Nernst-Gleichung!<br />
ELEK TROL Y SE<br />
→ Umkehrung Reaktion<br />
Es wird ein Potential benötigt das mind so gross ist wie dieses<br />
der spontanen Reaktion<br />
Elektrolyse Wasser<br />
Aluminiumgewinnung<br />
KORROSION V13<br />
DEF IN IT ION 13. 5<br />
→ Zerstörung eines Werkstoffes durch chem. oder<br />
elektrochemische Reaktion mit seiner Umgebung<br />
FORM E N<br />
KORR O SION IST E INE R EDOXREAK TION<br />
Metall ist Anode, Wasser mit Ionen auf Oberfläche ist Kathode<br />
Korrosion bei positiv<br />
U NBKENNATE K ORR OSI ON<br />
→ Metallionenkonzentration<br />
KORR OSI ONSS TR OM<br />
( )<br />
→ Spannungsdiff. des galvanischen Elementes pro Widerstände<br />
der Anode, Kathode und Elektrolyt<br />
KORR O SION UND PH<br />
→ Metalle korrodieren unterschiedlich je nach Umgebung<br />
Saure Umgebung: Typ, Wasserstoffbildung an Kathode<br />
Neutrale Umgebung: Typ, Sauerstoffreduktion an Kathode<br />
Passivität: Keine oder sehr langsame Korrosion<br />
POT E NTIAL - PH<br />
→ Darstellung Kathoden-Potenziale zu pH-Werte:<br />
Ein Metall korrodiert wenn<br />
→ Pourbaix Diagramme siehe Skript Seite 8<br />
KORR O SIONSP OTENT IAL<br />
→ Elektroneutralität: ( ) | ( )|<br />
WASSERS T OFFKORR OSI O N ( KATHODE) TY P<br />
→ Saure Medien (Metall + Wasser),<br />
Sehr schnelle Reaktion<br />
Verschiebt sich mit steigendem zu negat. Werten<br />
Die Reaktionsgeschwindigkeit nimmt so ab<br />
SAUERS T OFF K ORROSI ON (KA TH OD E) TY P<br />
→ Neutrale Medien (Metall + Wasser),<br />
Tiefer Gehalt heisst negative Korrosionspotentiale und<br />
kleine Geschwindigkeiten<br />
FARAD A YSC HE G E SET Z<br />
→ Messgrösse Geschwindigkeit Korrosionsreaktion<br />
: Gewichtsverlust, : Molmasse, Anz , Korrosionstrom<br />
PA SSIVIT ÄT, PA SSIVIERUN G<br />
Je höher das Potential (edel) eines Metalles ist, umso besser<br />
ist das Korrosionsverhalten<br />
und haben höhere Potentiale als theoretisch<br />
logisch, sie erscheinen edler als sie sind<br />
→ Erklärung durch schützende Oxidschicht (Passivfilm)<br />
Bedingung:<br />
LOCHRASS (L OKAL )<br />
→ An Passiven Metallen, wo Schutzschicht lokal zerstört ist.<br />
→ Bei Überschreiten des Lochfrass-Potentials tritt eine abrupte<br />
Erhöhung der Auflösungsgeschwindigkeit ein: Lochfrass<br />
Lochfrasspotential steigt mit zunehmenden Legierungsgehalt<br />
Sinkt mit zunehmenden Chloridgehalt<br />
LOC HWAC HSTUM<br />
→ Keine Neubildung der Passiven Schicht<br />
FOLG ERU NG E N<br />
hängt von Material ab<br />
hängt von Umgebung ab<br />
Passivität: Hochfester Stahl mit Cr+Ni-Legierungen<br />
Begrenzter Chloridgehalt von Beton<br />
Wasserrohre Einsanden (+ nicht mit Dreckschuhen drauf<br />
rumtrampeln) damit keine Korrosion mit Lehmboden möglich<br />
BETONK ORR O SIO N<br />
08. Februar 2012 S e i t e | 6 Christoph Hager