Hidrocarburos alicÃclicos Hidrocarburos alicÃclicos
Hidrocarburos alicÃclicos Hidrocarburos alicÃclicos
Hidrocarburos alicÃclicos Hidrocarburos alicÃclicos
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Hidrocarburos</strong><br />
alicíclicos<br />
clicos<br />
<strong>Hidrocarburos</strong> alicíclicos<br />
clicos<br />
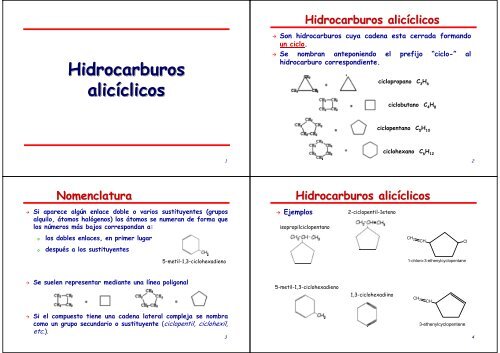
Son hidrocarburos cuya cadena esta cerrada formando<br />
un ciclo.<br />
Se nombran anteponiendo el prefijo “ciclo-” al<br />
hidrocarburo correspondiente.<br />
s<br />
ciclopropano C 3<br />
H 6<br />
ciclobutano C 4<br />
H 8<br />
ciclopentano C 5<br />
H 10<br />
ciclohexano C 6<br />
H 12<br />
1<br />
2<br />
Nomenclatura<br />
<strong>Hidrocarburos</strong> alicíclicos<br />
clicos<br />
<br />
Si aparece algún enlace doble o varios sustituyentes (grupos<br />
alquilo, átomos halógenos) los átomos se numeran de forma que<br />
los números más bajos correspondan a:<br />
Ejemplos<br />
isopropilciclopentano<br />
2-ciclopentil-1eteno<br />
o<br />
o<br />
los dobles enlaces, en primer lugar<br />
después a los sustituyentes<br />
CH 2<br />
CH<br />
Cl<br />
5-metil-1,3-ciclohexadieno<br />
1-chloro-3-ethenylcyclopentane<br />
<br />
Se suelen representar mediante una línea poligonal<br />
5-metil-1,3-ciclohexadieno<br />
1,3-ciclohexadiino<br />
CH 2<br />
CH<br />
<br />
Si el compuesto tiene una cadena lateral compleja se nombra<br />
como un grupo secundario o sustituyente (ciclopentil, ciclohexil,<br />
etc.).<br />
3<br />
3-ethenylcyclopentene<br />
4
Cicloalcanos. conformaciones<br />
Ejemplos de hidrocarburos:<br />
butano<br />
metilpropano<br />
ciclopropano<br />
ciclohexano<br />
eteno o<br />
etileno<br />
etino o acetileno<br />
2-etil-1-penteno<br />
3,5-dimetil-1-octino<br />
Ciclohexano<br />
conformación “silla”<br />
Ciclohexano<br />
conformación “bote”<br />
5<br />
1,3,5-ciclohexatrieno<br />
benceno<br />
naftaleno<br />
6<br />
<strong>Hidrocarburos</strong> alicíclicos<br />
clicos<br />
<strong>Hidrocarburos</strong> alicíclicos<br />
clicos<br />
Ejercicio I:<br />
1-etil-2-metil-ciclohexano<br />
1,2-ciclopentadien-4-ino<br />
Ejercicio II<br />
3-metilciclopropeno<br />
4-metilciclopenteno<br />
3,3-dimetilciclohexeno<br />
1,3-ciclohexadien-5-ino<br />
2-etil-1,4-dimetilciclohexano<br />
1,3,5-trimetilciclohexano<br />
1,1,2-trimetilciclobutano<br />
1,1,3,3-tetrametilciclopentano<br />
4-etil-1,2-dimetilciclohexano<br />
isopropilciclopentano<br />
2-etil-1,1-dimetilciclopentano<br />
1-etil-1,3-ciclobutadieno<br />
ciclopentino<br />
7<br />
8
Principios de Química Orgánica<br />
Páginas web interesantes para este tema:<br />
o http://www.juntadeandalucia.es/averroes/html/adjuntos/2007/09/24/0005/main<br />
.htm<br />
o http://www.quimicaorganica.net/index.htm<br />
o http://rabfis15.uco.es/weiqo/Tutorial_weiqo/index.htm<br />
o http://www.uam.es/departamentos/ciencias/qorg/docencia_red/qo/l00/lecc.html<br />
Derivados<br />
halogenados:<br />
Halogenuros de alquilo<br />
9<br />
10<br />
Halogenuros de alquilo<br />
Son compuestos que se forman por la sustitución de uno o más<br />
hidrógenos de los hidrocarburos por halógenos como el flúor,<br />
bromo, cloro o yodo.<br />
Su representación es R – X donde la R representa un radical<br />
alquilo y la X al halógeno.<br />
Ejemplos:<br />
CH 3 - CH – CH 3 Br - CH 2 -CH 2 -CH -CH 3<br />
Cl<br />
2-cloro-propano 1-bromo-3-cloro-butano<br />
Cl<br />
Nomenclatura<br />
En el sistema IUPAC se emplean los prefijos flúor, cloro,<br />
bromo o yodo, unidos al nombre básico del hidrocarburo,<br />
indicando la posición mediante un número que se antepone al<br />
nombre.<br />
Por ejemplo:<br />
Br - CH 2 -CH 2 -CH 3<br />
CH 3 -CH -CH 2 -CH 3<br />
1-bromo-propano 2-yodo-butano<br />
CH 3 - CH - CH 2 -CH –CH 3<br />
F CH 3<br />
2-flúor-4-metil-pentano<br />
I<br />
11<br />
12
Nomenclatura II<br />
Tradicionalmente los halogenuros de alquilo simples se<br />
nombran generalmente de acuerdo con el sistema común<br />
de las sales binarias. Se emplea el nombre del anión<br />
derivado del halógeno (cloruro, bromuro, fluoruro o<br />
yoduro), seguido del nombre del grupo alquilo (RADICAL).<br />
CH 3 -CH 2 - Br CH 3 -I<br />
bromuro de etilo yoduro de metilo<br />
CH 3 - CH - CH 2 -CH 3<br />
Cl<br />
cloruro de secbutilo<br />
Propiedades físicas<br />
La mayoría de los R-X son líquidos a temperatura ambiente<br />
con excepción de tres “halometanos” (cloro, bromo o<br />
flúormetano) los cuales son gases.<br />
Sus puntos de ebullición son más altos comparados con los<br />
hidrocarburos de peso molecular semejante. (presentan<br />
fuerzas intermoleculares –van der waals, puentes de<br />
hidrógeno- más intensas)<br />
Son insolubles en agua.<br />
Los yoduros y bromuros de alquilo son más densos que el agua<br />
y los cloro y flúoralcanos son menos densos que el agua.<br />
13<br />
14<br />
Importancia y aplicaciones de los R-X<br />
Diapositiva 16<br />
R1<br />
El DDT (Dicloro Difenil Tricloroetano) o más exactamente 1,1,1-tricloro-2,2-bis(4-clorofenil)-etano<br />
Ruben; 03/09/2010<br />
<br />
Todos los halogenuros de alquilo son potencialmente tóxicos y<br />
cancerígenos, la exposición durante períodos prolongados puede<br />
causar daños al hígado (hepatitis) y disolver los lípidos que<br />
protegen la piel originando una forma de dermatitis.<br />
Son materia prima para la obtención de alcoholes.<br />
Anestésicos (cloroformo (CHCl 3 ), cloruro de etilo -anestésico local-).<br />
Insecticidas, pesticidas y repelentes de polillas (DDT).<br />
Disolventes (cloroformo -triclorometano o tricloruro de metilo-,<br />
diclorometano, etc.).<br />
R<br />
Refrigerantes y aerosoles. (Clorofluorocarburos (freones) -<br />
CF 2 CCl 2 ó actualmente el CHClF 2 -, ¿recordáis el agujero de la capa de<br />
Ozono)<br />
16
Importancia y aplicaciones de los R-X<br />
Halogenuros de alquilo<br />
WIKIPEDIA:<br />
El DDT (Dicloro Difenil Tricloroetano) o más exactamente 1,1,1-tricloro-2,2-<br />
bis(4-clorofenil)-etano , de fórmula (ClC6H4)2CH(CCl3) es un compuesto<br />
organoclorado principal de los insecticidas. Es incoloro y cristalino. Es muy<br />
soluble en las grasas y en disolventes orgánicos, y prácticamente insoluble<br />
en agua. Su peso molecular es de 354 g/mol<br />
Ejercicio I:<br />
cloroetano<br />
3-cloro-1,4-hexadieno<br />
2,3-dicloro-2-buteno<br />
En el siglo XX fue utilizado con intensidad<br />
como insecticida pero, tras una campaña<br />
mundial que alegaba que este compuesto se<br />
acumulaba en las cadenas tróficas y ante el<br />
peligro de contaminación de los alimentos,<br />
se prohibió su uso.<br />
3-metil-2-yodopentano<br />
3,4-dicloro-1-pentino<br />
3,4-dibromo-1-penteno<br />
1-bromo-1-cloro-4-metil-2-hexeno<br />
17<br />
18<br />
<strong>Hidrocarburos</strong> Aromáticos<br />
Compuestos<br />
orgánicos que tienen una relación<br />
estructural y química con el benceno (C 6 H 6 )<br />
<strong>Hidrocarburos</strong> Aromáticos<br />
El benceno es un compuesto gaseoso a temperatura<br />
ambiente con una fomula molecular C 6 H 6<br />
H<br />
H<br />
C<br />
C<br />
H<br />
C<br />
H<br />
C<br />
C<br />
C<br />
H<br />
H<br />
Históricamente el nombre genérico<br />
de aromáticos<br />
a estos<br />
compuestos está asociado a sus intensos olores<br />
Un compuesto aromático:<br />
Es Cíclico<br />
Presenta dobles enlaces conjugados<br />
Friedich Kelulé en en 1865 propuso una estructura<br />
cíclica hexagonal con 3 dobles enlaces alternados.<br />
Presenta resonancia (movimiento de dobles enlaces) 19<br />
20<br />
H<br />
H<br />
C<br />
H<br />
C<br />
C<br />
C<br />
C<br />
H<br />
C<br />
H<br />
H<br />
Estructuras de Kelulé<br />
Las dos estructuras son igualmente válidas ¿los dobles<br />
enlace se mueven
El benceno<br />
Fórmula (empírica): C 6 H 6<br />
La molecula de benceno presenta una especial estabilidad en<br />
comparación con otros hidrocarburos insaturados<br />
La longitud de enlace entre carbonos es 1,4Å valor intermedio<br />
entre el la de los enlaces simples (1,53 Å) y la de los dobles enlaces<br />
(1,33Å)<br />
Todos los átomos de carbonos son exactamente equivalentes<br />
En las primeras teorías del enalce químico se considera que el<br />
benceno tiene una estructura plana cíclica con tres dobles enlaces<br />
alternados que presentan resonancia (existe resonancia o mesomería<br />
-Linus Pauling en el año 1928-) los dobles enlaces “se desplazan”<br />
El benceno<br />
Se considera que La estructura “real” es una combinación (mezcla)<br />
de las dos estructuras de resonancia<br />
Cuantas más formas resonantes tenga una molécula mayor será su<br />
estabilidad<br />
Actualmente se considera que cada carbono presenta Hibridación<br />
sp 2 (cada carbono tiene un orbital p). Se forman enlaces C-C por<br />
solapamiento sigma de orbitales sp 2<br />
Los orbitales p forman 3 enlaces deslocalizados por solapamiento<br />
π de los 6 orbitales p. Se forman dos anillos de densidad electrónica<br />
arriba y debajo del plano de la molécula, donde los 6 electrones p<br />
están deslocalizados.<br />
por la molécula.<br />
21<br />
22<br />
El benceno<br />
El benceno<br />
Nube “”común<br />
H<br />
C<br />
H<br />
C<br />
H<br />
C<br />
H<br />
C<br />
H<br />
C<br />
C<br />
H<br />
H<br />
C<br />
C<br />
H<br />
C<br />
H<br />
C<br />
H<br />
C<br />
H<br />
C<br />
H<br />
Esqueleto “”<br />
Hibridación sp 2 del benceno. Nube electrónica “”<br />
Imagen cedida por © Ed. ECIR. Química 2º Bachillerato.<br />
H H<br />
C C<br />
H C C H =<br />
C C<br />
H H<br />
23<br />
24
Benceno<br />
Compuestos aromáticos<br />
El benceno es un sistema cíclico de 6 electrones π deslocalizados. Está<br />
formado por 6 carbonos con hibridación sp 2 cuyos orbitales p solapan<br />
formando una nube que permite la deslocalización de los electrones p y<br />
confiere al benceno una gran estabilidad.<br />
Para Para saber saber más más<br />
(sólo (sólo para para curiosos)<br />
Esta estructura es presente presente en otras moléculas que podemos<br />
identificar siguiendo las reglas de Hückel:<br />
25<br />
•Regla 1.- Un sistema aromático debe ser cíclico y plano (sin carbonos sp 3<br />
en el ciclo)<br />
•Regla 2.- Existe conjugación cíclica de los dobles enlaces.<br />
•Regla 3.- El número de electrones p del sistema aromático cumple la<br />
fórmula 4n+2, con n = 0, 1, 2, 3 ......<br />
26<br />
Nomenclatura<br />
Muchos de los hidrocarburos aromáticos tienen nombres<br />
comunes. Estos nombres comunes se emplean en la<br />
nomenclatura IUPAC como base para el sistema anular.<br />
<strong>Hidrocarburos</strong> Aromáticos (Benceno). Nomenclatura<br />
<br />
Cuando sobre el benceno existe un sustituyente, el hidrocarburo se<br />
nombra anteponiendo el nombre del radical, seguido de la palabra<br />
benceno. Ej: etilbenceno.<br />
CH 2<br />
CH 3<br />
CH 2<br />
CH 3<br />
Cuando el hidrocarburo aromático está sustituido, se debe<br />
nombrar el sustituyente y su posición (con número o letras) de<br />
acuerdo con las reglas básicas de la nomenclatura IUPAC.<br />
Como nombre base se emplea el nombre común de los<br />
hidrocarburos aromáticos. Por ejemplo:<br />
Cl<br />
1,2 dibromo benceno 1,4 dicloro benceno<br />
Br<br />
Br<br />
<br />
<br />
Cuando hay dos sustituyentes sobre el anillo:<br />
o combinación de localizadores: 1,2-, 1-3, 1,4-<br />
o mediante los prefijos o- (orto), m-(meta) y p-(para)-<br />
Ej: 1,2-dietilbenceno (o-dietilbenceno).<br />
CH 3<br />
CH 2<br />
Si el anillo bencenico está como sustituyente en una cadena principal<br />
(como radical), se denomina “grupo fenilo” y se nombra “fenil”<br />
RADICAL FENILO<br />
RADICAL BENCILO<br />
Cl 27<br />
28
Algunos derivados del benceno con nombre propio<br />
CH 3<br />
tolueno<br />
<br />
Algunos bencenos sustituidos<br />
se conocen más<br />
por su nombre común:<br />
OH<br />
COOH<br />
CHO<br />
CONH 2<br />
fenol<br />
ácido benzoico<br />
benzaldehído<br />
benzamida<br />
RADICAL BENCILO<br />
RADICAL FENILO 29<br />
30<br />
Nomenclatura<br />
Particularidades en la nomenclatura<br />
Ejemplos:<br />
Nombres: etil–benceno (o feniletano)<br />
Ejemplos<br />
Br<br />
Br<br />
puede nombrarse también:<br />
o-dibromobenceno<br />
CH 2 –CH 3<br />
32<br />
Cuando hay dos sustituyentes puede usarse los<br />
préfijos:<br />
o Si están en los carbonos 1 y 2 Orto (o)<br />
o Si están en los carbonos 1 y 3 meta- (m)<br />
o Si están en los carbonos 1 y 4 para- (p)<br />
Br<br />
NO 2<br />
H 3 C– CH 3<br />
meta-cloronitrobenceno<br />
(1cloro-3-nitrobenceno)<br />
p-dimetilbenceno (ó p-metiltolueno)<br />
31
Derivados del benceno<br />
Derivados del benceno<br />
H<br />
CH 3<br />
H<br />
H<br />
H<br />
C<br />
C<br />
C<br />
H<br />
H<br />
C<br />
C<br />
C<br />
H<br />
H<br />
C<br />
C<br />
C<br />
C<br />
C<br />
H<br />
H<br />
C<br />
C<br />
C<br />
H<br />
H<br />
C<br />
C<br />
C<br />
H<br />
H<br />
C<br />
C<br />
C<br />
C<br />
C<br />
H<br />
H<br />
H<br />
H<br />
H<br />
Benceno Tolueno Naftaleno<br />
34<br />
35<br />
<strong>Hidrocarburos</strong> Aromáticos (Benceno). Propiedades físicasf<br />
Benceno: Efectos sobre la salud<br />
Los hidrocarburos aromáticos son líquidos o<br />
sólidos a temperatura ambiente.<br />
Son no polares y solubles en solventes de baja<br />
polaridad como el hexano, y éter .<br />
Son menos densos que el agua.<br />
Respirar, inhalar, aspirar, inspirar o ingerir niveles de benceno<br />
muy altos puede causar la muerte, mientras que niveles bajos<br />
pueden causar somnolencia, mareo, alucinaciones, aceleración<br />
del latido del corazón o taquicardia, dolores de cabeza,<br />
migrañas, temblores, tiritar, confusión y pérdida del<br />
conocimiento. Comer o tomar altos niveles de benceno puede<br />
causar vómitos o acidez, irritación del estómago, úlceras<br />
estomacales, mareo, somnolencia o convulsiones; y en último<br />
extremo la muerte.<br />
La exposición de larga duración al benceno se manifiesta en la<br />
sangre. El benceno produce efectos nocivos en la médula de los<br />
huesos y puede causar una disminución en el número de glóbulos<br />
rojos, lo que conduce a anemia. El benceno también puede<br />
producir hemorragias y daños en el sistema inmunitario,<br />
aumentando así las posibilidades de contraer infecciones por<br />
inmunodepresión.<br />
36<br />
38
<strong>Hidrocarburos</strong> Aromáticos (Benceno)<br />
<br />
Ejercicio:<br />
etil–benceno<br />
CH 2 –CH 3<br />
1,2-dimetilbenceno<br />
1,3-dicloro-2-bromobenceno<br />
<strong>Hidrocarburos</strong> aromáticos<br />
Ejercicio II:<br />
1-isobutil-3-metilbenceno<br />
2-metilnaftaleno<br />
1,2,3,5-tetrametilbenceno<br />
p-dimetilbenceno<br />
(ó p-metiltolueno)<br />
Etenibenceno<br />
(vinilbenceno)<br />
1,2-dimetilbenceno<br />
1,4-dietilbenceno<br />
4-etil-2-metilantraceno<br />
H 3 C– CH 3<br />
o-dibromobenceno<br />
1-metil-2,3-dipropilbenceno<br />
Br<br />
Br<br />
1-metil-3-(1-propenil)benceno<br />
40<br />
2-etil-1,4-dimetilbenceno<br />
41<br />
<strong>Hidrocarburos</strong> aromáticos<br />
<strong>Hidrocarburos</strong> Aromáticos (Benceno)<br />
Ejercicio III:<br />
1-isobutil-3-metilbenceno<br />
tolueno<br />
<br />
Ejercicio:<br />
Antraceno<br />
1-metil-3-(1-propenil)benceno<br />
1,6-dimetilnaftaleno<br />
antraceno<br />
fenantreno<br />
fenantreno<br />
naftaleno<br />
1,3-dicloro-2-bromobenceno<br />
1,4-dibromociclohexano<br />
42<br />
43
<strong>Hidrocarburos</strong> Aromáticos<br />
Páginas web interesantes para este tema:<br />
o http://www.uhu.es/quimiorg/aromati1.html<br />
45