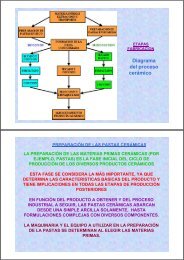
Leccion2.Ceramicas.MateriasPrimas.Presentacion.2011.2012
Leccion2.Ceramicas.MateriasPrimas.Presentacion.2011.2012
Leccion2.Ceramicas.MateriasPrimas.Presentacion.2011.2012
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
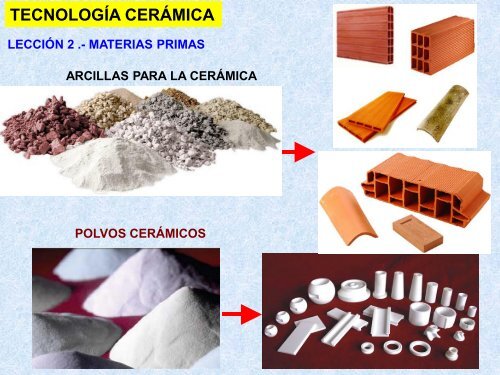
TECNOLOGÍA CERÁMICALECCIÓN 2 .- MATERIAS PRIMASARCILLAS PARA LA CERÁMICAPOLVOS CERÁMICOS
DEBIDO A SU ALTO PUNTO DE FUSIÓN LOS COMPONENTES CERÁMICOS NOPUEDEN SER FABRICADOS, EN GENERAL, POR LOS PROCESOS EN FASELIQUIDA QUE SE USAN PARA LOS METALES Y POLÍMEROSSU FABRICACIÓN SE EFECTÚA POR SINTERIZADO, ENTRANDO DE ESTE MODOEN EL ÁREA DE LA METALURGIA DE POLVOS
EXTRUSIÓN Y TORNEADO
LAS CATEGORÍAS DE MATERIAS PRIMAS INCLUYEN:(1).- MATERIAL CRUDO NO UNIFORME DE DEPÓSITOS NATURALESBall Clay is a variety of Kaolinite, like china-clay. It differs from china-clay in havinghigh plasticity and less refractoriness. In chemical composition, Ball clays usuallycontain three dominant minerals: from 20-80% kaolinite, 10-25% mica, and 6-65%quartz. In addition, there are other 'accessory' minerals and some carbonaceousmaterial (derived from ancient plants) present.BALL CLAY
(2).- MINERALES INDUSTRIALES QUE HAN SIDO BENEFICIADOS PARA QUITARIMPUREZAS CON EL FIN DE AUMENTAR CONSIDERABLEMENTE LA PUREZAMINERAL Y MEJORAR LAS CARACTERISTICAS FÍSICAS Y QUÍMICASFELDESPATO SÓDICOEl feldespato sódico principalmente actúacomo fundente produciendo a una menortemperatura el producto, sobre todo enmedia alta temperatura, para baja esnecesario reforzarlos con otros fundentes.Constituye el "cemento" entre las partículasde los demás componentes.Disminuye en productos porosos elcoeficiente de dilatación.
(3).- SUSTANCIAS QUÍMICAS INDUSTRIALES INORGÁNICAS, CON UN GRANTONELAJE DE PRODUCCIÓN, QUE HAN SUFRIDO UN PROCESADO QUÍMICOSIGNIFICATIVO Y UN REFINAMIENTO PARA MEJORAR CONSIDERABLEMENTELA PUREZA QUÍMICA Y MEJORAR LAS CARACTERÍSTICAS FÍSICAS.
PROCESO BAYER
(4).- SUSTANCIAS QUÍMICAS INORGÁNICAS ESPECIALESLOS NUEVOS Y POTENCIALES USOS DE LOS MATERIALES CERÁMICOS, ENLO QUE SE DENOMINA APLICACIONES DE ALTO RENDIMIENTO O DE ALTATECNOLOGÍA, HAN GENERADO MUCHO INTERÉS EN NUEVAS TÉCNICAS DEPREPARACIÓN DE POLVOS CERÁMICOS CON CARACTERÍSTICASESPECIALES, COMO SON:1.- PUREZAS SUPERIORES AL 99.9%2.- COMPOSICIÓN QUÍMICA REPRODUCIBLE, CONTROLADA CON GRANPRECISIÓN, INCLUYENDO SUSTANCIAS DOPANTES3.- HOMOGENEIDAD QUÍMICA A ESCALA ATÓMICA4.- TAMAÑO DE PARTÍCULAS INFERIOR A LA MICRA CONTROLADO CON GRANPRECISIÓN.POLVO DE CIRCONIARODAMIENTOS DE CIRCONIA
CERAMICAS TRADICIONALES // MATERIAS PRIMAS.PLÁSTICAS.ARCILLAS NATURALES DE UNA O MÁS VARIEDADES PARA PODERCONSEGUIR MEJORES PROPIEDADES.DESDE EL PUNTO DE VISTA MINERALÓGICO SU COMPOSICIÓN ESMAYORITARIAMENTE CAOLINITA CON MONTMORILLONITA COMOCOMPONENTE SUBORDINADO, SUELEN ACOMPAÑAR HALLOYSITA, ILLITA YPIROFILITA, ADEMÁS DE MINERALES NO ARCILLOSOS COMO:CUARZO, FELDESPATO, MICAS Y VIDRIO VOLCÁNICO.NO PLÁSTICAS.MATERIAS QUE SE AGREGAN A LAS ARCILLAS PARA:-DISMINUIR SU EXCESIVA PLASTICIDAD-REDUCIR LA RETRACCION AL SECARSE LA PASTA-REBAJAR SU TEMPERATURA DE COCCIÓN-AUMENTAR SU POROSIDAD-COLOREAR O RECUBRIR DE ESMALTE LAS PIEZAS.SE DEBEN AÑADIR FINAMENTE MOLIDASPARA NO QUITAR HOMOGENEIDAD.
NO PLÁSTICAS / DESGRASANTESMATERIALES ARENOSOS QUE:1.- REDUCEN LA EXCESIVA PLASTICIDAD DE ALGUNAS ARCILLAS2.- DISMINUYEN LA ADHERENCIA DE LAS ARCILLAS AL ESTAR HÚMEDAS, LO QUEDIFICULTA SU MANEJO Y MOLDEO.3.- AL SECARSE LA PASTA LA CONTRACCIÓN ES MENOR4.- ACTÚAN COMO ESQUELETO, ARMAZÓN O SOPORTE DE LA FORMA CERÁMICA, YAQUE AUNQUE ALGUNOS MATERIALES SE ABLANDEN PARA OBTENER UN DETERMINADOGRADO DE VITRIFICACIÓN, LA FORMA QUE SE DA AL PRODUCTO EN VERDE, HA DESOSTENERSE HASTA EL FINAL DEL PROCESO
NO PLÁSTICAS / DESGRASANTES- LA ARENA DE CUARZO (SiO 2 ) O ANHIDRIDO SILÍCICO, QUE PUEDE ESTARPRESENTE EN LA PROPIA ARCILLA O AÑADIRSE.AUMENTA DE VOLUMEN AL ELEVAR LA TEMPERATURA REDUCIENDO LACONTRACCIÓN DE LA PASTA AUNQUE UN CALENTAMIENTO BRUSCO PRODUCEUNA EXPANSIÓN VIOLENTA QUE PODRÍA ROMPER LA PIEZA.EL TAMAÑO DE PARTÍCULA DE LA SÍLICE ES IMPORTANTE. CUANDO EL TAMAÑODE PARTÍCULA ES PEQUEÑO PUEDE REACCIONAR Y ACTUAR COMO FUNDENTEY CUANDO EL TAMAÑO DE PARTÍCULA ES GRANDE, LA SÍLICE AUMENTA LAREFRACTARIEDAD.- EL FELDESPATO POTÁSICO, EL CUAL ADEMÁS DA TRANSPARENCIA A LASPORCELANAS Y LOZAS Y SIRVE TAMBIÉN PARA FABRICAR ESMALTES CERÁMICOS.- LA CHAMOTA O BARRO COCIDO ES EL MÁS UTILIZADO Y ECONÓMICO POR PROCEDERDE PIEZAS ROTAS O DEFECTUOSAS QUE SE PULVERIZAN AÑADIÉNDOSE A LA ARCILLAY NO SE CONTRAE AL VOLVERSE A COCER.- ESCORIA GRANULADA.EL DESGRASANTE IDEAL ES LA CHAMOTA, QUE SE ADICIONA EN CIERTA PROPORCIÓN ALA COMPOSICIÓN CRUDA, APORTANDO, PRINCIPALMENTE, LAS SIGUIENTES VENTAJAS:1.- REDUCE LAS MERMAS O CONTRACCIONES POR SECADO Y POR COCCIÓN, LO QUEAMINORA LAS TENSIONES INTERNAS Y EL RIESGO DE GRIETAS Y FISURAS.2.- APORTA MÁS RESISTENCIA MECÁNICA AL CUERPO CERÁMICO CRUDO.3.- AUMENTA LA FACILIDAD DE DRENAJE RESPECTO AL SECADO CERÁMICO.4.- MEJORA LA RESISTENCIA AL CHOQUE TÉRMICO.
NO PLÁSTICAS /FUNDENTESSE AÑADEN A LA PASTA PARA REDUCIR LA TEMPERATURA DE COCCIÓN, YAQUE BAJAN EL PUNTO DE FUSIÓN DEL MATERIAL, ABARATANDO COSTOS YPERMITIENDO LA VITRIFICACIÓN PARCIAL DE LAS PIEZAS.-CARBONATO CÁLCICO- CARBONATO CÁLCICO, QUE MUY FRECUENTEMENTE ES IMPUREZA DE LA ARCILLA, NOSIENDO NECESARIO AÑADIRLO. EL APORTE CALIZO ES SIN EMBARGO PERJUDICIALPARA LA PIEZA Y CONVIENE REDUCIRLO O MOLERLO FINAMENTE.LOS PRINCIPALES EFECTOS DE LOS MINERALES DE CALCIO EN LAS ARCILLASSON:-ACTÚAN COMO FUNDENTES YA QUE SE COMBINAN CON LA SÍLICE Y LA ALÚMINAPARA DAR EUTÉCTICOS DE BAJO PUNTO DE FUSIÓN Y POR TANTO REDUCEN LATEMPERATURA DE VITRIFICACIÓN Y LA REFRACTARIEDAD.- A TEMPERATURAS MENORES A LA DE REACCIÓN REDUCEN LA CONTRACCIÓN DELA ARCILLA Y FACILITAN EL SECADO.- LOS COMPUESTOS DE CALCIO, CUANDO SE COMBINAN CON MINERALES DEHIERRO, REDUCEN EL COLOR ROJO DE ESTOS ÚLTIMOS TRASLADÁNDOLO HACIAEL BLANCO.-EL CARBONATO CÁLCICO, CUANDO SE CALIENTA A 900 °C, SE CONVIERTE ENÓXIDO CÁLCICO QUE, SI PERMANECE SIN COMBINAR, EN EL ENFRIMIENTO PUEDEABSORBER HUMEDAD DEL AIRE, AUMENTAR DE VOLUMEN Y QUEBRAR O FISURARLA PIEZA.
NO PLÁSTICAS /FUNDENTES- FELDESPATO ALCALINOSEL OBJETIVO FUNDAMENTAL DE LOS FELDESPATOS EN LAS PASTASCERÁMICAS ES EL DE REBAJAR EL PUNTO DE FUSIÓN, LO QUE ES DE MÁXIMAIMPORTANCIA, TANTO DESDE EL PUNTO DE VISTA TÉCNICO COMOECONÓMICO, PRODUCIENDO LAS REACCIONES FUNDAMENTALES PARA LACONSTITUCIÓN DEL PRODUCTO CERÁMICO A UNA TEMPERATURA MÁS BAJA.SE FACILITAN ASÍ LAS COMBINACIONES SÍLICE-ALÚMINA PARA FORMAR LOSCOMPUESTOS QUE SE PRETENDE OBTENER, SIENDO CAPAZ LA MASA VÍTREAFELDESPÁTICA DE ASIMILAR UNA NOTABLE CANTIDAD DE SÍLICE, DEALÚMINA Y DE MULLITA.ENTRE 1300 °C Y 1400 °C SE PRODUCE LA DISOLUCIÓN DE TODA LA SÍLICE YSE SATURA DE MULLITA EN GRAN PARTE CRISTALIZADA.OBSERVANDO LA CURVA VISCOSIDAD-TEMPERATURA, SE APRECIA QUEMIENTRAS PREVALECE EL FELDESPATO POTÁSICO LA MASA VÍTREA SEMANTIENE MUY VISCOSA, INCLUSO A ALTA TEMPERATURA, MIENTRAS QUE SIPREDOMINA EL SÓDICO EL DESCENSO DE VISCOSIDAD CON EL AUMENTO DETEMPERATURA SE HACE MUY RÁPIDO. DE LA VISCOSIDAD DEPENDE LAPOSIBILIDAD DE DEFORMARSE MÁS O MENOS RÁPIDAMENTE POR ACCIÓNDEL PROPIO PESO, Y ES ESTE EL MOTIVO DE LA DIFICULTAD DEL USO DE LOSFELDESPATOS SÓDICOS EN LAS PASTAS VITRIFICADAS, COMO POR EJEMPLOLA PORCELANA.
NO PLÁSTICAS /FUNDENTES- SOSA Y POTASAEL PRINCIPAL EFECTO DE LOS ÁLCALIS PRESENTES EN LAS ARCILLAS ESREDUCIR LA REFRACTARIEDAD O TEMPERATURA DE VITRIFICACIÓN YA QUESE COMBINAN CON LA SÍLICE Y LA ALÚMINA PARA DAR FASES LÍQUIDAS ABAJA TEMPERATURA DE FUSIÓN (=700 °C)1713 ºC
NO PLÁSTICAS / MATERIALES QUEMANTESSE AÑADEN A LA PASTA CON EL FIN DE AUMENTAR LA POROSIDAD YFAVORECER LA SINTERIZACIÓN UNIFORME DE LA PASTA CERÁMICA.SE UTILIZAN MATERIALES ORGÁNICOS COMO EL SERRÍN O CARBÓN(LIGNITO), POLIESTIRENO EXPANDIDO, QUE AL QUEMARSE EN EL HORNO DANPIEZAS DE ALTA POROSIDAD Y POCO PESO.
LOS SILICATOS SON EL GRUPO DE MINERALES DE MAYOR ABUNDANCIA,PUES CONSTITUYEN MÁS DEL 95% DE LA CORTEZA TERRESTRE. TODOS LOSSILICATOS ESTÁN COMPUESTOS POR SILICIO Y OXÍGENO. ESTOS ELEMENTOSPUEDEN ESTAR ACOMPAÑADOS DE OTROS, ENTRE LOS QUE DESTACANALUMINIO, HIERRO, MAGNESIO, CALCIO, SODIO Y POTASIO.
LOS SILICATOS Y SU ESTRUCTURA.EN LUGAR DE CARACTERIZAR LAS ESTRUCTURAS CRISTALINAS DE ESTOSMATERIALES EN TÉRMINOS DE CELDILLAS UNIDAD, ES MÁS CONVENIENTEUTILIZAR VARIAS COMBINACIONES DE tetraedros de SiO 44-.Configuración electrónica Si: [Ne]3s 2 3p 2 → Hibridación sp 3SiO 44CADA ATOMO DE SILICIO ESTA UNIDO A CUATRO ÁTOMOSDE OXIGENO, LOS CUALES ESTÁN SITUADOS EN LOSVÉRTICES DEL TETRAEDRO. EL ÁTOMO DE SILICIO ESTACOLOCADO EN EL CENTROPUESTO QUE ESTA ES LA UNIDAD BÁSICA DE LOSSILICATOS, FRECUENTEMENTE SE CONSIDERA UNAENTIDAD CARGADA NEGATIVAMENTE (- 4).VCVA( CN) ( CN)C ( CN ) CVA( ) 4 xCN2A 2V 4CA
SEGÚN EL TIPO DE ESTRUCTURA, LOSSILICATOS PUEDEN DIVIDIRSE EN SEISGRUPOS DEPENDIENDO DEL NÚMERODE OXÍGENOS DEL TETRAEDRO DESILICIO QUE ESTÁN UNIDOSDIRECTAMENTE A OTROS TETRAEDROSDE SILICIO VECINOS (ES DECIR, SEGÚNEL NÚMERO DE VÉRTICESCOMPARTIDOS POR TETRAEDROS, QUEPUEDEN SER 0, 1, 2, 3, y 4):GRUPOS DE SILICATOS
ESTRUCTURA DE LOS SILICATOS
AISLADOSPAREJASANILLOSCADENAS PLANOS /SIMPLES DOBLES/LÁMINASARCILLASTRIDIMENSIONALCUARZO(Si 2 O 6 ) 4- (Si 4 O 11 ) 6- (Si 2 O 5 ) 2-
ESTRUCTURA CRISTALINA DEL CIRCÓNTURMALINAFórmula:(Na,Ca)(Li,Mg,Al) 3 (Al,Fe,Mn) 6 (BO) 3 (Si 6 O 18 )(OH) 4Estructura cristalina de turmalina. Los grupostriangulares planos BO3, perpendiculares al ejecristalográfico c, están coloreados en verde sonlos grupos. Los grupos OH están coloreados enazul. Li, Mg, Al están coloreados en rojo. Al,Fe3+, Mn3+ están coloreados en naranja. El Ca2+y el Na+ están coloreados en rosa.
RELACIÓN ENTRE LAESTRUCTURA DE LOSSILICATOS Y LAPROPORCIÓN O/SiLA MANERA MÁS SIMPLEDE DETERMINAR ELNÚMERO DE OXÍGENOSNO PUENTE POR Si, ESDIVIDIR LA CARGA DE LAUNIDAD QUE SE REPITEPOR EL NÚMERO DEÁTOMOS DE Si EN ELLA(Si 2 O 5 ) 2-
SÍLICE / ESTRUCTURA TRIDIMENSIONALLA SÍLICE, AISLADAMENTE O EN COMBINACIÓN CON OTROSÓXIDOS CERÁMICOS (FORMANDO LOS SILICATOS), REPRESENTAUNA GRAN FRACCIÓN DE LOS MATERIALES CERÁMICOSQUÍMICAMENTE, EL SILICATO MÁS SENCILLO ES EL DIÓXIDO DESILICIO, O SÍLICE (SiO 2 )ESTRUCTURALMENTE, ES UNA RED TRIDIMENSIONAL QUE SEGENERA CUANDO TODOS LOS ÁTOMOS DE OXIGENO DE CADATETRAEDRO SON COMPARTIDOS CON TETRAEDROS ADYACENTES
SÍLICESi todos los tetraedros se colocan de una forma regular y ordenada, seforma una estructura cristalina.Existen tres formas cristalinas polimórficas primarias de la sílice:CUARZO, CRISTOBALITA Y TRIDIMITA.Sus estructuras son relativamente complicadas, y comparativamenteabiertas, o sea, los átomos no están empaquetados al máximo. Comoconsecuencia, estas sílices cristalinas tienen densidades relativamentebajas. Por ejemplo, a temperatura ambiente, el cuarzo tiene una densidadde solo 2.65 g/cm 3 . La resistencia del enlace Si -O se refleja en unatemperatura de fusión relativamente alta, 1710 °C.OXIGENOSILICIO
(Si 2 O 5 ) 2-
FILOSILICATOS // ARCILLASLAS ARCILLAS SON “ROCAS” O MATERIALES TERROSOS FORMADASPRINCIPALMENTE POR ALUMINOSILICATOS HIDRATADOS CON MATERIACOLOIDAL Y TROZOS DE FRAGMENTOS DE ROCAS, QUE GENERALMENTESE HACEN PLÁSTICAS CUANDO ESTÁN HÚMEDAS Y PÉTREAS PORLA ACCIÓN DEL FUEGO.LA FABRICACIÓN TIENE SU FUNDAMENTO EN LA PLASTICIDAD OCAPACIDAD DE MOLDEO POR DEFORMACIÓN PLÁSTICA QUE TIENEN LASARCILLAS SEGÚN SU CONTENIDO DE AGUA. UNA VEZ CONFORMADAS LASPIEZAS, POR DESECACIÓN Y COCCIÓN SE PRODUCEN LASTRANSFORMACIONES IRREVERSIBLES QUE LE DAN CARÁCTER PÉTREO.ESTAS PROPIEDADES DAN A LAS ARCILLAS SU UTILIDAD, PUESTO QUE SELES PUEDE MOLDEAR EN CASI TODAS LAS FORMAS, LAS CUALESCONSERVAN DESPUÉS DE SER SOMETIDAS A LA ACCIÓN DEL FUEGO.
FILOSILICATOS. ARCILLASLOS ALUMINOSILICATOS HIDRATADOS POSEEN UNA ESTRUCTURA LAMINARO DE CAPAS Y SUELEN ESTAR ACOMPAÑADOS DE OTROS MINERALESDENOMINADOS “ACCESORIOS” ENTRE LOS QUE PODEMOS CITAR:CUARZO, CALCITA, ÓXIDOS Y SULFUROS DE HIERRO, YESO, RUTILO (TiO 2 ),ILMENITA (FeTiO 3 ), DOLOMITA, ÁLCALIS (QUE SE DERIVAN PRINCIPALMENTE DE LASMICAS Y FELDESPATOS, AUNQUE PARTE SE DEBE AL INTERCAMBIO CATIÓNICO DELAS PROPIAS ARCILLAS), MATERIA ORGÁNICA, ETC.Sustancias presentes en la naturaleza junto con la arcilla:- SO 4 Ca·2H 2 0 (piedra de yeso)- CaCO 3 (carbonato cálcico/calcita)- Fe(OH) 3 (hidróxido férrico)- Fe 2 O 3 (óxido férrico)- SiO 2 (cuarzo)- TiO 2 (rutilo)- FeTiO 3 (ilmenita)- FeS 2 (Pirita)- CaMg(CO 3 ) 2 (Dolomita)- Álcalis (que se derivan principalmente de las micas y feldespatos)- Materia orgánica
ESTRUCTURA DE LOS FILOSILICATOS1.- PLANOS CONSTITUIDOS POR ÁTOMOS, TALES COMO O Y OH2.-CAPAS, TETRAÉDRICAS U OCTAÉDRICAS, FORMADAS POR UNA COMBINACIÓN OAPILAMIENTO DE PLANOS3.- EL APILAMIENTO DE CAPAS DA LUGAR A LA FORMACION DE LAMINAS TO: BILAMINAR ,TOT: TRILAMINAR , TOTO: CLORITAS4.- CRISTAL, QUE ES EL RESULTADO DE UN APILAMIENTO DE LAMINAS EN LA DIRECCIÓNCRISTALOGRÁFICA c MAS EL ESPACIO INTERLAMINARCapa tetraédrica:Planos hexagonales ycompactos.Capa octaédrica:Planos compactosESTRUCTURAGENERAL DE LOSFILOSILICATOS
Capa compactaCada cavidad está limitadapor seis esferas y por ello aesta capa la vamos adenominar, "capa hexagonal"o "no compacta".El apilamiento de dos capas compactas, define agrupaciones de 6 esferas cuyosvértices forman un octaedro. Es la coordinación octaédrica o de 6 anionesEl apilamiento de una capa hexagonal y de una capa compacta, defineuna serie de agrupaciones de 4 esferas cuyos vértices forman untetraedro. Es la coordinación tetraédrica o de 4 aniones.El silicio y el aluminio pueden ocupar los puestos de coordinación tetraédrica(entre una capa hexagonal y una capa compacta), y el aluminio, magnesio y hierroson los que normalmente ocupan los puestos de coordinación octaédrica ( entredos capas compactas)
Estructura final correspondiente a la lámina 1:1Estructura final correspondiente a la lámina 2:1Las láminas de lasarcilla se originan porel apilamiento deplanos alternos deiones (O y OH) ycationes (Si 4+, Mg 2+ yAl 3+)
ESTRUCTURAGENERAL DE LOSFILOSILICATOSUnidades fundamentales de laestructura cristalina de losfilosilicatosCAPA TETRAÉDRICACAPA OCTAÉDRICA
Composición química de los minerales de la arcilla(O 2- ) y (OH) - son los aniones que formanparte de la estructura.En los huecos que forman sus apilamientosde planos, se sitúan los cationes, dedimensiones mucho menoresLa coordinación de cada catión estádeterminada por su radio iónico.- (Si) 4+ Ocupa huecos decoordinación tetraédrica.- (Al) 3+ Puede ocupar huecosoctaédricos ó sustituir al Si encoordinación tetraédrica.- (Mg) 2+ , (Fe) 2+ , (Fe) 3+ ... Ocupanhuecos de coordinación octaédrica- (K) + , (Na) + , (Ca) 2+ . Ocupanposiciones en el espacio interlaminar.Cationesintercambiables
ESTRUCTURA DE LOS FILOSILICATOSEstán constituidos por una capa indefinida de tetraedros que comparten tres desus vértices de forma que quedan en un mismo plano. Se presenta en forma deuna red hexagonal regular en la que la relación (Silicio/Oxigeno) es de 2/5.En el plano definido por el cuarto vértice de cada tetraedro se ubica ungrupo OH en el centro del hexagono definido por los oxígenos apicalestetraédricos.El tamaño del triángulo entre los dos oxígenos y un (OH) es aproximadamente elmismo (pero no idéntico a la cara triangular de un octaedro XO 6 (en donde X escomúnmente Mg o Al). Esto significa que es posible enlazar a una red regular deoxígenos apicales y grupos OH de composición (Si 2 O 5 OH) 3- una lámina deoctaedros regulares, donde cada octaedro está inclinado sobre uno de sus ladostriangulares
Así pues, en el plano definido por el cuarto vértice de cada tetraedro se ubica un grupo OHen el centro del hexágono definido por los oxígenos apicales tetraédricos. Este grupo OHy dos oxígenos del hexágono, forman un triángulo sobre el que se apoya un octaedrocuyos otros tres vértices se sitúan en un plano inferior, y están constituidos por gruposOH que pertenecen a una capa hexagonal centrada, o bien por un grupo OH y dosoxígenos, correspondientes a una capa tetraédrica análoga a la primera y situadaespecularmente con ella. Los huecos octaédricos pueden estar ocupados por Al o por MgInterlámina
Cuando el catión central de los octaedros es trivalente (Al3+) (Lámina octaédrica de alúmina, tipo gibbsita)sólo se necesita que dos tercios de los huecos centrales octaédricos estén ocupados para balancear lacapa eléctricamenteCuando el catión central es bivalente Mg 2+ , (Lámina octaédrica de óxido de magnesio, Mg(OH) 2 , tipobrucita) o Fe 2+ se necesita que todos los huecos centrales estén ocupados. En este último caso seproduce una mayor simetría en el reparto de las valencias con el silicio. Esta estructura puedeconsiderarse como derivada de la gibbsita por sustitución de 3 Mg 2+ por 2 Al 3+ .Capa ÁtomosValencia+ -Hexagonal 6 O 124 Si 16Compacta 4O-2OH 8 + 24 Al 12Compacta 6 OH 64 (O 2- )+2(OH) -LAMINA DIOCTAEDRICACapa ÁtomosValencia+ -Hexagonal 6 O 124 Si 16Compacta 4O-2OH 8 + 26 Mg 12Compacta 6 OH 6LAMINA TRIOCTAEDRICA
LA DIVISIÓN DE LOS FILOSILICATOS SE BASA EN TRES CRITERIOS:1.- Iones que ocupan la coordinación octaédrica.Dioctaédricos: con iones trivalentes, generalmente aluminioTrioctaédricos: con iones divalentes, por ejemplo magnesio2.- La existencia, o no, de sustituciones en las coordinaciones tetraédricas o/yoctaédricas y, en el caso de existencia de las mismas, la forma de compensación deeste déficit de carga.3.- El espesor de las hojas y las fuerzas de ligazón entre las mismas.CON RESPECTO A ESPESOR, SE DISTINGUEN TRES TIPOS DISTINTOS:Tipo de 7Å (Te-Oc):Hoja formada por tres capas, una hexagonal de O y dos compactas, una de O y(OH) y otra de (OH).CaolinitaSerpentina6 O 6 O4 Si 4 Si4O - 2OH4O - 2OH4 Al 6 Mg6 OH 6 OHSi 4O 10Al 4(OH) 8Si 4O 10Mg 6(OH) 8
Tipo de 1OÅ (Te-Oc-Te):Hoja formada por cuatro capas, 2 compactas de O y (OH) encerradas, amodo de bocadillo, entre dos capas hexagonales de O.PirofillitaMuscovitaK6 O 6 OKKSi9,5 104 Si 3Si - 1Al4O - 2OHSi4O - 2OHMg4 Al 4 Al9,5 10Mg4 Si 3Si - 1AlTALCO6 O 6 OKMICASi 4O 10Al 2(OH) 2Si 3AlO 10Al 2(OH) 2K
•Tipo de 14Å (Te-De-Te-Oc-Oc):•Hoja doble, una presenta la estructura anterior y otra (llamada hojabrucítica) está formada por dos capas compactas de (OH).Clorita6 O3Si - 1Al4O - 2OH4 Al4O - 2OH3Si - 1Al6 O6 OH4Mg -4Al6 OH
CLASIFICACIÓN DE LOS FILOSILICATOS1.- Iones que ocupan la coordinación octaédrica.Dioctaédricos: con iones trivalentes, generalmente, aluminioTrioctaédricos: con iones divalentes, por ejemplo magnesio
IMPUREZAS ARCILLA - SILICELAS ARCILLAS SEDIMENTARIAS PRESENTAN NORMALMENTECANTIDADES APRECIABLES DE CUARZO QUE HA SIDO TRANSPORTADO YDEPOSITADO JUNTO CON LOS MINERALES ARCILLOSOS. ADEMÁS DECUARZO, SE PRESENTAN FORMAS CRIPTOCRISTALINAS Y AMORFAS DELA SÍLICE, COMO LA CALCEDONIA Y EL PEDERNAL. ESTAS FORMAS DESÍLICE SON MUCHO MÁS REACTIVAS QUE EL CUARZO CRISTALINO Y PORLO TANTO SE CONVIERTEN MÁS RAPIDAMENTE EN CRISTOBALITA YTRIDIMITA Y REACCIONAN CON LOS COMPUESTOS FUNDENTES ATEMPERATURAS MÁS BAJAS.EL EFECTO DE LA SÍLICE LIBRE EN LAS ARCILLAS ES EL SIGUIENTE:- REDUCE LA PLASTICIDAD.- DISMINUYE LA CONTRACCIÓN DE SECADO Y COCCIÓN.- REDUCE LA RESISTENCIA MECÁNICA.-REDUCE LA REFRACTARIEDAD EN MUCHOS CASOS, AUNQUE NO ENTODOS
IMPUREZAS DE LA ARCILLA - ALÚMINALA ALÚMINA SE PRESENTA EN LAS ARCILLAS NO SOLAMENTE ENFORMA DE MINERALES ARCILLOSOS SINO TAMBIÉN COMOFELDESPATOS, MICA Y OTROS SILICATOS ALUMINICOS. EN ALGUNASARCILLAS SE PRESENTA ALÚMINA LIBRE DERIVADA DE BAUXITAS YLATERITAS. LAS ARCILLAS HALLOISÍTICAS CONTIENEN,FRECUENTEMENTE, ALÚMINA LIBRE ASOCIADA EN FORMA DE GIBBSITA.ESTAS ARCILLAS SON VALIOSAS PARA SU UTILIZACIÓN ENREFRACTARIOS. OTRAS ARCILLAS PUEDEN CONTENER ALÚMINA ENFORMA DE GIBBSITA, DIÁSPORO (AlO.OH) O ALÚMINA COLOIDAL.LOS COMPUESTOS ALUMINOSOS NO ARCILLOSOS TIENEN LOSSIGUIENTES EFECTOS SOBRE LAS ARCILLAS:-REDUCEN LA PLASTICIDAD.- AUMENTAN LA REFRACTARIEDAD DE LA ARCILLA SIEMPRE QUEEL CONTENIDO EN ALÚMINA SEA MAYOR DEL 5%, YA QUE LAREFRACTARIEDAD DE LOS LADRILLOS DE SÍLICE SE REDUCEENORMEMENTE CON EL CONTENIDO EN ALÚMINA.APROXIMADAMENTE POR CADA 0.1 % DE ALÚMINA SE REDUCELA TEMPERATURA MÁXIMA DE OPERACIÓN DEL ORDEN DE 10 °C.
IMPUREZAS DE LA ARCILLA - ALCALINOSLOS ALCALINOS ESTÁN PRESENTES EN LAS ARCILLAS COMO:(A).- SILICATOS O SILICATOS ALÚMINICOS (FELDESPATOS, MICAS, ETC.)(B).- CATIONES ADSORBIDOS EN LA SUPERFICIE DE LOS CRISTALES DELOS MINERALES ARCILLOSOS. EL GRADO DE ADSORCIÓN DEPENDE DELA SUPERFICIE ESPECÍFICA Y DE LA NATURALEZA DE LOS MINERALESARCILLOSOS.(C).- SALES SOLUBLES COMO SULFATO SÓDICO, CLORURO SÓDICO,SULFATO POTÁSICO, ETC.EN GRES, PORCELANA Y OTROS PRODUCTOS CERÁMICOS CUANTOMAYOR ES LA PROPORCIÓN DE ALCALINOS MÁS FUNDENTE ES LAMASA.EL PRINCIPAL EFECTO DE LOS ÁLCALIS PRESENTES EN LAS ARCILLAS ESREDUCIR LA REFRACTARIEDAD O TEMPERATURA DE VITRIFICACIÓN, YA QUESE COMBINAN CON LA SÍLICE Y LA ALÚMINA PARA DAR FASES LÍQUIDAS ABAJA TEMPERATURA DE FUSIÓN (=700 °C) Y CONSECUENTEMENTE SEDENOMINAN FUNDENTES.
IMPUREZAS DE LA ARCILLA – MINERALES DE HIERROLOS PRINCIPALES EFECTOS DE LOS COMPUESTOS DE HIERRO EN LASARCILLAS SON:-VARIACIÓN DEL COLOR.ÓXIDO de HIERRO COLOR ROJOÓXIDO de TITANIO COLOR AZUL- REDUCCIÓN DE LA REFRACTARIEDAD DE LA ARCILLA.- LOS COMPUESTOS SOLUBLES PUEDEN DAR EFLORESCENCIAS.- PUEDEN FORMAR MANCHAS VISIBLES EN LOS PRODUCTOSCOCIDOS.
IMPUREZAS DE LA ARCILLA – MINERALES DE CALCIOLOS PRINCIPALES EFECTOS DE LOS MINERALES DE CALCIO EN LAS ARCILLAS SON:-ACTÚAN COMO FUNDENTES, YA QUE SE COMBINAN CON LA SÍLICE Y LA ALÚMINAPARA DAR EUTÉCTICOS DE BAJO PUNTO DE FUSIÓN Y POR TANTO REDUCEN LATEMPERATURA DE VITRIFICACIÓN Y LA REFRACTARIEDAD.-LOS COMPUESTOS DE CALCIO, CUANDO SE COMBINAN CON MINERALES DE HIERRO,REDUCEN EL COLOR ROJO DE ESTOS ÚLTIMOS TRASLADÁNDOLO HACIA EL BLANCO.-EL CARBONATO CÁLCICO, CUANDO SE CALIENTA A 900 °C, SE CONVIERTE EN ÓXIDOCÁLCICO QUE, SI PERMANECE SIN COMBINAR, EN EL ENFRIAMIENTO PUEDEABSORBER HUMEDAD DEL AIRE, AUMENTAR DE VOLUMEN Y QUEBRAR O FISURAR LAPIEZA.-EL SULFATO CÁLCICO ES ESTABLE A LA COCCIÓN A BAJA TEMPERATURA,PERMANECIENDO INALTERABLE EN LADRILLOS DE CONSTRUCCIÓN Y AZULEJOS.ESTA ES UNA DE LAS CAUSAS MÁS FRECUENTES DE EFLORESCENCIAS.
FELDESPATOSLos feldespatos son los minerales más abundantes de la corteza terrestre y participan enella con más de 60% de volumen, en detalle las plagioclasas ocupan el 41% de volumen, losfeldespatos alcalinos ocupan el 21% de volumen. Forman un grupo de 3 componentes: Feldespato potásico KAlSi 3 O 8 (Sanidina) Albita NaAlSi 3 O 8 Anortita CaAl 2 Si 2 O 8Los minerales mixtos con una composición entre el feldespato potásico y la albita sedenominan FELDESPATOS ALCALINOS, los minerales mixtos de composición entre albita yanortita forman el grupo de las PLAGIOCLASAS.El tipo estructural a partir del cual se pueden derivar todas las demásestructuras de los feldespatos es el de la sanidina KAlSi3O8.Las estructuras de los feldespatosestán formadas por un armazóntridimensional de tetraedros SiO 4y AlO 4 , que comparten sus cuatrooxígenos apicales con lostetraedros contiguos, dando unared tridimensional en cuyoshuecos se sitúan los cationes Na,K, Ca y Ba.Este armazón posee cierta elasticidady puede ajustarse al tamaño de loscationes cuando estos son de mayortamaño (K y Ba), originando unasimetría monoclínica. Cuando loscationes son de menor tamaño (Na yCa), la simetría es triclínica.
FELDESPATOSLas relaciones entre ellos se presentan en el SISTEMA TERNARIO DE LOSFELDESPATOS. En los extremos de este triangulo están expresados las formulascristaloquímicas de las tres componentes. Todas las mezclas entre estas trescomponentes se encuentran en un punto determinado dentro del triángulo.Las PLAGIOCLASAS tienendistintas denominaciones segúnsu composición química o es decirsegún su contenido en lacomponente Albita (Ab) y en lacomponente Anortita (An)Tipo deplagioclasaAlbita (Ab) en % Anortita en %Albita 100 - 90 0 - 10Oligoclasa 90 - 70 10 - 30Andesina 70 - 50 30 - 50Labradorita 50 - 30 50 - 70Bytownita 30 - 10 70 - 90Anortita 10 - 0 90 - 100SISTEMATERNARIO DE LOSFELDESPATOS
CUALIDADES QUE DEBE PRESENTAR UN POLVO CERAMICO1.- TAMAÑO Y DISTRIBUCION DE TAMAÑOS2.- FORMA Y RUGOSIDAD SUPERFICIAL3.- GRAN PUREZA QUIMICA4.- GRAN SUPERFICIE ESPECIFICA5.- GRAN HOMOGENEIDAD FISICA. ESTADO DE AGLOMERACION(EVITAR LA PRESENCIA DE AGLOMERADOS)6.- BUENA APTITUD A LA SINTERIZACION7.- ESTADO DE CRISTALIZACION CONSTANTE8.- ESTRUCTURA Y QUIMICA DE LA SUPERFICIELA CALIDAD DE LOSPOLVOS DEPENDE DELMÉTODO DE PREPARACIÓNOBJETIVOS:‣DENSIDAD ALTA (MINIMA POROSIDAD)‣TAMAÑO DE GRANO PEQUEÑO‣MICROESTRUCTURA UNIFORMELAS CARACTERÍSTICAS DELPOLVO TIENEN UNAINFLUENCIA SIGNIFICATIVA ENLA HOMOGENEIDAD DELEMPAQUETAMIENTO DE LAPIEZA CONSOLIDADA YEN LA EVOLUCIÓNMICROESTRUCTURAL YPROPIEDADES DE LA PIEZASINTERIZADA
FORMA Y RUGOSIDAD SUPERFICIAL
PEQUEÑAS VARIACIONES EN LA COMPOSICIÓN QUÍMICA Y EN LAPUREZA DEL POLVO PUEDE PROVOCAR SIGNIFICATIVOS EFECTOS ENLA MICROESTRUCTURA Y PROPIEDADES DE LOS MATERIALESCERÁMICOS AVANZADOS
EL TAMAÑO DE PARTICULA TIENE UN GRAN EFECTO ENLA SINTERIZACIONLA VELOCIDAD A LA CUAL DENSIFICA UN CUERPO AUMENTADE FORMA SIGNIFICATIVA AL DISMINUIR EL TAMAÑO DE PARTICULAUN TAMAÑO DE PARTICULA DE ~1 mm PERMITE ALCANZARDENSIDADES ALTAS EN UN PERIODO DE TIEMPO RAZONABLE, POREJEMPLO UNAS POCAS HORAS
POLVO CON UNA DISTRIBUCION ESTRECHA DE TAMAÑOS DEPARTICULAS (POLVO MONODISPERSO)DENSIDADES DE EMPAQUETAMIENTO EN LA PIEZA EN VERDE MASBAJAS QUE EN EL CASO DEL POLVO POLIDISPERSOPERMITE CONTROLAR LA MICROESTRUCTURA DURANTE LASINTERIZACIONLAS FORMAS ESFERICAS O EQUIAXICAS SON BENEFICIOSAS PARACONTROLAR LA UNIFORMIDAD DEL EMPAQUETAMIENTO
POLVO CON UNA DISTRIBUCION AMPLIA DE TAMAÑOS DE PARTICULAS(POLVO POLIDISPERSO)‣DENSIDADES DE EMPAQUETAMIENTO ALTAS EN LA PIEZA EN VERDE‣DIFICULTAD DE CONTROLAR LA MICROESTRUCTURA DURANTELA SINTERIZACIONUN PROBLEMA COMUN ESQUE LOS GRANOSGRANDES CRECEN AEXPENSAS DE LOS MASPEQUEÑOS, HACIENDOIMPOSIBLE LACONSECUCIÓN DE UNADENSIDAD ALTA CON UNTAMAÑO DE GRANOCONTROLADONO EXISTE POROSIDAD RESIDUALLA MICROESTRUCTURA CONSISTE EN GRANOS CRISTALINOSSEPARADOS UNOS DE OTROS POR LÍMITES DE GRANO
POROS
TIPOS DE PARTÍCULAS
FORMACIÓN DE AGLOMERADOS DEBIDO A LAS FUERZAS DE CAPILARIDADSURGEN COMO CONSECUENCIA DE LA CONDENSACIÓN DE VAPORESATMOSFÉRICOS, NORMALMENTE AGUA, EN LA SUPERFICIE DEL POLVO.CUANDO EL LÍQUIDO CONDENSADO “MOJA” AL SÓLIDO, SE CONCENTRA ENLA ZONA DE CONTACTO DE LAS PARTÍCULAS Y GENERA FUERZAS DECAPILARIDAD ATRACTIVAS ENTRE ELLAS.SE FORMAN ASÍ LAS LLAMADAS UNIONES PENDULARES (“PENDULARBONDS”)La fuerza atractiva entre partículas depende de lacantidad de líquido condensado, perobásicamente se puede describir por la siguienteecuación:F 5LVD
LA FUERZA DE CAPILARIDAD ATRACTIVA HACE QUE EL AGLOMERADO TENGAUNA RESISTENCIA APROXIMADA DADA POR: 7 SLV1DPara partículas por debajo de 100 micras,un líquido que moje proporciona un efectoaglomerante significativo.
AGLOMERADOPARTICULAPRIMARIA
PRESENCIA DE AGLOMERADOSEMPAQUETAMIENTO HETEROGENEO EN LA PIEZA EN VERDE, LO QUECONDUCE A UNA SINTERIZACIÓN DIFERENCIAL DURANTE LA ETAPA DECOCCION.LA SINTERIZACION DIFERENCIAL OCURRE CUANDO ZONASDIFERENTES DE LA PIEZA CONTRAEN A VELOCIDADES DIFERENTES, LOQUE PUEDE DAR LUGAR AL DESARROLLO DE GRANDES POROS Y HUECOSDEBIDOS A LAS GRIETAS EN LA PIEZA COCIDAHUECO DEBIDO A UNA GRIETAPRODUCIDA POR UNAGLOMERADO DE ZrO 2 QUE SECONTRAE DENTRO DE LAMATRIZ Al 2 O 3 /ZrO 2 QUE LERODEA
IMPUREZAS DE LA SUPERFICIE DEL POLVOPUEDEN INFLUIR SOBRE LA DISPERSION DEL POLVO EN UN LIQUIDOETAPA DE COCCIONLAS IMPUREZAS PUEDEN CONDUCIR A LA FORMACION DE UNA PEQUEÑACANTIDAD DE FASE LIQUIDA A LA TEMPERATURA DE SINTERIZACION, LOQUE CAUSA UNCRECIMIENTO SELECTIVO FORMANDOSE GRANOS DE MAYORTAMAÑOHETEROGENEIDADMICROESTRUCTURALDEBIDA A LAPRESENCIA DEIMPUREZAS EN UNAALUMINA PRENSADAEN CALIENTE
RESUMEN
MÉTODOSDE PREPARACIÓNDEPOLVOS CERÁMICOS