EQUILIBRIO QUÍMICO
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
QUÍMICA II Dpto. de Química Física<br />
Tema 6 Equilibrio químico<br />
19<br />
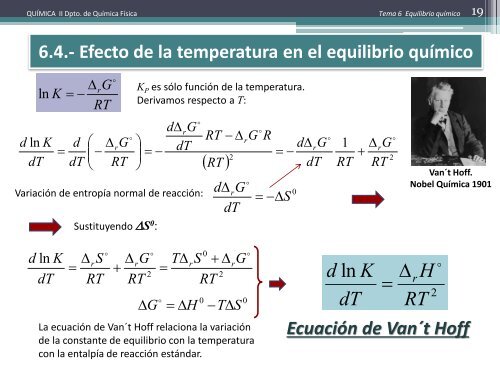
6.4.- Efecto de la temperatura en el equilibrio químico<br />
d ln K<br />
dT<br />
<br />
<br />
ln K rG<br />
RT<br />
<br />
d<br />
dT<br />
<br />
<br />
<br />
<br />
rG<br />
RT<br />
<br />
K P es sólo función de la temperatura.<br />
Derivamos respecto a T:<br />
drG<br />
<br />
dT<br />
<br />
Variación de entropía normal de reacción:<br />
Sustituyendo S 0 :<br />
<br />
RT<br />
r<br />
G<br />
R<br />
d<br />
<br />
G<br />
2<br />
2<br />
RT<br />
dT RT RT<br />
d r<br />
<br />
G<br />
dT<br />
<br />
<br />
<br />
S<br />
0<br />
r<br />
<br />
1<br />
<br />
<br />
r<br />
G<br />
<br />
Van´t Hoff.<br />
Nobel Química 1901<br />
d ln K<br />
dT<br />
rS<br />
<br />
RT<br />
<br />
rG<br />
<br />
2<br />
RT<br />
<br />
G<br />
<br />
T<br />
<br />
r<br />
H<br />
0<br />
S <br />
2<br />
RT<br />
0<br />
r<br />
G<br />
TS<br />
La ecuación de Van´t Hoff relaciona la variación<br />
de la constante de equilibrio con la temperatura<br />
con la entalpía de reacción estándar.<br />
0<br />
<br />
d ln K<br />
<br />
dT<br />
rH<br />
RT<br />
Ecuación de Van´t Hoff<br />
2