EQUILIBRIO QUÍMICO
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
QUÍMICA II Dpto. de Química Física<br />
Tema 6 Equilibrio químico<br />
31<br />
Efecto ión común y efecto salino. Comparativa<br />
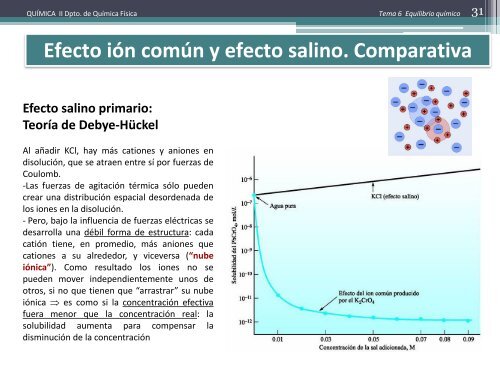
Efecto salino primario:<br />
Teoría de Debye-Hückel<br />
Al añadir KCl, hay más cationes y aniones en<br />
disolución, que se atraen entre sí por fuerzas de<br />
Coulomb.<br />
-Las fuerzas de agitación térmica sólo pueden<br />
crear una distribución espacial desordenada de<br />
los iones en la disolución.<br />
- Pero, bajo la influencia de fuerzas eléctricas se<br />
desarrolla una débil forma de estructura: cada<br />
catión tiene, en promedio, más aniones que<br />
cationes a su alrededor, y viceversa (“nube<br />
iónica”). Como resultado los iones no se<br />
pueden mover independientemente unos de<br />
otros, si no que tienen que “arrastrar” su nube<br />
iónica es como si la concentración efectiva<br />
fuera menor que la concentración real: la<br />
solubilidad aumenta para compensar la<br />
disminución de la concentración