Cours 2 CP NCI 2012 - Département de biologie
Cours 2 CP NCI 2012 - Département de biologie
Cours 2 CP NCI 2012 - Département de biologie
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Neuro<strong>biologie</strong> <strong>de</strong>s canaux ioniques<br />
Master I DI<br />
porcher@inmed.univ-mrs.fr
Chapitre 2 : l’excitabilité<br />
Luigi Galvani (1737-1798)<br />
Un courant électrique appliqué à un nerf provoque une contraction musculaire.<br />
Chaque animal contient <strong>de</strong> l’électricité continuellement présente dans son corps,<br />
"l’électricité animale".<br />
Lorsque nerf et muscle sont reliés l'un à l'autre par un ustensile fait <strong>de</strong> <strong>de</strong>ux<br />
métaux différents, cette électricité se décharge.
Avec une quantité adéquate d’électricité injectée dans le cerveau, un cadavre<br />
revient à la vie
Alessandro Volta (1745-1827)<br />
La rivalité entre Galvani et Volta<br />
D'aprés Volta, les travaux <strong>de</strong> Galvani ne prouvent pas<br />
l'existence d'une électricité animale, mais au contraire<br />
celle d'une électricité métallique.<br />
Volta ne met pas en doute les expériences <strong>de</strong> Galvani<br />
mais les interprète différemment.
l’excitabilité<br />
1850 : H. von Helmholtz mesure la<br />
vitesse <strong>de</strong> l'influx nerveux dans un<br />
nerf.<br />
Vitesse <strong>de</strong> quelques m/s seulement.<br />
C’est donc beaucoup plus lent que<br />
L’électricité circulant dans un fil<br />
Métallique.<br />
La cellule agit comme une pile électrique
L’excitabilité<br />
Les neurones transmettent <strong>de</strong>s informations par le biais<br />
<strong>de</strong> signaux électriques. Ces signaux se basent sur<br />
<strong>de</strong>s flux d’ions membranaire.<br />
Nous allons abor<strong>de</strong>r les notions <strong>de</strong> :<br />
• Potentiel <strong>de</strong> repos membranaire<br />
• Potentiel seuil<br />
• Potentiel d’action<br />
• Potentiel d’inversion
Mécanisme du potentiel <strong>de</strong> repos<br />
La membrane plasmique est constituée d’une bicouche lipidique isolante à propriété capacitive<br />
(propriété d’un con<strong>de</strong>nsateur à accumuler un gradient <strong>de</strong> charges électriques <strong>de</strong> part et d’autre d’une<br />
substance isolante).<br />
On peut donc assimiler un élément <strong>de</strong> membrane à une pile <strong>de</strong> 70mV (Um), négative à l’intérieur,<br />
reliée à une résistance membranaire (Rm) mise en parallèle avec un con<strong>de</strong>nsateur membranaire<br />
(Cm).
Partie hydrophyle<br />
La membrane biologique<br />
Partie centrale<br />
hydrophobe<br />
La membrane plasmique constitue une barrière entre le milieu intra et extracellulaire.<br />
Elle est composée d’une bicouche <strong>de</strong> phospholipi<strong>de</strong>s. Les protéines<br />
membranaires traversent (proteines intrinseques) ou sont attachées à la<br />
bicouche <strong>de</strong> lipi<strong>de</strong>s sans la pénétrer (protéines extrinsèques)
Canaux et protéines <strong>de</strong> transport<br />
Les membranes <strong>de</strong>s neurones possè<strong>de</strong>nt <strong>de</strong> nombreuses protéines qui participent au transport<br />
<strong>de</strong>s molécules :<br />
1. canaux ioniques (voltage- ou chimio-dépendants i.e. neurotransmetteur).<br />
2. Uniporteurs qui permettent à <strong>de</strong> petites molécules hydrophyles <strong>de</strong> traverser la membrane<br />
selon leur gradient <strong>de</strong> concentration (diffusion facilitée).<br />
3. Transports couplés aux mouvements d’autres substances (en général <strong>de</strong>s ions), soit dans<br />
la même direction (symporteur), soit dans <strong>de</strong>s directions opposées (antiporteur).<br />
4. Transport actif : processus dépendant d’energie utilisé pour transporter <strong>de</strong>s ions ou <strong>de</strong><br />
petites molécules contre leur gradient électrochimique.
• D’un changement <strong>de</strong><br />
potentiel<br />
transmembranaire.<br />
• Il existe <strong>de</strong>ux types <strong>de</strong><br />
potentiels<br />
transmembranaires<br />
– Potentiel <strong>de</strong> repos<br />
(pas excité)<br />
– Potentiel d’action<br />
(excité suite à une<br />
stimulation)<br />
D’où vient l’excitabilité ?
L’excitabilité : principe<br />
Solution aqueuse d’ions (NaCl)<br />
Les électrons du métal<br />
sont attirés par la borne positive<br />
et repoussés par la borne négative:<br />
mouvement d’électrons<br />
mouvement <strong>de</strong> particules chargées<br />
genèse d’un courant<br />
Les ions positifs (Na + ) sont attirés<br />
par la borne -. Les ions<br />
négatifs (Cl - ) par la borne +<br />
et repoussés par la borne - :<br />
mouvement d’ions
L’excitabilité<br />
Les ions + (cations) en solution attirent les molécules d'eau par leur<br />
partie négative. Les ions - (anions) en solution attirent les molécules<br />
d'eau par leur partie positive. Il en résulte que chaque ion s'entoure<br />
d'un certain nombre <strong>de</strong> molécules d'eau.<br />
Ce phénomène est appelé solvatation <strong>de</strong>s ions. Lorsque le solvant<br />
est l'eau la solvatation est appelée hydratation.
Comment mesurer le potentiel membranaire<br />
Solution conductrice : e.g. la micropipette est remplie d’une solution saline (KCl)
THE PATCH-CLAMP TECHNIQUE<br />
Erwin Neher Bert Sakmann<br />
(1991 Nobel Laureates) ‘gigaseal’
Configuration insi<strong>de</strong>-out<br />
La face intracellulaire du canal baigne dans le milieu <strong>de</strong> superfusion<br />
But: étudier la régulation <strong>de</strong> l’activité d’un canal ou d’un récepteur par <strong>de</strong>s<br />
enzymes, messagers seconds etc…. Cela donne une idée <strong>de</strong> la régulation<br />
intracellulaire <strong>de</strong> l’activité <strong>de</strong>s canaux
Configuration whole-cell<br />
Le milieu intracellulaire est conditionné par la solution intra-pipette<br />
But: étudier l’activité électrophysiologique <strong>de</strong> l’ensemble <strong>de</strong>s canaux et <strong>de</strong>s<br />
récepteurs au niveau d’une cellule entière.
Configuration cellule attachée<br />
But: Etudier les propriétés d’un canal ionique ou d’un récepteur dans les<br />
conditions physiologiques (sans perturber le milieu intracellulaire).
Configuration outsi<strong>de</strong>-out<br />
Un canal ionique ou un récepteur est isolé, sa partie extracellulaire baigne dans<br />
la milieu <strong>de</strong> superfusion<br />
But: étudier les propriétés d’un récepteur-canal et déterminer particulièrement<br />
l’affinité du récepteur pour un agoniste
Patch-clamp recording : setup<br />
la préparation (cellule) est reliée via une pipette <strong>de</strong> patch à une tête<br />
d'amplificateur, elle même connectée à un amplificateur, lui-même connecté à<br />
un ordinateur.
Potentiel <strong>de</strong> repos<br />
Cette différence <strong>de</strong> potentiel est maintenue<br />
grâce à la pompe Na + K + .
Potentiel <strong>de</strong> repos<br />
• Dans une cellule, la charge électrique est différente <strong>de</strong><br />
celle du milieu.<br />
• Cela génère une différence <strong>de</strong> potentiel (ddp)<br />
• Cette ddp est créée par les différences dans la<br />
composition du milieu intérieur et extérieur<br />
• Pourquoi ?<br />
– Perméabilité sélective <strong>de</strong> la membrane.<br />
• perméable au K + et Cl - .<br />
• Imperméable au Na + .<br />
– Mécanisme <strong>de</strong> transport actif. (Na + et Cl - )
Concentrations en ions <strong>de</strong> part et d’autre <strong>de</strong> la membrane<br />
Extérieur <strong>de</strong> la membrane:<br />
• Ions positifs = Na + surtout (un peu <strong>de</strong> K + aussi)<br />
• Ions négatifs = Cl - surtout<br />
Surplus d’ions +<br />
Intérieur du neurone:<br />
• Ions positifs = K + surtout (un peu <strong>de</strong> Na + aussi)<br />
• Ions négatifs = Protéines et ions phosphates<br />
Surplus d’ions -<br />
BILAN : + à l’extérieur; - à l’intérieur
Supposons que <strong>de</strong> part et d’autre d’une membrane on ait<br />
autant d’ions positifs que négatifs<br />
10 Cl - et 10 Na +<br />
10 K + et 10 ions -<br />
Potentiel nul (autant <strong>de</strong> + que <strong>de</strong> -)<br />
Potentiel nul (autant <strong>de</strong> + que <strong>de</strong> -)
Que se passe-t-il si on ajoute <strong>de</strong>s canaux permettant le passage<br />
<strong>de</strong>s K + , mais pas <strong>de</strong>s autres ions?<br />
==> diffusion du potassium<br />
10 Cl-<br />
10 Na +<br />
3 K+<br />
10 ions -<br />
7 K +<br />
13 charges + et 10 - = +3<br />
+3<br />
-3<br />
7 charges + et 10 - = -3
La diffusion ne se fera pas jusqu’à équilibre <strong>de</strong>s<br />
concentrations du K +<br />
Le K + cherche à<br />
diffuser en suivant<br />
son gradient <strong>de</strong><br />
concentration<br />
Le K + est attiré par<br />
les charges - <strong>de</strong><br />
l'intérieur et<br />
repoussé par les<br />
charges + <strong>de</strong><br />
l'extérieur<br />
Le gradient électrique qui se forme arrête la diffusion.
À l’équilibre:<br />
+3<br />
Valeurs<br />
arbitraires<br />
-3<br />
Les charges positives en surplus<br />
s ’accumulent sur la membrane<br />
Les charges négatives en surplus<br />
s ’accumulent sur la membrane
The plasma membrane separates two media of different ionic composition<br />
Cations:<br />
• Intracellular: K +<br />
• Extracellular: Na +<br />
Anions:<br />
• Intracellular: organic molecules (P - ):<br />
negatively charged amino acids<br />
(glutamate and aspartate), proteins,<br />
nucleic acids, phosphates, etc…<br />
• Extracellular: Cl -<br />
A marked difference between cytosolic and<br />
extracellular Ca 2+ concentrations is also<br />
observed
The plasma membrane separates two media of different ionic composition<br />
Intracellular and extracellular media are neutral ionic solutions: in each<br />
medium, the concentration of (+) ions = (-) ions.<br />
Extracellular:<br />
[Na + ]e + [K + ]e + 2[Ca 2+ ]e = 140 +3 + (2 x 1.5) = 146 mM and [Cl - ]e = 146 mM<br />
Intracellular:<br />
[Na + ] i + [K + ] i + 2[Ca 2+ ] i = 7 + 140 + 0.0002 = 147 mM but [Cl - ] i = 7 mM<br />
In the intracellular compartment, other anions than chlori<strong>de</strong> ions are present<br />
and compensate for the positive charges (HCO 3 - , PO4 2- , aminoacids, proteins,<br />
nucleic acids, etc …).
The unequal distribution of ions across the neuronal plasma<br />
membrane is kept constant by active transport of ions<br />
Concentration gradients for Na + , K + , Ca 2+ and Cl - ions are constant in the<br />
external and cytosolic compartments.<br />
Two hypotheses can explain this constancy:<br />
1. Na + , K + , Ca 2+ and Cl - ions cannot cross the plasma membrane. In<br />
that case, concentration gradients need to be established only<br />
once in the lifetime.<br />
2. Plasma membrane is permeable to Na + , K + , Ca 2+ and Cl - ions but<br />
there are mechanisms that continuously re-establish the<br />
gradients and maintain constant the unequal distribution of ions.
The unequal distribution of ions across the neuronal plasma<br />
membrane is kept constant by active transport of ions<br />
When proteins are absent from a synthetic lipid bilayer, no movements of<br />
ions occur.<br />
The lipid bilayer is a barrier for the diffusion of ions and most polar<br />
molecules.<br />
E.g. When a axon is immerged in a bath containing a control concentration<br />
of radioactive *Na + ( 24 Na + ), *Na + constantly appear in the cytoplasm.<br />
This *Na + influx is not affected by dinitrophenol (DNP), a blocker of ATP<br />
synthesis in mitochondria. It does not require energy expenditure.<br />
This is passive transport.<br />
But what are the mechanisms that maintain concentration gradients across<br />
neuronal membranes?
The unequal distribution of ions across the neuronal plasma<br />
membrane is kept constant by active transport of ions<br />
When the reverse experiment is conducted, the axon is passively loa<strong>de</strong>d<br />
with radioactive *Na + , and is transferred to a bath containing cold Na + .<br />
Measuring the quantity of *Na + that appears in the bath per unit of time<br />
(d*Na + /dt, expressed in counts per minute) allows quantification of the efflux<br />
of *Na +.<br />
In the presence of dinitrophenol (DNP) this *Na + efflux quickly diminishes to<br />
nearly zero.<br />
The process can be started up again by intracellular injection of ATP.<br />
Therefore the *Na + efflux is active transport.
Ionic composition of cytosol and<br />
extracellular compartments are<br />
maintained at the expense of a<br />
continuous basal metabolism that<br />
provi<strong>de</strong>s energy (ATP) utilized to<br />
actively transport ions and thus to<br />
compensate for their passive<br />
movements.<br />
(a) Effect of dinitrophenol on the outflux of *Na + as a function of time<br />
(b) Passive and active Na + fluxes are in opposite directions
La polarité <strong>de</strong> la membrane est donc due:<br />
• Différence <strong>de</strong> concentration en ions entre l’intérieur<br />
et l’extérieur <strong>de</strong> la cellule.<br />
• Perméabilité sélective <strong>de</strong> la membrane (laisse<br />
passer le K+).<br />
La polarité se maintient même si<br />
du Na + parvient à pénétrer:<br />
pompes à sodium / potassium.<br />
– Une pompe Na+ K+ travaille à<br />
200 Na + /secon<strong>de</strong>s<br />
– Il y a plus <strong>de</strong> 200 pompes / µm 2 .
Equation <strong>de</strong> Nernst<br />
– Ex = potentiel d’équilibre pour l’ion x<br />
– R = constante <strong>de</strong>s gaz parfaits<br />
– T = température absolue (Kelvin)<br />
– Z = valence (charge électrique) <strong>de</strong> l’ion perméant
Origine du potentiel <strong>de</strong> membrane<br />
• Le potentiel <strong>de</strong> membrane est le résultat <strong>de</strong> la différence<br />
<strong>de</strong> concentration d’ions (gradients) et <strong>de</strong> la perméabilité<br />
sélective <strong>de</strong> la membrane cellulaire.<br />
– Si P K est importante, E m est proche <strong>de</strong> E K<br />
– if P Na est importante, E m est proche <strong>de</strong> E Na<br />
– etc. etc<br />
E<br />
m<br />
=<br />
RT<br />
F<br />
ln<br />
P [ K] + P [ Na] + P [ Cl]<br />
K o Na o Cl i<br />
P [ K] + P [ Na] + P [ Cl]<br />
K i Na i Cl o
Les potentiels électriques<br />
• Ces potentiels électriques dépen<strong>de</strong>nt<br />
<strong>de</strong> <strong>de</strong>ux sortes <strong>de</strong> protéines <strong>de</strong> la<br />
membrane cellulaire :<br />
– Les canaux ioniques<br />
– Les pompes à ions
Les canaux ioniques déterminent la perméabilité<br />
• Ils permettent à certains ions<br />
<strong>de</strong> franchir la membrane<br />
suivant leurs gradients <strong>de</strong><br />
concentration.<br />
• L’ouverture <strong>de</strong> ces canaux<br />
augmente la perméabilité<br />
membranaire.
Les pompes à ions instaurent <strong>de</strong>s gradients ionique<br />
• Ils transportent activement<br />
certains ions, contre leurs<br />
gradients <strong>de</strong> concentration.
Résumé canaux et pompes<br />
Canaux et pompes travaillent les uns contre les autres<br />
et produisent ainsi l’électricité cellulaire.<br />
• Les pompes instaurent <strong>de</strong>s différences <strong>de</strong><br />
concentration ionique<br />
• Les canaux utilisent ces gradients <strong>de</strong> concentration<br />
pour permettent une diffusion <strong>de</strong>s ions dans le sens<br />
<strong>de</strong> leurs gradients chimiques
Le potentiel d’action<br />
Les neurones peuvent réagir à un stimulus (excitabilité).<br />
Réaction = ouverture <strong>de</strong> canaux Na + <strong>de</strong> la membrane<br />
Baisse d’ions + à l’extérieur<br />
Hausse d’ions + à l’intérieur<br />
Il y a dépolarisation <strong>de</strong> la membrane<br />
(l’intérieur qui était négatif <strong>de</strong>vient moins négatif)
• Début : dépolarisation proportionnelle à la stimulation<br />
(infraliminaire).<br />
• Si la stimulation est assez forte, la dépolarisation atteint<br />
un seuil <strong>de</strong> dépolarisation (supraliminaire).<br />
– Tous les canaux Na + ouvrent <strong>de</strong> façon explosive = entrée<br />
massive <strong>de</strong> Na + .<br />
– L’intérieur <strong>de</strong>vient même + (+30-40 mV) !<br />
– L’entrée <strong>de</strong> Na+ arrête grâce à un système d’inactivation <strong>de</strong>s<br />
canaux Na + .<br />
• Ensuite, repolarisation, par ouverture <strong>de</strong> canaux K + (=<br />
sortie massive <strong>de</strong> K + ).<br />
• La pompe rétablit les ions.<br />
Le potentiel d’action
Le potentiel d’action<br />
Lorsque la dépolarisation au point stimulé dépasse un certain seuil (~ -<br />
50 mV), il y a un potentiel d’action <strong>de</strong> déclenché.<br />
Le stimulus 1 (S1) est plus petit que S2 qui est plus petit que S3. Seul<br />
S3 provoque une dépolarisation qui atteint le seuil du neurone.
• Si la dépolarisation ne dépasse pas le seuil : la<br />
membrane reprend sa polarisation normale et il n’y a<br />
pas d’influx.<br />
• Si la dépolarisation dépasse le seuil ==> la<br />
dépolarisation se poursuit jusqu’à + 40 mV :<br />
dépolarisation et repolarisation = potentiel d’action<br />
==> influx nerveux<br />
• Peu importe l’intensité du stimulus, la dépolarisation<br />
ne dépassera pas + 40 mV
Entrée massive <strong>de</strong> Na + ==> baisse <strong>de</strong> la polarité là où<br />
les canaux à sodium se sont ouverts.<br />
- 70mV → - 60mV → - 50 mV → ...<br />
Si le seuil est atteint, la polarité s'inverse au point stimulé.
Le point dépolarisé reprend rapi<strong>de</strong>ment sa polarité:<br />
• Fermeture <strong>de</strong>s canaux Na + .<br />
• Ouverture <strong>de</strong> canaux à K +<br />
qui étaient fermés<br />
==> ↑ perméabilité au K +<br />
==> ↑ sortie <strong>de</strong> K +<br />
= potentiel d ’action
Potentiel <strong>de</strong> repos et potentiel d’action<br />
Les changements <strong>de</strong> conductance (<strong>de</strong>s ions Na+ et K+) qui sont à<br />
la base du PA sont dépendants du voltage et du temps.
Quelques caractéristiques<br />
1) Le seuil <strong>de</strong> dépolarisation :<br />
• Le seuil <strong>de</strong> dépolarisation peut être différent d’un<br />
neurone à l’autre.<br />
• Il reste constant pour un neurone donné.<br />
• Plus un stimulus est intense, moins il a besoin d’être<br />
appliqué longtemps pour provoquer un PA.
Quelques caractéristiques<br />
2) La loi du tout-ou-rien<br />
• Dès que le seuil est atteint, il y a production d’un PA<br />
d’intensité maximale, peu importe l’intensité du<br />
stimulus.<br />
3) Les sommations locales (temporelles et spatiales)<br />
• Si le stimulus n’est pas assez intense pour déclencher le<br />
potentiel, l’effet d’un <strong>de</strong>uxième stimulus rapproché peut<br />
s’additionner, pour déclencher un PA.
Quelques caractéristiques<br />
4) Les pério<strong>de</strong>s réfractaires<br />
• Pério<strong>de</strong>s durant lesquelles le neurone est difficilement<br />
excitable :<br />
– Absolue : impossible <strong>de</strong> déclencher un PA<br />
– Relative : Il est beaucoup plus difficile <strong>de</strong> déclencher<br />
un PA.<br />
• Limitent la fréquence <strong>de</strong>s PA.
Pério<strong>de</strong>s réfractaires : Le canal Na + voltage dépendant
La phase ascendante du PA<br />
coïnci<strong>de</strong> avec la perméabilité aux<br />
ions Na+.<br />
La conductance au Na s’inactive<br />
lorsque la dépolarisation est<br />
proche <strong>de</strong> Eeq Na.<br />
Cette dépolarisation active la<br />
conductance K+ dépendante du<br />
voltage, qui a pour effet <strong>de</strong><br />
repolariser la membrane.<br />
L’hyperpolarisation rend non<br />
opérationnelle la conductance K +<br />
voltage dépendante.<br />
Modèle du PA
Potentiel seuil
Potentiel seuil
Le potentiel-seuil<br />
• Les PA d’un neurone<br />
suivent la loi du “tout ou<br />
rien”.<br />
• Ainsi, l’intensité d’un<br />
stimulus est codée par la<br />
fréquence <strong>de</strong>s PA et non par<br />
leur amplitu<strong>de</strong>.
Le potentiel-seuil<br />
• Lorsque le potentiel <strong>de</strong> membrane approche -70 mV, il y a<br />
apparition d’un PA.
Le potentiel-seuil<br />
• Il existe une plage <strong>de</strong> dépolarisation sous-liminaire :<br />
entrée Na + < sortie K + .<br />
• Seuil : c’est la valeur du PM entre le niveau du PRM<br />
et 0, pour laquelle entrée Na + = sortie K +<br />
• Dès qu’un stimulus dépolarise la membrane au-<strong>de</strong>là<br />
<strong>de</strong> cette valeur, il y a rétroaction + (entrée <strong>de</strong> Na + ) et<br />
départ d’un PA.
Le potentiel d’action<br />
• Proriétés communes à tous les PA :<br />
– Seuil<br />
– Conduction<br />
– Pério<strong>de</strong> réfractaire<br />
• Une propriété qui distingue les PA :<br />
– Forme du PA
Formes et terminologie <strong>de</strong>s PA
Formes <strong>de</strong>s potentiels d’action<br />
• La forme du PA va influencer la fréquence maximum à<br />
laquelle un neurone peut générer <strong>de</strong>s PA et le nombre <strong>de</strong><br />
PA généré pour un stimulus donné.<br />
• L’encodage <strong>de</strong> cette information apparaît en terme <strong>de</strong><br />
fréquence <strong>de</strong> décharge.
Formes <strong>de</strong>s potentiels d’action<br />
Hugunard et McCormack,<br />
Electrophysiology of the Neuron
Formes <strong>de</strong>s potentiels d’action<br />
• La forme du PA va influencer le taux <strong>de</strong> Ca 2+<br />
qui entre dans la terminaison présynaptique<br />
au cours d’un PA (ou d’un train <strong>de</strong> PA).<br />
• Le taux <strong>de</strong> Ca 2+ intracellulaire conditionne la<br />
quantité <strong>de</strong> NT qui va être libéré
Formes <strong>de</strong>s potentiels d’action<br />
• La forme <strong>de</strong>s PA est<br />
fonction <strong>de</strong> la nature <strong>de</strong>s<br />
canaux ioniques<br />
présents sur la<br />
membrane plasmique et<br />
<strong>de</strong> leur mo<strong>de</strong><br />
d’activation.<br />
Il existe <strong>de</strong>s canaux pour les différents ions.<br />
Aujourd’hui, plus <strong>de</strong> 100 canaux sont répertoriés et il y en a probablement<br />
plus…
Formes <strong>de</strong>s potentiels d’action<br />
• Les canaux Ca 2+ :<br />
– forme du potentiel d’action<br />
– influx Ca 2+ (intracellulaire)
Formes <strong>de</strong>s potentiels d’action<br />
• Les canaux Cl - :<br />
– Forme du potentiel d’action<br />
– Influence le potentiel <strong>de</strong> repos
Extracellular<br />
milieu<br />
membrane<br />
Intracellulaire<br />
milieu<br />
+ <strong>de</strong> chlore et <strong>de</strong>s effets excitateurs du GABA initialement<br />
Cl -<br />
Cl -<br />
Cl -<br />
GABA<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
GABA<br />
Cl -<br />
Cl -<br />
Cl - Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Développement<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl - Cl -<br />
Cl -<br />
Cl -<br />
GABA<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
GABA<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl -<br />
Cl-
NKCC1 accumule le Cl- dans les neurones<br />
Cl -‐ Cl -‐<br />
Cl -‐<br />
Cl -‐
GABA A R<br />
Cl -<br />
Cl -<br />
Cl -<br />
NKCC1<br />
Cl -<br />
Une séquence maturative<br />
Cl -<br />
KCC2<br />
Jeune<br />
Cl -<br />
GABA A R<br />
Cl -<br />
KCC2<br />
Cl - Cl -<br />
NKCC1<br />
Adulte
Formes <strong>de</strong>s potentiels d’action<br />
• Exemple 1 – Les canaux K + sont activés par une<br />
augmentation du taux <strong>de</strong> [Ca 2+ ] i .<br />
• Au cours d’un PA, il y a ouverture <strong>de</strong>s canaux Ca 2+ VD et<br />
entrée <strong>de</strong> Ca 2+ dans la cellule.<br />
• Cette augmentation <strong>de</strong> [Ca 2+ ] i , accroit P K , et hyperpolarise<br />
la membrane.
Formes <strong>de</strong>s potentiels d’action<br />
Hugunard et McCormack, Electrophysiology of the Neuron<br />
page 40, 1994
Formes <strong>de</strong>s potentiels d’action<br />
• Exemple 2 – Le transport électrogène d’ions par la pompe à Na + /K +<br />
peut affecter le PM.<br />
• Après une salve <strong>de</strong> PA, l’activité <strong>de</strong>s pompes va augmenter afin <strong>de</strong><br />
restaurer le taux <strong>de</strong> i[K + ] et enlever l’excès <strong>de</strong> Na + .<br />
• Parceque la pompe est électrogénique (3Na + pour 2 K + ), cette activité<br />
provoque un courant hyperpolarisant transitoire.<br />
• Cette hyperpolarisation est bloquée par l’ouabaïne
Formes <strong>de</strong>s potentiels d’action
Conduction du potentiel <strong>de</strong> membrane<br />
La conduction du courant en l’absence <strong>de</strong> PA est dite<br />
conduction passive.<br />
L’amplitu<strong>de</strong> <strong>de</strong> la variation <strong>de</strong> potentiel décroît<br />
exponentiellement avec la distance.<br />
Le courant fuit à travers la membrane <strong>de</strong> l’axone.
Conduction du potentiel <strong>de</strong> membrane<br />
Conduction passive
Conduction du potentiel <strong>de</strong> membrane<br />
Si l’intensité du courant dépolarisant est suffisant pour<br />
déclencher un PA, le PA se propage sur toute la<br />
longueur <strong>de</strong> l’axone sans perte d’amplitu<strong>de</strong>.<br />
La propagation du PA exige une conduction active et<br />
une conduction passive du courant.
Conduction du potentiel <strong>de</strong> membrane<br />
Conduction active
Vitesse <strong>de</strong> déplacement <strong>de</strong> l’influx<br />
~ 3 Km / heure à ~ 300 Km / heure<br />
Vitesse dépend :<br />
• Diamètre <strong>de</strong> la fibre nerveuse : ↑ diamètre ==> ↑ vitesse<br />
• Présence <strong>de</strong> myéline ==> ↑ vitesse
La conduction saltatoire<br />
« Une fibre non myélinisée <strong>de</strong>vrait avoir un calibre <strong>de</strong><br />
plusieurs centimètres pour conduire l'influx à la même<br />
vitesse (100 m/s) qu'une fibre myélinisée <strong>de</strong> 20 micromètres<br />
<strong>de</strong> diamètre. »
dépolarisation<br />
repolarisation<br />
dépolarisation<br />
repolarisation dépolarisation
Loi du tout ou rien<br />
Pour qu’il y ait PA, la dépolarisation au point stimulé doit<br />
dépasser un certain seuil (~ - 50 mV).<br />
• Si la dépolarisation ne dépasse pas le seuil : la membrane<br />
reprend sa polarisation normale et il n ’y a pas d’influx.<br />
• Si la dépolarisation dépasse le seuil ==> la dépolarisation se<br />
poursuit jusqu’à + 40 mV : dépolarisation et repolarisation =<br />
potentiel d’action<br />
==> influx nerveux<br />
• Peu importe l’intensité du stimulus, la dépolarisation ne<br />
dépassera pas + 40 mV
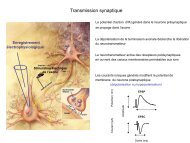
Rôle du Ca 2+ dans la libération <strong>de</strong>s<br />
neurotransmetteurs
Mécanismes moléculaires<br />
• Il existe beaucoup <strong>de</strong><br />
molécules impliquées<br />
dans la libération <strong>de</strong>s<br />
vésicules.<br />
• Trois protéines sont<br />
mieux connues : les<br />
protéines SNARE<br />
(récepteur <strong>de</strong>s<br />
protéines SNAP), la<br />
synaptotagmine et les<br />
canaux Ca 2+ .
Mécanismes moléculaires<br />
• SNAP-25 régule<br />
l’assemblage <strong>de</strong>s <strong>de</strong>ux<br />
SNARE :<br />
– SNARE vésiculaire<br />
(synaptobrevine)<br />
– SNARE membranaire<br />
(syntaxine)
Mécanismes moléculaires<br />
• La vésicule peut<br />
s’accrocher lorsque<br />
les protéines sont<br />
en place.<br />
• SNARES<br />
– Synaptobrevine<br />
– SNAP-25<br />
• Synaptotagmine<br />
• Canaux Ca 2+
Mécanismes moléculaires<br />
• La dépolarisation ouvre les canaux<br />
Ca 2+ VD situés très prêt <strong>de</strong> la<br />
vésicule.
Endocytose médiée par <strong>de</strong>s clathrines
Le modèle du « kiss and run »<br />
Endocytose <strong>de</strong> type “kiss and run” : pas <strong>de</strong> mise en jeu <strong>de</strong>s clathrines
Propagation du signal et exocytose : synthèse