CHAPITRE 1: Notions de thermodynamique - Master 2 en ...
CHAPITRE 1: Notions de thermodynamique - Master 2 en ...
CHAPITRE 1: Notions de thermodynamique - Master 2 en ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
1. Définitions<br />
Gestion <strong>de</strong> l’Energie et Environnem<strong>en</strong>t<br />
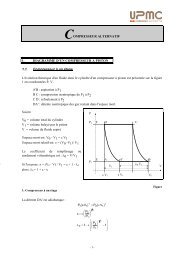
Exemple d’équation d’état : le modèle du gaz parfait<br />
Hypothèses :<br />
• Géométrie <strong>de</strong>s molécules : les atomes ou molécules du gaz sont assimilés à <strong>de</strong>s masses<br />
ponctuelles, <strong>de</strong> dim<strong>en</strong>sion négligeable <strong>de</strong>vant la distance moy<strong>en</strong>ne qui les sépare (gaz<br />
suffisamm<strong>en</strong>t dilué).<br />
• Interaction <strong>de</strong> courte portée : interactions locales <strong>en</strong>tre les molécules, collisions<br />
élastiques. On ne considère que les chocs <strong>en</strong>tre les molécules et les parois du cont<strong>en</strong>ant<br />
(pression).<br />
Chaque atome a une énergie purem<strong>en</strong>t cinétique, on néglige les énergies pot<strong>en</strong>tielles.<br />
• Chaos moléculaire à l’équilibre : les composantes <strong>de</strong>s vecteurs positions et <strong>de</strong>s vecteurs<br />
quantités <strong>de</strong> mouvem<strong>en</strong>t <strong>de</strong>s molécules, suivant trois directions orthogonales, sont<br />
distribuées au hasard.<br />
Répartition uniforme <strong>de</strong>s molécules, isotropie <strong>de</strong>s vitesses, indép<strong>en</strong>dance <strong>de</strong>s<br />
composantes <strong>de</strong> vitesse.<br />
<strong>CHAPITRE</strong> 1: <strong>Notions</strong> <strong>de</strong> <strong>thermodynamique</strong><br />
11