Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Sistem Periodik Unsur<br />
4. SIFAT-SIFAT PERIODIK UNSUR<br />
Walaupun unsur yang berdekatan dalam satu golongan atau periode mempunyai<br />
kemiripan, tetapi diantara sesamanya terdapat perbedaan tertentu. Perbedaan sifat itu berubah<br />
dengan kecenderungan tertentu, sesuai dengan perubahan nomor atomnya. Kecenderungan itu<br />
berulang pada golongan atau periode berikutnya, maka disebut sifat-sifat periodik unsur. Sifatsifat<br />
periodik unsur yang dibahas di sini adalah jari-jari atom, energi ionisasi, afinitas electron,<br />
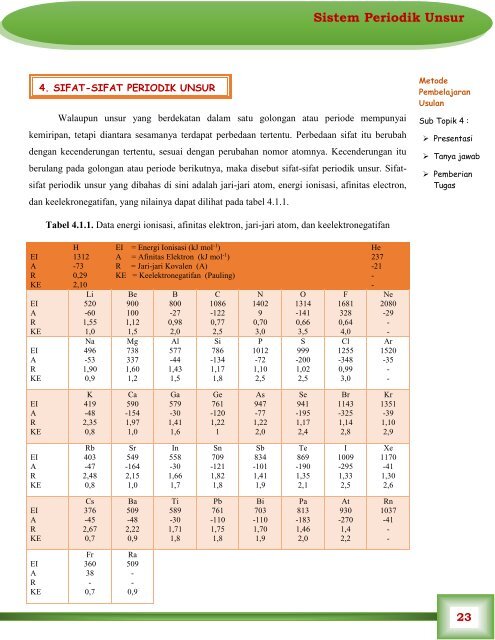
dan keelekronegatifan, yang nilainya dapat dilihat pada tabel 4.1.1.<br />
Tabel 4.1.1. Data energi ionisasi, afinitas elektron, jari-jari atom, dan keelektronegatifan<br />
Metode<br />
Pembelajaran<br />
Usulan<br />
Sub Topik 4 :<br />
‣ Presentasi<br />
‣ Tanya jawab<br />
‣ Pemberian<br />
Tugas<br />
‣<br />
EI<br />
A<br />
R<br />
KE<br />
EI<br />
A<br />
R<br />
KE<br />
EI<br />
A<br />
R<br />
KE<br />
H<br />
1312<br />
-73<br />
0,29<br />
2,10<br />
Li<br />
520<br />
-60<br />
1,55<br />
1,0<br />
Na<br />
496<br />
-53<br />
1,90<br />
0,9<br />
EI = Energi Ionisasi (kJ mol -1 )<br />
A = Afinitas Elektron (kJ mol -1 )<br />
R = Jari-jari Kovalen (A)<br />
KE = Keelektronegatifan (Pauling)<br />
Be<br />
900<br />
100<br />
1,12<br />
1,5<br />
Mg<br />
738<br />
337<br />
1,60<br />
1,2<br />
B<br />
800<br />
-27<br />
0,98<br />
2,0<br />
Al<br />
577<br />
-44<br />
1,43<br />
1,5<br />
C<br />
1086<br />
-122<br />
0,77<br />
2,5<br />
Si<br />
786<br />
-134<br />
1,17<br />
1,8<br />
N<br />
1402<br />
9<br />
0,70<br />
3,0<br />
P<br />
1012<br />
-72<br />
1,10<br />
2,5<br />
O<br />
1314<br />
-141<br />
0,66<br />
3,5<br />
S<br />
999<br />
-200<br />
1,02<br />
2,5<br />
F<br />
1681<br />
328<br />
0,64<br />
4,0<br />
Cl<br />
1255<br />
-348<br />
0,99<br />
3,0<br />
He<br />
237<br />
-21<br />
-<br />
-<br />
Ne<br />
2080<br />
-29<br />
-<br />
-<br />
Ar<br />
1520<br />
-35<br />
-<br />
-<br />
EI<br />
A<br />
R<br />
KE<br />
K<br />
419<br />
-48<br />
2,35<br />
0,8<br />
Ca<br />
590<br />
-154<br />
1,97<br />
1,0<br />
Ga<br />
579<br />
-30<br />
1,41<br />
1,6<br />
Ge<br />
761<br />
-120<br />
1,22<br />
1<br />
As<br />
947<br />
-77<br />
1,22<br />
2,0<br />
Se<br />
941<br />
-195<br />
1,17<br />
2,4<br />
Br<br />
1143<br />
-325<br />
1,14<br />
2,8<br />
Kr<br />
1351<br />
-39<br />
1,10<br />
2,9<br />
EI<br />
A<br />
R<br />
KE<br />
Rb<br />
403<br />
-47<br />
2,48<br />
0,8<br />
Sr<br />
549<br />
-164<br />
2,15<br />
1,0<br />
In<br />
558<br />
-30<br />
1,66<br />
1,7<br />
Sn<br />
709<br />
-121<br />
1,82<br />
1,8<br />
Sb<br />
834<br />
-101<br />
1,41<br />
1,9<br />
Te<br />
869<br />
-190<br />
1,35<br />
2,1<br />
I<br />
1009<br />
-295<br />
1,33<br />
2,5<br />
Xe<br />
1170<br />
-41<br />
1,30<br />
2,6<br />
EI<br />
A<br />
R<br />
KE<br />
Cs<br />
376<br />
-45<br />
2,67<br />
0,7<br />
Ba<br />
509<br />
-48<br />
2,22<br />
0,9<br />
Ti<br />
589<br />
-30<br />
1,71<br />
1,8<br />
Pb<br />
761<br />
-110<br />
1,75<br />
1,8<br />
Bi<br />
703<br />
-110<br />
1,70<br />
1,9<br />
Pa<br />
813<br />
-183<br />
1,46<br />
2,0<br />
At<br />
930<br />
-270<br />
1,4<br />
2,2<br />
Rn<br />
1037<br />
-41<br />
-<br />
-<br />
EI<br />
A<br />
R<br />
KE<br />
Fr<br />
360<br />
38<br />
-<br />
0,7<br />
Ra<br />
509<br />
-<br />
-<br />
0,9<br />
23