MICOBATTERI - Sezione di Microbiologia
MICOBATTERI - Sezione di Microbiologia
MICOBATTERI - Sezione di Microbiologia
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Facoltà <strong>di</strong> Me<strong>di</strong>cina e Chirurgia Università <strong>di</strong> Genova<br />
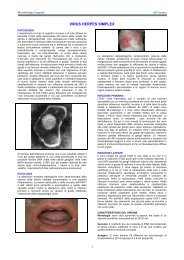
TUBERCOLOSI<br />
<strong>MICOBATTERI</strong><br />
prof. Oliviero E. Varnier<br />
WWW.MICROBIOLOGIA.UNIGE.IT<br />
<strong>Sezione</strong> <strong>di</strong> <strong>Microbiologia</strong> – Dipartimento <strong>di</strong> Scienze Chirurgiche Diagnostiche Integrate (DISC)<br />
2<br />
CLASSIFICAZIONE<br />
CLASSIFICAZIONE<br />
Il genere comprende oltre 100 specie che si presentano come cellule <strong>di</strong><br />
forma bacillare, lunghe dai 2 ai 4 µm e con un <strong>di</strong>ametro tra i 0,3-0,5 µm.<br />
I micobatteri appartengono alla famiglia delle Mycobacteriaceae e sono<br />
inclusi, assieme a corinebatteri, nocar<strong>di</strong>e e ad altri batteri, nell’or<strong>di</strong>ne<br />
degli Actinomycetales.<br />
Del genere Mycobacterium fanno parte importanti patogeni per l’uomo<br />
e gli animali e numerosi batteri ambientali, alcuni dei quali in particolari<br />
circostanze possono causare patologie nell’ospite immunocompromesso.<br />
Storicamente sono sempre stati considerati dei batteri aerobi, tuttavia<br />
recentemente è stata <strong>di</strong>mostrata la presenza <strong>di</strong> una completa batteria <strong>di</strong><br />
enzimi coinvolti nel metabolismo anaerobio e si ritiene quin<strong>di</strong> che possano<br />
essere considerati aerobi/anaerobi facoltativi.<br />
Sono immobili, asporigeni e presentano una caratteristica parete cellulare,<br />
ricca in lipi<strong>di</strong> complessi, polisaccari<strong>di</strong> e glicolipi<strong>di</strong>.<br />
Esternamente alla membrana plasmatica troviamo lo strato <strong>di</strong><br />
peptidoglicano, cui sono legati covalentemente polisaccari<strong>di</strong> a<br />
lunga catena come arabinogalattani, lipoarabinomannani (LAM)<br />
e lipomannani che formano un ponte tra il peptidoglicano e gli aci<strong>di</strong><br />
micolici.<br />
3<br />
4<br />
1
CLASSIFICAZIONE<br />
Figura 23.1 Ultrastruttura <strong>di</strong> Mycobacterium tuberculosis e struttura della parete cellulare.<br />
A. Microfotografi a al microscopio elettronico a trasmissione, con ingran<strong>di</strong>mento della zona<br />
corrispondente alla parete cellulare.<br />
FATTORE<br />
CORDALE<br />
CLASSIFICAZIONE<br />
Gli aci<strong>di</strong> micolici, che costituiscono i principali costituenti della parete<br />
esterna, sono aci<strong>di</strong> grassi a lunga catena (fino a 70 atomi <strong>di</strong> carbonio) la<br />
cui testa polare è rivolta verso la membrana plasmatica, e la porzione<br />
apolare verso l’esterno, dove interagisce con altri glicolipi<strong>di</strong> <strong>di</strong> piccole<br />
<strong>di</strong>mensione che rivestono la parete.<br />
Esternamente alla parete ritroviamo zuccheri che costituiscono una<br />
struttura simil-capsulare, in associazione con lipi<strong>di</strong> e glicolipi<strong>di</strong> che sono<br />
rilasciati dal batterio e che interagiscono <strong>di</strong>rettamente con la cellula.<br />
È stato <strong>di</strong>mostrato che molti componenti della parete cellulare<br />
presentano un’attività biologica essenziale per i micobatteri patogeni umani<br />
come Mycobacterium tuberculosis.<br />
B. Rappresentazione schematica della parete cellulare. MP,<br />
membrana plasmatica; PG, peptidoglicano; AG, arabinogalattano;<br />
ME, membrana esterna; LAM, lipoarabinomannano; AM, aci<strong>di</strong><br />
micolici; TDIM, trealosio <strong>di</strong>micolato (fattore cordale); GL, glicolipi<strong>di</strong>.<br />
5<br />
La parete dei micobatteri è quin<strong>di</strong> costituita da un doppio strato lipi<strong>di</strong>co,<br />
assimmetrico e complesso, che definisce una struttura funzionalmente<br />
simile alla membrana esterna dei batteri gram-negativi.<br />
6<br />
CLASSIFICAZIONE<br />
Le caratteristiche della parete fanno sì che i micobatteri non si colorino<br />
con la colorazione <strong>di</strong> Gram ma me<strong>di</strong>ante la colorazione Ziehl-Nielsen,<br />
che evidenzia le proprietà tintoriali note come acido-alcol resistenza.<br />
Tale proprietà consiste nella capacità dei batteri <strong>di</strong> trattenere, una volta<br />
colorati con carbolfucsina, la colorazione rossa anche quando<br />
sottoposti a trattamenti decoloranti energici con aci<strong>di</strong> e alcol.<br />
CLASSIFICAZIONE<br />
I micobatteri vengono sud<strong>di</strong>visi in due gran<strong>di</strong> gruppi: a lenta e a rapida<br />
crescita (tab. 23.1).<br />
I micobatteri a lenta crescita comprendono numerose specie <strong>di</strong> interesse<br />
nella patologia umana e animale e tra queste le più importanti sono: M.<br />
tuberculosis, M. leprae e M. ulcerans.<br />
Alcune specie possono causare infezioni croniche granulomatose nell’ospite<br />
immunocompetente, mentre l’ospite immunodepresso è esposto alla possibilità<br />
<strong>di</strong> infezioni <strong>di</strong>sseminate da parte <strong>di</strong> molti micobatteri, che si comportano da<br />
opportunisti.<br />
Le specie più frequentemente isolate sono: da M. avium intracellulare (MAI)<br />
complex.<br />
I micobatteri a rapida crescita comprendono specie prevalentemente<br />
ambientali e non <strong>di</strong> interesse per la patologia umana, sebbene alcuni <strong>di</strong><br />
esse possano raramente causare patologia nell’uomo:<br />
È il caso <strong>di</strong>: M. chelone, che può causare infezioni polmonari croniche; M.<br />
fortuitum e M. abscessus, che possono causare infezione dei tessuti molli o<br />
infezioni <strong>di</strong>sseminate nell’ospite immunocompromesso.<br />
7<br />
8<br />
2
Tab 23.1 Micobatteri non tubercolari che possono essere isolati da<br />
campioni clinici<br />
MYCOBACTERIUM TUBERCULOSIS<br />
Mycobacterium tuberculosis è l’agente eziologico della tubercolosi (TB),<br />
un’antica malattia polmonare cronica che ha accompagnato la storia<br />
dell’uomo negli ultimi millenni.<br />
Numerosi reperti archeologici come scheletri <strong>di</strong> oltre 8000 anni fa e<br />
mummie degli Egizi e Inca hanno evidenziato lesioni ossee compatibili con<br />
l’infezione tubercolare.<br />
Nel corso dei secoli la TB è stata una minaccia costante per l’uomo, in<br />
particolare nelle aree urbane e densamente popolate, dove si sono verificati<br />
frequenti fenomeni epidemici responsabili della attuale pandemia.<br />
M. tuberculosis appartiene al gruppo Mycobacterium tuberculosis<br />
complex (MTBC), <strong>di</strong> cui fanno parte M. canettii, M. africanum, M. microti<br />
e M. bovis. Per l’elevata omologia nucleoti<strong>di</strong>ca. il gruppo MTBC oggi è<br />
considerato come singola specie e i suoi componenti come subspecie.<br />
M. tuberculosis, M. canetti e M. africanum sono gli agenti eziologici della TB<br />
nell’uomo.<br />
9<br />
10<br />
MYCOBACTERIUM TUBERCULOSIS<br />
M. bovis è l’agente eziologico della TB negli animali e ha uno spettro<br />
d’ospite molto ampio, potendo infettare bovini, antilopi, foche, elefanti, leoni<br />
ecc. Raramente causa patologia nell’uomo, che si infetta assumendo<br />
alimenti contaminati, come il latte <strong>di</strong> bovini infetti.<br />
M. microti è l’agente eziologico della TB nei ro<strong>di</strong>tori e non è patogeno per<br />
l’uomo.<br />
Nel 1998 è stato completato il sequenziamento del genoma <strong>di</strong> M.<br />
tuberculosis H37Rv. Il genoma è costituito da 4 411 529 bp e<br />
co<strong>di</strong>fica per 3986 proteine.<br />
Più recentemente è stato completato il genoma <strong>di</strong> un ceppo clinico <strong>di</strong> M.<br />
tuberculosis (ceppo CDC1551) e quello <strong>di</strong> un ceppo <strong>di</strong> M. bovis.<br />
Nel complesso è stato osservato che M. tuberculosis presenta:<br />
un maggior numero <strong>di</strong> geni rispetto a quanto osservato per altri batteri patogeni,<br />
un metabolismo più complesso <strong>di</strong> quanto fosse possibile ritenere in passato<br />
e può essere considerato:<br />
una specie geneticamente stabile con poca variabilità genetica.<br />
11<br />
MYCOBACTERIUM TUBERCULOSIS<br />
Analisi <strong>di</strong> genomica comparativa tra vari ceppi <strong>di</strong> MTBC hanno<br />
permesso <strong>di</strong> in<strong>di</strong>viduare regioni in cui maggiori sono le <strong>di</strong>fferenze<br />
tra questi e <strong>di</strong> definire in modo corretto i rapporti genetici e quin<strong>di</strong><br />
evolutivi tra le varie specie e/o sottospecie.<br />
È stato possibile costruire un albero genealogico all’interno <strong>di</strong> MTBC<br />
e <strong>di</strong> <strong>di</strong>mostrare come le varie subspecie si siano evolute attraverso<br />
un processo <strong>di</strong> DELEZIONE GENICA, in cui frammenti <strong>di</strong> genoma<br />
anche <strong>di</strong> <strong>di</strong>verse decine <strong>di</strong> kb SONO STATI PERSI.<br />
12<br />
3
MYCOBACTERIUM TUBERCULOSIS<br />
EPIDEMIOLOGIA<br />
È interessante notare come questo processo abbia avuto un effetto<br />
sull’adattamento all’ospite/i mammifero.<br />
Ad esempio, le tre subspecie che causano la TB nell’uomo, M. tuberculosis,<br />
M. africanum e M. canettii, raramente o mai infettano gli animali.<br />
M. microti è l’agente eziologico della TB nei ro<strong>di</strong>tori <strong>di</strong> campagna, ma è<br />
assolutamente avirulento per l’uomo.<br />
È interessante osservare inoltre come M. microti abbia perso per delezione<br />
genica un frammento <strong>di</strong> genoma simile a quello responsabile della per<strong>di</strong>ta <strong>di</strong><br />
virulenza del ceppo BCG.<br />
M. bovis presenta il maggior numero <strong>di</strong> delezioni geniche e<br />
paradossalmente presenta il più ampio spettro d’ospite.<br />
Si stima che la TB uccida ogni giorno circa 5000 persone.<br />
L’OMS in<strong>di</strong>ca<br />
circa 1,5-2 milioni il numero <strong>di</strong> decessi all’anno,<br />
8-10 milioni il numero <strong>di</strong> nuovi casi e<br />
circa 30 milioni il numero <strong>di</strong> pazienti con TB attiva.<br />
Il 95% dei casi si registra nei Paesi in via <strong>di</strong> sviluppo: Africa sub-sahariana e<br />
alcuni Paesi del Sud-Est asiatico, dove l’incidenza della malattia è<br />
nell’or<strong>di</strong>ne dei 100-500/100.000 abitanti.<br />
in questi Paesi la TB rappresenta un drammatico problema sanitario, sociale<br />
ed economico.<br />
Le nuove migrazioni, l’avvento dell’AIDS, la comparsa <strong>di</strong> nuove povertà<br />
hanno determinato un riemergere dell’infezione anche nei paesi<br />
industrializzati.<br />
Per tali motivi l’OMS ha <strong>di</strong>chiarato nel 1993 la TB emergenza globale.<br />
13<br />
14<br />
QUIZ N° 41042<br />
Si stima che la TB uccida ogni giorno circa 5000 persone.<br />
L’Organizzazione Mon<strong>di</strong>ale della Sanità (OMS) in<strong>di</strong>ca in circa 1,5-2<br />
milioni il numero <strong>di</strong> decessi all’anno, in 8-10 milioni il numero <strong>di</strong> nuovi<br />
casi e in circa 30 milioni il numero <strong>di</strong> pazienti con TB attiva. Il 95% dei<br />
casi si registra nei Paesi in via <strong>di</strong> sviluppo, in particolare nell’Africa subsahariana<br />
e alcuni Paesi del Sud-Est asiatico, dove l’incidenza della<br />
malattia è nell’or<strong>di</strong>ne dei 100-500/100.000 abitanti.<br />
QUALE È L’EPIDEMIOLOGIA DELLA TUBERCOLOSI NEL MONDO<br />
15 16<br />
4
QUIZ N° 41043<br />
QUIZ N° 41045<br />
Le nuove migrazioni, l’avvento della sindrome da immuno<br />
deficienza acquisita (AIDS), la comparsa <strong>di</strong> nuove povertà hanno<br />
determinato un riemergere dell’infezione anche nei paesi sviluppati<br />
In Italia …La situazione è ancora sotto controllo (incidenza 5-<br />
10/100 000 abitanti) e si stima che circa la metà dei pazienti con<br />
TB sia rappresentata da emigrati provenienti da regioni ad alta<br />
endemia <strong>di</strong> TB.<br />
PER QUALI MOTIVI L’OMS HA DICHIARATO NEL 1993 LA TB<br />
EMERGENZA GLOBALE<br />
QUALE È L’EPIDEMIOLOGIA DELLA TUBERCOLOSI IN<br />
ITALIA<br />
17<br />
18<br />
Malattie Frequenti<br />
CARATTERISTICHE GENERALI<br />
Mycobacterium tuberculosis è senza dubbio uno dei più antichi,<br />
complessi ed evoluti agenti infettivi per l’uomo, e ha sviluppato nel corso<br />
dell’evoluzione sofisticati meccanismi per evadere la risposta<br />
immunita ria dell’ospite o per trarre vantaggio dalla stessa.<br />
Una delle principali caratteristiche <strong>di</strong> M. tuberculosis è la sua capacità<br />
<strong>di</strong>:<br />
resistere all’azione battericida dei macrofagi, me<strong>di</strong>ante un meccanismo<br />
che prevede l’inibizione della fusione lisosoma-fagosoma.<br />
Il micobatterio rimane così in un vacuolo non aci<strong>di</strong>ficato, in cui sono assenti<br />
gli enzimi e molecole ad azione microbicida e dove il micobatterio è in grado<br />
<strong>di</strong> replicarsi attivamente.<br />
19<br />
20<br />
5
Figura 23.2. Analisi microscopica <strong>di</strong> tessuto polmonare isolato da un topo<br />
infettato Sperimentalmente con Mycobacterium tuberculosis<br />
FATTORI <strong>di</strong> VIRULENZA<br />
Non sono stati ancora identificati le proteine e i fattori <strong>di</strong> virulenza <strong>di</strong><br />
M. tuberculosis, sebbene si ipotizzi un <strong>di</strong>retto coinvolgimento delle<br />
proteine co<strong>di</strong>ficate dalla regione <strong>di</strong> <strong>di</strong>fferenza 1 (RD1).<br />
La regione RD1 è un frammento <strong>di</strong> genoma <strong>di</strong> 10,7 kb che co<strong>di</strong>fica per<br />
numerosi geni, tra cui in particolare Esat-6 e cfp10.<br />
Tale regione è assente nel ceppo vaccinico M. bovis BCG ed è stato<br />
<strong>di</strong>mostrato come l’attenuazione <strong>di</strong> quest’ultimo sia dovuta all’assenza <strong>di</strong><br />
RD1. Infatti l’inserimento della regione RD1 nel genoma <strong>di</strong> BCG ha come<br />
risultato un aumento della virulenza del ceppo BCG ricombinante.<br />
A. Infiltrato cellulare che si organizza in granuloma. I micobatteri risiedono prevalentemente<br />
nella parte centrale del granuloma, all’interno <strong>di</strong> macrofagi “schiuomosi”. B. Macrofagi infettati<br />
con M. tuberculosis.<br />
la proteina ESAT-6, co<strong>di</strong>ficata dalla regione RD1, potrebbe indurre la<br />
formazione <strong>di</strong> pori nelle membrane dei vacuoli del macrofago in cui il<br />
micobatterio si moltiplica.<br />
La regione che co<strong>di</strong>fica per ESAT-6 e CFP10 comprende anche altre<br />
proteine che costituiscono l’apparato secretorio.<br />
21<br />
22<br />
FATTORI <strong>di</strong> VIRULENZA<br />
La secrezione <strong>di</strong> proteine e antigeni attraverso la membrana<br />
rappresenta un potente ed efficace sistema per interferire con i<br />
meccanismi <strong>di</strong> <strong>di</strong>fesa dell’ospite.<br />
Anche per M. tuberculosis questo meccanismo promuove l’azione<br />
patogena e assicura la moltiplicazione nei tessuti dell’ospite.<br />
Oltre ai sistemi <strong>di</strong> secrezione delle proteine ESAT-6 e CFP10, M.<br />
tuberculosis presenta altri sistemi <strong>di</strong> secrezione come il Sec e il TAT.<br />
Il sistema Sec è coinvolto nella secrezione della superossido <strong>di</strong>smutasi, un<br />
enzima che consente al micobatterio <strong>di</strong> rendere meno battericida l’ambiente<br />
all’interno del fagolisosoma. Ceppi <strong>di</strong> M. tuberculosis in cui il Sec è stato<br />
inattivato geneticamente risultano essere fortemente attenuati.<br />
I sistemi <strong>di</strong> secrezione finora caratterizzati me<strong>di</strong>ano il trasporto delle proteine<br />
attraverso la membrana plasmatica.<br />
È noto che componenti non proteiche della parete cellulare <strong>di</strong> M.<br />
tuberculosis intervengono nel meccanismo <strong>di</strong> patogenicità e tra questi un ruolo<br />
importante viene svolto dagli aci<strong>di</strong> micolici che sono delle complesse strutture<br />
molecolari <strong>di</strong> aci<strong>di</strong> grassi a lunga catena. Gli aci<strong>di</strong> micolici più semplici sono<br />
costituiti da due catene, una lunga fino a 60 atomi <strong>di</strong> carbonio (<strong>di</strong>stale) e una<br />
più corta (prossimale). Esistono cinque tipi <strong>di</strong> aci<strong>di</strong> micolici.<br />
23<br />
PATOGENESI<br />
Gli aci<strong>di</strong> micolici possono essere organizzati in strutture complesse<br />
quando legati covalentemente con arabinogalattani o altri zuccheri.<br />
Il trealosio <strong>di</strong>micolato (TDIM), anche noto come FATTORE CORDALE, è<br />
uno dei più importanti ed esercita una potente azione biologica.<br />
Presenta un’attività immunostimolatoria, stimola la secrezione <strong>di</strong> citochine ed<br />
è strettamente coinvolto nel meccanismo <strong>di</strong> patogenesi che sfocia con il danno<br />
tissutale tipico della TB.<br />
È coinvolto nella protezione da stress ambientali, contribuisce alla bassa<br />
permeabilità della parete cellulare che conferisce una naturale resistenza ai<br />
farmaci ed è coinvolto nella protezione dagli stress ossidativi e nella<br />
persistenza nei tessuti dell’ospite immunocompetente.<br />
La porzione esterna della parete è ricca in glicolipi<strong>di</strong> complessi e fenolici,<br />
che sono delle cere non polari rilasciate dalla cellula e svolgono una importante<br />
azione biologica<br />
24<br />
6
RAPPORTO OSPITE-PARASSITA<br />
L’interazione dei micobatteri con il sistema immunitario innato e<br />
acquisito, gioca un ruolo fondamentale nel rapporto ospite-parassita.<br />
Alcuni componenti <strong>di</strong> parete interagiscono con recettori presenti sulla<br />
superficie delle cellule del sistema immunitario, tra cui in particolare i<br />
recettori Toll-like (TLR). È stato <strong>di</strong>mostrato ad esempio che il LAM<br />
interagisce con il TLR2, così come alcune proteine <strong>di</strong> parete.<br />
è stato possibile <strong>di</strong>mostrare l’induzione <strong>di</strong> apoptosi, che consente al<br />
micobatterio <strong>di</strong> evadere la risposta dell’ospite o <strong>di</strong> modulare l’intensità<br />
della risposta immunitaria.<br />
M. tuberculosis induce una intensa risposta cellulare specifica <strong>di</strong>retta<br />
verso gli antigeni secreti dal micobatterio durante le prima fasi dell’infezione.<br />
Ad esempio, le proteine Esat-6 e CFP10 sono due tra gli antigeni più<br />
immunogenici <strong>di</strong> M. tuberculosis, tanto da essere utilizzati come base per<br />
la <strong>di</strong>agnosi in<strong>di</strong>retta <strong>di</strong> infezione da M. tuberculosis.<br />
RISPOSTA IMMUNITARIA<br />
La caratterizzazione immunologica della risposta immunitaria che si<br />
sviluppa in risposta all’infezione da M. tuberculosis è piuttosto complessa.<br />
La risposta cellulare è caratterizzata dalla presenza <strong>di</strong> linfociti CD4, che<br />
secernono citochine pro-infiammatorie (IFN-γ) e da linfociti CD8 ad azione<br />
citotossica.<br />
Non è stato possibile ad oggi evidenziare dei correlati immunologici <strong>di</strong><br />
protezione, vale a <strong>di</strong>re un tipo <strong>di</strong> risposta immunitaria specifica correlabile<br />
con il controllo dell’infezione.<br />
L’assenza <strong>di</strong> tali informazioni rende ancora più <strong>di</strong>fficile lo sviluppo <strong>di</strong> un<br />
nuovo vaccino contro la TB.<br />
25<br />
26<br />
PATOGENESI<br />
Mycobacterium tuberculosis si trasmette per via aerea da un paziente malato con<br />
TB polmonare attiva e aperta e si ritiene siano sufficienti pochi batteri per iniziare<br />
infettato il ciclo patogenetico <strong>di</strong> infezione nel nuovo paziente.<br />
Il bacillo, una volta raggiunto lo spazio alveolare, viene fagocitato dai macrofagi<br />
alveolari, dove può essere rapidamente ucciso oppure può resistere a tale azione<br />
microbicida. Nel primo caso l’infezione non ha luogo e l’ospite non matura alcuna<br />
risposta immunitaria specifica.<br />
PATOGENESI<br />
Quando viceversa i bacilli resistono all’azione mi<br />
crobicida dei macrofagi, si ha moltiplicazione atti<br />
va all’interno del macrofago e i micobatteri possono<br />
infettare anche altri fagociti e cellule epiteliali pre<br />
senti in prossimità del sito <strong>di</strong> infezione.<br />
Durante questa fase i batteri possono <strong>di</strong>sseminarsi<br />
e raggiungere attraverso il sangue qualsiasi tessuto<br />
e organo.<br />
Alveolo 27<br />
28<br />
7
PATOGENESI<br />
La moltiplicazione batterica richiama<br />
cellule del sistema immunitario che<br />
iniziano a infiltrarsi e a organizzare il<br />
tipico granuloma attorno al sito <strong>di</strong><br />
infezione primaria.<br />
La presenza <strong>di</strong> leucociti e la secrezione<br />
<strong>di</strong> citochine e chemochine ad azione<br />
infiammatoria inducono la comparsa<br />
della tipica necrosi caseosa.<br />
Nel 90-95% dei casi la risposta<br />
dell’ospite è in grado <strong>di</strong> circoscrivere e<br />
controllare l’infezione e nell’ospite per<br />
mane soltanto una lesione nel sito <strong>di</strong><br />
infezione primaria che prende il nome <strong>di</strong><br />
complesso primario<br />
PATOGENESI<br />
In questi soggetti il bacillo non viene completamente ucciso ma permane<br />
in una fase <strong>di</strong> latenza.<br />
Si stabilisce un equilibrio tra M. tuberculosis e il sistema immunitario<br />
dell’ospite, in cui da un lato si impe<strong>di</strong>sce la moltiplicazione incontrollata<br />
del bacillo e dall’altro il bacillo è in grado <strong>di</strong> resistere all’azione<br />
microbicida del sistema immunitario.<br />
Tale con<strong>di</strong>zione è evidenziata dalla presenza <strong>di</strong> una intensa risposta<br />
cellulo-me<strong>di</strong>ata nei confronti degli antigeni <strong>di</strong> M. tuberculosis,<br />
classicamente evidenziata dalla reazione della tubercolina (Mantoux).<br />
29<br />
30<br />
PATOGENESI<br />
La fase <strong>di</strong> latenza, clinicamente asintomatica,<br />
può perdurare anche per decenni e può sfociare<br />
in circa il 5-10% dei casi in una riattivazione<br />
dell’infezione con comparsa <strong>di</strong> TB attiva.<br />
In questi casi, così come quando l’infezione<br />
primaria non viene controllata, il bacillo si replica<br />
attivamente e la risposta dell’ospite non solo<br />
non è in grado <strong>di</strong> controllare l’infezione ma è<br />
responsabile del danno tissutale tipicamente<br />
associato alla TB (immunopatologia).<br />
PATOGENESI<br />
La moltiplicazione del batterio richiama cellule del sistema immunitario, che<br />
me<strong>di</strong>ante la secrezione <strong>di</strong> chemochine e citochine inducono uno stato infi<br />
ammatorio che causa una necrosi caseosa e danno tissutale che sfocia<br />
nella comparsa delle tipiche caverne presenti a livello del parenchima<br />
polmonare: questa è la classica forma <strong>di</strong> TB polmonare, clinicamente<br />
evidente e che rappresenta la forma contagiosa dell’infezione.<br />
31<br />
32<br />
8
PATOGENESI<br />
Sebbene nella maggior parte dei casi la TB attiva si presenti a livello<br />
polmonare, pressoché tutti gli organi possono essere colpiti (reni, ossa,<br />
linfono<strong>di</strong>, cute ecc.) e in questi casi si assiste alla comparsa <strong>di</strong> strutture<br />
granulomatose che sono poi responsabili del danno tissutale e quin<strong>di</strong> della<br />
comparsa della patologia.<br />
Nei neonati o in soggetti con deficit immunitari importanti si può assistere<br />
a una moltiplicazione incontrollata del bacillo, con comparsa <strong>di</strong> una infezione<br />
<strong>di</strong>sseminata (ad esempio TB miliare) che può anche evolvere in meningite<br />
tubercolare. In questi casi, in assenza <strong>di</strong> un opportuno trattamento,<br />
l’evoluzione della malattia può essere rapida e ad esito infausto.<br />
VACCINO BCG:IL BACILLO DI CALMETTE E GUÉRIN<br />
Il bacillo <strong>di</strong> Calmette e Guérin (BCG) è ancora oggi l’unico vaccino<br />
<strong>di</strong>sponibile contro la TB.<br />
Il BCG è un vaccino vivo attenuato, ottenuto da Calmette e Guérin<br />
me<strong>di</strong>ante passaggi seriali in terreno <strong>di</strong> patata biliata a partire da un ceppo<br />
virulento <strong>di</strong> M. bovis.<br />
Durante il processo <strong>di</strong> attenuazione, il ceppo BCG ha perso numerosi<br />
frammenti <strong>di</strong> genoma, che prendono il nome <strong>di</strong> regioni <strong>di</strong> <strong>di</strong>fferenza (RD).<br />
Poiché il passaggio dei ceppi è avvenuto anche dopo l’isolamento del<br />
ceppo vaccinico da Calmette e Guérin, si è assistito alla per<strong>di</strong>ta <strong>di</strong><br />
frammenti <strong>di</strong> genoma anche in epoche successive, tanto che oggi si<br />
conoscono ceppi <strong>di</strong>versi <strong>di</strong> BCG, che normalmente prendono il nome<br />
dalle case farmaceutiche che li producono, i quali presentano un <strong>di</strong>verso<br />
pattern <strong>di</strong> RD.<br />
La più importante delle regioni RD è la RD1, che contiene una regione del<br />
genoma che co<strong>di</strong>fica per i geni Esat-6 e cfp10, e più in generale per il<br />
cluster genico ESX1:<br />
RD1 è essenziale per la virulenza <strong>di</strong> M. tuberculosis.<br />
33<br />
34<br />
VACCINO<br />
VACCINO<br />
A partire dal 1921, anno della prima immunizzazione con BCG, sono<br />
state somministrate in tutto il mondo centinaia <strong>di</strong> milioni <strong>di</strong> dosi <strong>di</strong><br />
BCG.<br />
Il vaccino BCG si somministra subito dopo la nascita per via<br />
sottocutanea e dopo un mese si verifica l’avvenuta immunizzazione<br />
me<strong>di</strong>ante il test della tubercolina.<br />
Nel corso del secolo scorso è stato possibile evidenziare pregi e <strong>di</strong>fetti<br />
del vaccino. Il vaccino si è <strong>di</strong>mostrato sostanzialmente sicuro e il basso<br />
costo ha reso possibile l’attuazione <strong>di</strong> procedure <strong>di</strong> immunizzazione<br />
anche nei paesi più poveri.<br />
Il vaccino BCG si è inoltre <strong>di</strong>mostrato effi cace nel prevenire le forme,<br />
spesso fatali, <strong>di</strong> TB <strong>di</strong>sseminata (miliare) e <strong>di</strong> meningite tubercolare<br />
nei bambini.<br />
Stu<strong>di</strong> in paesi ad alta endemia <strong>di</strong> TB hanno <strong>di</strong>mostrato come l’efficacia <strong>di</strong><br />
BCG nel prevenire le forme <strong>di</strong> TB attiva sia scarsa e spesso quasi zero<br />
l’interferenza <strong>di</strong> micobatteri ambientali con lo sviluppo <strong>di</strong> una risposta<br />
immunitaria, che potrebbe essere responsabile dello svanire col tempo della<br />
risposta immunitaria indotta dal vaccino e dell’inefficacia <strong>di</strong> strategie <strong>di</strong> richiamo<br />
(boosting);<br />
BCG, ceppo attenuato ma vitale, non dovrebbe essere somministrato per ragioni<br />
<strong>di</strong> sicurezza nei soggetti con infezione da HIV, che come noto rappresentano una<br />
popolazione particolarmente a rischio per lo sviluppo della TB.<br />
Poiché le persone vaccinate con BCG sviluppano una positività alla<br />
tubercolina, questo test non può essere efficacemente utilizzato, in una<br />
popolazione vaccinata, per valutare la prevalenza dell’infezione in una data<br />
comunità o in<strong>di</strong>viduare i contatti (persone che, vivendo a contatto con un<br />
soggetto cui è stata <strong>di</strong>agnosticata una TB attiva, sono state infettate da M.<br />
tuberculosis).<br />
Questi aspetti limitano fortemente la vali<strong>di</strong>tà del test della tubercolina come<br />
strumento <strong>di</strong> <strong>di</strong>agnosi immunologica.<br />
35<br />
36<br />
9
NUOVI VACCINI<br />
HOSPITAL ALLI CAUSAI<br />
Negli ultimi anni, anche grazie a un rinnovato investimento nella<br />
ricerca sulla TB, abbiamo assistito allo sviluppo <strong>di</strong> nuovi vaccini<br />
sperimentali.<br />
Sono state implementate <strong>di</strong>verse strategie <strong>di</strong> vaccinazione:<br />
vaccini a subunità, costituiti da due o più antigeni ricombinanti e purifi<br />
cati <strong>di</strong> M. tuberculosis, somministrati con sostanze a<strong>di</strong>uvanti;<br />
ceppi <strong>di</strong> Vaccinia virus ricombinanti che esprimono antigeni dominanti<br />
<strong>di</strong> M. tuberculosis;<br />
ceppi <strong>di</strong> BCG ricombinanti che iperesprimono antigeni dominanti o che<br />
sono stati mo<strong>di</strong>fi cati per renderli più immunogenici.<br />
I risultati ottenuti con alcuni <strong>di</strong> questi vaccini sono buoni in modelli<br />
preclinici animali e si spera che gli stu<strong>di</strong> clinici possano a breve<br />
fornire una valida alternativa al vaccino BCG.<br />
37<br />
38<br />
DIAGNOSI<br />
PROMOZIONE E ASSISTENZA COMUNITARIA<br />
La <strong>di</strong>agnosi <strong>di</strong> infezione da M. tuberculosis, così come per gli altri<br />
agenti <strong>di</strong> infezione, viene classicamente <strong>di</strong>stinta in <strong>di</strong>agnosi<br />
microbiologica o <strong>di</strong>retta e in <strong>di</strong>agnosi immunologica o in<strong>di</strong>retta.<br />
La prima viene utilizzata per evidenziare soggetti con TB attiva,<br />
mentre la seconda viene utilizzata per evidenziare i soggetti infettati<br />
con M. tuberculosis, ma non è in grado <strong>di</strong> <strong>di</strong>stinguere tra soggetti<br />
sani (infezione latente) e soggetti malati (infezione attiva).<br />
39<br />
40<br />
10
RISULTATI TB<br />
DIAGNOSI DIRETTA<br />
15 comunitá sotto controllo<br />
2400 persone monitorate<br />
2169 PPD (Mantoux) letti<br />
408 Bacilloscopie realizzate<br />
380 Colture Lowenstein realizzate<br />
21 Pazienti tratatti<br />
CAMPIONI: la <strong>di</strong>agnosi microbiologica si basa normalmente sulla ricerca <strong>di</strong> M.<br />
tuberculosis nel campione biologico (espettorato, lavaggio bronco alveolare,<br />
urine, linfonodo ecc.).<br />
DECONTAMINAZIONE: i campioni biologici polimicrobici, quali ad esempio<br />
espettorati, devono essere decontaminati me<strong>di</strong>ante trattamento con soluzioni<br />
contenenti idrossido <strong>di</strong> so<strong>di</strong>o, cui il bacillo è resistente, per eliminare la flora<br />
microbica presente e concentrati per incrementare le possibilità <strong>di</strong> isolare il<br />
bacillo.<br />
PAUCIBACILLARE: è infatti importante ricordare che pazienti con TB attiva<br />
possono eliminare anche solo pochi bacilli, che moltiplicandosi molto lentamente<br />
nei terreni <strong>di</strong> coltura, verrebbero rapidamente sopraffatti dalla presenza <strong>di</strong> altri<br />
batteri nel campione biologico. Anche per tali motivi, la <strong>di</strong>agnosi microbiologica<br />
viene normalmente eseguita, laddove possibile, su almeno tre campioni<br />
consecutivi <strong>di</strong> espettora to e sulle urine del mattino raccolte per tre giorni<br />
consecutivi.<br />
41<br />
42<br />
DIAGNOSI DIRETTA: ESAME MICROSCOPICO<br />
Il campione viene analizzat0 al microscopio previa colorazione con Ziehl-Nielsen. La<br />
presenza <strong>di</strong> batteri AAR è in<strong>di</strong>cativa <strong>di</strong> una infezione attiva causata da micobatteri<br />
patogeni, sebbene sia necessario identificare i micobatteri e <strong>di</strong>stinguerli da altri<br />
batteri acido-alcol resistenti (actinomiceti, nocar<strong>di</strong>e).<br />
I micobatteri si presentano al microscopio come dei bacilli rossi su sfondo blu,<br />
allungati (A) e nel caso <strong>di</strong> M. tuberculosis spesso organizzati in piccoli gruppi <strong>di</strong> 3-10<br />
bacilli (aggregati, B).<br />
L’analisi microscopica presenta importanti vantaggi: 1) semplicità, 2) rapi<strong>di</strong>tà <strong>di</strong><br />
esecuzione, 3) il basso costo e 4) permette <strong>di</strong> evidenziare i soggetti contagiosi. È<br />
stato calcolato che nei Paesi ad alta endemia <strong>di</strong> TB, l’analisi microscopica consenta<br />
<strong>di</strong> evidenziare circa il 60% dei pazienti con TB attiva.<br />
DIAGNOSI DIRETTA: ESAME COLTURALE<br />
Il metodo <strong>di</strong>agnostico più sensibile è rappresentato dalla coltura. Per tali<br />
motivi, nei laboratori opportunamente attrezzati, una seconda aliquota <strong>di</strong><br />
campione viene utilizzata per allestire le colture.<br />
Si procede normalmente all’inoculo <strong>di</strong> un terreno solido (Lowestein-<br />
Jensen), costituito da tuorlo d’uovo, glicerolo e verde <strong>di</strong> malachite come<br />
inibitore della crescita <strong>di</strong> altri batteri (B).<br />
La crescita dei micobatteri e in particolare <strong>di</strong> M. tuberculosis è molto lenta, e<br />
possono essere necessari fino a 45 giorni <strong>di</strong> incubazione prima <strong>di</strong><br />
evidenziare colonie nel terreno (D).<br />
43<br />
44<br />
11
DIAGNOSI DIRETTA: AUTOMAZIONE E IDENTIFICAZIONE<br />
Al fine <strong>di</strong> evidenziare più rapidamente i micobatteri in coltura, sono stati<br />
sviluppati dei sistemi automatizzati costituiti da terreni liqui<strong>di</strong>, in grado <strong>di</strong><br />
evidenziare la crescita dei micobatteri me<strong>di</strong>ante la misurazione del<br />
consumo <strong>di</strong> ossigeno o <strong>di</strong> altri metaboliti come ad esempio aci<strong>di</strong> grassi<br />
marcati ra<strong>di</strong>oattivamente (14C). L’utilizzo <strong>di</strong> tali sistemi <strong>di</strong> coltura ha<br />
permesso <strong>di</strong> ridurre significativamente il tempo necessario per isolare in<br />
coltura i micobatteri (20-30 giorni).<br />
Una volta che la coltura evidenzia la presenza <strong>di</strong> micobatteri, è importante<br />
procedere all’identificazione. In passato venivano utilizzate numerose<br />
reazioni per identifi care la specie <strong>di</strong> micobatterio isolata.<br />
Recentemente, l’utilizzo delle tecniche <strong>di</strong> <strong>di</strong>agnosi e identificazione<br />
molecolare ha reso queste tecniche obsolete.<br />
DIAGNOSI MOLECOLARE<br />
La <strong>di</strong>agnosi molecolare <strong>di</strong> infezione da M. tuberculosis o da micobatteri è<br />
oggi uno strumento <strong>di</strong> grande utilità, che consente <strong>di</strong> <strong>di</strong>agnosticare<br />
rapidamente (< 24 ore) e con elevata specificità e sensibilità la presenza <strong>di</strong><br />
micobatteri nei campioni biologici.<br />
La <strong>di</strong>agnosi molecolare può essere eseguita <strong>di</strong>rettamente nel campione<br />
biologico o nella colonia isolata in coltura. Nel primo caso si ricerca<br />
normalmente M. tuberculosis, che è <strong>di</strong> gran lunga il principale micobatterio<br />
<strong>di</strong> interesse nella patologia umana, me<strong>di</strong>ante tecniche <strong>di</strong> amplificazione<br />
genica che ricercano sequenze <strong>di</strong> DNA specifiche per M. tuberculosis. La<br />
specificità <strong>di</strong> tali sistemi <strong>di</strong>agnostici è molto elevata, e così pure la<br />
sensibilità che consente <strong>di</strong> in<strong>di</strong>viduare fi no a 10-50 batteri per campione.<br />
L’identificazione molecolare può essere eseguita amplificando delle sequenze <strong>di</strong><br />
DNA con<strong>di</strong>vise tra i micobatteri (ad esempio un frammento <strong>di</strong> DNA che co<strong>di</strong>fica<br />
per la proteina HSP65 o per l’rRNA 16S) e procedere successivamente al<br />
sequenziamento della suddetta regione.<br />
Nei paesi in via <strong>di</strong> sviluppo l’analisi microscopica dell’espettorato rappresenta<br />
spesso l’unico strumento per fare <strong>di</strong>agnosi <strong>di</strong> TB.<br />
45<br />
46<br />
Diagnosi in<strong>di</strong>retta<br />
Diagnostica<br />
La <strong>di</strong>agnosi in<strong>di</strong>retta si basava sulla <strong>di</strong>mostrazione <strong>di</strong> una risposta<br />
immunitaria specifica dell’ospite nei confronti <strong>di</strong> antigeni <strong>di</strong> M.<br />
tuberculosis. La reazione alla tubercolina consiste nell’inoculo per via<br />
intradermica <strong>di</strong> un preparato proteico purificato <strong>di</strong> M. tuberculosis (PPD).<br />
Dopo 48-72 ore nei soggetti infettati con M. tuberculosis si assiste alla<br />
comparsa <strong>di</strong> una reazione <strong>di</strong> ipersensibilità ritardata, visibile per la<br />
comparsa <strong>di</strong> una papula eritematosa, che in alcuni casi può andare<br />
incontro a necrosi. Una reazione si definisce positiva quando il <strong>di</strong>ametro<br />
della papula è maggiore <strong>di</strong> 10-15 mm.<br />
La reazione alla tubercolina è stata (NON PIU’) utilizzata come sistema<br />
<strong>di</strong> screening della popolazione e per evidenziare i contatti.<br />
È noto che tale reazione presenti alcuni importanti svantaggi. La<br />
specificità è normalmente bassa, poiché soggetti venuti a contatto con<br />
micobatteri ambientali possono risultare positivi alla reazione. Nella PPD<br />
sono infatti presenti antigeni simili a quelli <strong>di</strong> altri micobatteri. Un altro<br />
importante svantaggio è rappresentato dal fatto che soggetti vaccinati<br />
con BCG risultano positivi al test della tubercolina, e considerando che<br />
la vaccinazione con BCG è obbligatoria nei paesi ad alta endemia <strong>di</strong> TB,<br />
è facile concludere come in questi paesi la reazione alla PPD sia <strong>di</strong><br />
scarsa utilità. 47<br />
48<br />
12
IMMUNITA’ CELLULO MEDIATA<br />
Recentemente sono stati messi in commercio test <strong>di</strong>agnostici specifici per<br />
la reazione immunitaria nei confronti <strong>di</strong> antigeni <strong>di</strong> M. tuberculosis.<br />
Gli antigeni utilizzati sono specifici per M. tubercolosis e non sono<br />
espressi da BCG.<br />
Si procede al prelievo <strong>di</strong> sangue periferico dai soggetti e alla stimolazione<br />
dei leucociti in vitro con gli antigeni purifi cati per 16-20 ore a 37 °C.<br />
Si procede quin<strong>di</strong> alla raccolta del plasma e si misura la quantità <strong>di</strong> interferone-γ<br />
prodotta.<br />
I leucociti isolati da soggetti con infezione da M. tuberculosis (latente o attiva)<br />
saranno in grado <strong>di</strong> secernere interferone-γ quando messi a contatto con gli<br />
antigeni <strong>di</strong> M. tuberculosis.<br />
Questi sistemi <strong>di</strong> <strong>di</strong>agnosi immunologica <strong>di</strong> TB consentono <strong>di</strong> <strong>di</strong>stinguere tra<br />
soggetti vaccinati con BCG e soggetti infetti, presentando l’ulteriore<br />
vantaggio <strong>di</strong> non richiedere l’inoculo <strong>di</strong> sostanze nel paziente.<br />
Diversi sistemi <strong>di</strong> <strong>di</strong>agnosi sierologica per la ricerca <strong>di</strong> anticorpi specifici<br />
sono stati messi a punto, ma la sensibilità e la specificità osservate sono<br />
state poco sod<strong>di</strong>sfacenti e tali da sconsigliare l’utilizzo.<br />
TERAPIA<br />
La terapia contro le infezioni da M. tuberculosis si basa sempre sull’utilizzo<br />
<strong>di</strong> più farmaci contemporaneamente per non selezionare le resistenze.<br />
I farmaci contro M. tuberculosis vengono <strong>di</strong>stinti in:<br />
farmaci <strong>di</strong> prima linea (streptomicina, isoniazide, etambutolo, rifampicina e<br />
pirazinamide) e<br />
farmaci <strong>di</strong> seconda linea (fl uorochinoloni, etionamide, amikacina, acido paraaminosalicilico,<br />
capreomicina, kanamicina e cicloserina).<br />
L’ISONIAZIDE (idrazide dell’acido isonicotinico) è altamente efficace contro<br />
M. tuberculosis, e agisce nel processo metabolico che porta alla sintesi degli<br />
aci<strong>di</strong> micolici. Prima <strong>di</strong> poter esercitare la sua azione a carico degli enzimi<br />
co<strong>di</strong>ficati dai geni inhA e kasA, l’isoniazide deve essere attivata dalla<br />
catalasi del micobatterio (KATG). L’isoniazide è battericida su batteri in<br />
fase <strong>di</strong> moltiplicazione attiva (lesioni polmonari) e batteriostatica nei batteri a<br />
lenta crescita o persistenti.<br />
La RIFAMPICINA inibisce l’azione dell’RNA polimerasi batterica ed esercita<br />
un azione battericida sia su batteri in rapida crescita che su batteri<br />
persistenti.<br />
49<br />
50<br />
TERAPIA<br />
Prima e Dopo TERAPIA<br />
La PIRAZINAMIDE è un farmaco che deve essere attivato in ambiente<br />
acido per raggiungere la forma attiva, inibisce la sintesi degli aci<strong>di</strong> grassi<br />
e agisce sulla popolazione batterica presente all’interno dei macrofagi.<br />
L’ETAMBUTOLO interferisce nella sintesi della parete batterica, inibendo<br />
la sintesi degli arabinogalattani. Tale azione, pur essendo <strong>di</strong> per se<br />
batteriostatica, ha il merito <strong>di</strong> scompaginare la regolare struttura della<br />
parete, facilitando l’ingresso degli altri farmaci nella cellula, potenziandone<br />
l’effi cacia, riducendo il rischio <strong>di</strong> comparsa <strong>di</strong> farmacoresistenze.<br />
51<br />
52<br />
13
DOTS Directed Observed Therapy Short-course<br />
Il protocollo terapeutico suggerito dall’OMS prende il nome <strong>di</strong> DOTS e<br />
consiste nell’assunzione simultanea <strong>di</strong>:<br />
3 farmaci (isoniazide, pirazinamide e rifampicina) per i primi 2 mesi<br />
2 farmaci (isoniazide e rifampicina) per i restanti quattro mesi.<br />
Il trattamento con più farmaci contemporaneamente si rende necessario per<br />
evitare la selezione <strong>di</strong> resistenze nel corso della terapia.<br />
È stato calcolato, ad esempio, che la frequenza <strong>di</strong> mutanti primari è <strong>di</strong> circa<br />
1 ogni 10 5 per l’isoniazide, 1 ogni 10 6 per la streptomicina e 1 ogni 10 7 per la<br />
rifampicina.<br />
La lenta crescita del micobatterio e i lunghi perio<strong>di</strong> <strong>di</strong> trattamento fanno sì<br />
che la comparsa <strong>di</strong> resistenze ai singoli farmaci sarebbe frequente nel caso<br />
<strong>di</strong> terapia con un singolo antibiotico. Viceversa, poiché la probabilità <strong>di</strong><br />
resistenza ai farmaci è moltiplicativa, l’utilizzo <strong>di</strong> più farmaci fa sì che la<br />
frequenza passi da 10 -5 nel caso dell’isoniazide a 10 -18 nel caso <strong>di</strong><br />
somministrazione con i suddetti tre farmaci contemporaneamente.<br />
ottobre 2007 e marzo 2008<br />
missione in ECUADOR:<br />
la tubercolosi<br />
53<br />
54<br />
L'esame colturale su terreno solido (tecnica già <strong>di</strong>sponibile ai<br />
tempi <strong>di</strong> R. Koch) è l'unica tecnica <strong>di</strong>agnostica attualmente<br />
<strong>di</strong>sponibile nei Paesi in via <strong>di</strong> sviluppo<br />
Terreno<br />
(LJ) SOLIDO<br />
Terreno LIQUIDO<br />
(Bactec)<br />
Terreno LIQUIDO<br />
(MGIT)<br />
Biologia molecolare<br />
(COSTI 55 EVOLUZIONE TECNICHE (e aumento 56<br />
14
MODS: MICROSCOPIC-OBSERVATION DRUG-SUSCEPTIBILITY<br />
October 12, 2006, New England Journal of Me<strong>di</strong>cine:<br />
“…è più sensibile, rapido ed economico da eseguire degli attuali<br />
test <strong>di</strong>sponibili.”<br />
GENERALITÀ<br />
Tecnica messa a punto presso la Universidad Cayetano Here<strong>di</strong>a<br />
<strong>di</strong> Lima, Perú.<br />
Si basa su due caratteristiche ben conosciute dei micobatteri:<br />
M. tuberculosis cresce più rapidamente in terreno líquido che nel<br />
solido<br />
“Aggregati ” caratterístici <strong>di</strong> M. tuberculosis possono essere visti con<br />
il microscopio invertito osservando il terreno liquido<br />
www.modsperu.org<br />
The philosophy underlying MODS is laboratory freeware: all the<br />
components are rea<strong>di</strong>ly available from laboratory suppliers; there are no<br />
hidden, patented secrets.<br />
57<br />
58<br />
STRUMENTI O REATTIVI<br />
RISULTATI<br />
terreno Middlebrook 7H9<br />
(< 1 $ / campione)<br />
microscopio invertito (1500 – 3000 $)<br />
Presenza o assenza <strong>di</strong> M. tuberculosis nel campione<br />
Sensibilità/resistenza a rifampicina<br />
Sensibilità/resistenza a isoniazide<br />
in 10-15 giorni!<br />
Moore DAJ et al. Microscopic-observation drug-susceptibility assay for the <strong>di</strong>agnosis of TB.<br />
New Eng J Med 355: 1539–1551, 2006<br />
59<br />
60<br />
15
NaOH-<br />
NALC<br />
Vortex and<br />
stand for 15<br />
minutes<br />
PBS<br />
Fill tube<br />
to 14ml<br />
Centrifuge<br />
15 min 3000g<br />
7H9<br />
PANTA<br />
OADC<br />
sample 1 sample 2 Negative QC sample 3 sample 4 sample 5 or<br />
Positive QC<br />
Sputum decontamination<br />
900µl / well<br />
C<br />
C C<br />
C C<br />
1 3 4<br />
C<br />
MODS<br />
1 2 NEG 3 4 5 / POS<br />
control<br />
control<br />
C<br />
C<br />
C<br />
C<br />
C<br />
C<br />
Culture and<br />
<strong>di</strong>rect<br />
susceptibility<br />
testing<br />
Drug-free<br />
Isoniazid<br />
Rifampici<br />
I<br />
R<br />
I<br />
R<br />
I<br />
R<br />
I<br />
R<br />
I<br />
R<br />
I<br />
R<br />
2 wells for drug-free control (C), 1 for isoniazid 0.4 µg/ml (I), 1 for rifampicin 1 µg/ml (R)<br />
Istituto <strong>di</strong> <strong>Microbiologia</strong> - Genova<br />
61<br />
62<br />
Moore DAJ et al. Microscopic-observation drug-susceptibility assay for the <strong>di</strong>agnosis of TB. New Eng J Med 355: 1539–1551, 2006<br />
63<br />
64<br />
16
65 66<br />
Istituto <strong>di</strong> <strong>Microbiologia</strong> - Genova<br />
Laboratorio del Hospital Alli Causai<br />
67<br />
Laboratorio del Hospital Alli Causai<br />
68<br />
17
COSTI<br />
Caviedes L, et al. Rapid, efficient detection and drug susceptibility testing of Mycobacterium<br />
tuberculosis in sputum by microscopic observation of broth cultures. The Tuberculosis Working<br />
69<br />
Group in Peru. J Clin Microbiol. 2000 Mar;38(3):1203-8<br />
Laboratorio del Hospital Alli Causai<br />
70<br />
ABSTRACT<br />
A collaborative project was established between the Alli Causai<br />
Foundation in Ambato, Ecuador, and the University of Genova,<br />
Italy, to introduce the microscopic observation drug susceptibility<br />
(MODS) assay for the rapid identification of Mycobacterium<br />
tuberculosis in Ecuador.<br />
A total of 507 samples were evaluated during a 10-month<br />
period, and DNA was extracted from each isolate and sent to<br />
Genova for confirmatory molecular analysis.<br />
M. tuberculosis was identified in 45 samples by MODS, and drug<br />
resistance was observed in approximately 21% of the isolates,<br />
with four multidrug-resistant strains detected in two patients.<br />
71 72<br />
18
73 74<br />
TERAPIA: RESISTENZE<br />
A seconda dei risultati del test <strong>di</strong> sensibilità ai farmaci eseguito sul ceppo<br />
isolato o a seconda della tollerabilità del farmaco da parte del paziente, la<br />
combinazione <strong>di</strong> farmaci può essere mo<strong>di</strong>ficata e/o integrata. Per una<br />
corretta ed efficace terapia è fondamentale seguire correttamente la terapia<br />
antibiotica.<br />
Negli ultimi anni si è assistito alla comparsa <strong>di</strong><br />
ceppi MDR-TB (Multi-Drug Resistant TB) che sono ceppi <strong>di</strong> M. tuberculosis<br />
resistenti a isoniazide e rifampicina e più recentemente <strong>di</strong><br />
ceppi XDR-TB (Extensively Drug Resistant TB), che sono ceppi resistenti alla<br />
rifampicina e all’isoniazide, ma anche a tutti i fluorochinoloni e ad almeno uno dei<br />
tre seguenti farmaci iniettabili: capreomicina, kanamicina e amikacina.<br />
Epidemie veicolate da tali ceppi sono state osservate in Sud-Africa e nei<br />
Paesi dell’Est Europa, e sono stati isolati anche in Europa e in Italia. La<br />
mortalità in pazienti infettati con tali ceppi è molto maggiore rispetto ai<br />
ceppi sensibili, per l’inefficacia dei trattamenti terapeutici <strong>di</strong>sponibili.<br />
La comparsa <strong>di</strong> epidemie veicolate da questi ceppi rende ancora più urgente<br />
lo sviluppo <strong>di</strong> nuovi farmaci contro M. tuberculosis. La maggior parte dei<br />
farmaci in uso sono stati sviluppati oltre quarant’anni fa, e le poche molecole<br />
attive identificate <strong>di</strong> recente stentano ad essere inserite nei regimi<br />
75 76<br />
terapeutici.<br />
19
MYCOBACTERIUM LEPRAE<br />
Mycobacterium leprae è l’agente eziologico della lebbra o malattia<br />
<strong>di</strong> Hansen.<br />
Si stima che nel mondo siano 1-2 milioni le persone con <strong>di</strong>sabilità<br />
ascrivibile all’infezione da M. leprae.<br />
Nel 2006 i casi <strong>di</strong> lebbra conclamata sono stati circa 220 000, la<br />
maggior parte dei quali sono stati registrati in In<strong>di</strong>a, Brasile e Africa<br />
centrale.<br />
M. leprae è un bacillo AAR che cresce nei macrofagi, cellule neurali,<br />
nella zona plantare <strong>di</strong> topi atimici e nell’arma<strong>di</strong>llo.<br />
Non è mai stato coltivato in terreno <strong>di</strong> coltura e viene considerato un<br />
patogeno intracellulare obbligato.<br />
Si ritiene che il tempo <strong>di</strong> replicazione (stimato in circa 12-14 giorni)<br />
sia responsabile del lungo tempo <strong>di</strong> incubazione e della necessità <strong>di</strong><br />
adottare lunghi trattamenti terapeutici.<br />
77<br />
MYCOBACTERIUM LEPRAE<br />
Il completamento della sequenza del genoma <strong>di</strong> M. leprae ha permesso <strong>di</strong><br />
comprendere meglio alcuni aspetti della biologia <strong>di</strong> questo importante<br />
micobatterio.<br />
Il genoma <strong>di</strong> M. leprae è <strong>di</strong> circa 3 268 203 bp (circa 75% <strong>di</strong> quello <strong>di</strong> M.<br />
tuberculosis), ma i geni co<strong>di</strong>ficati sono soltanto 1606 (40% <strong>di</strong> M.<br />
tuberculosis).<br />
Nel genoma <strong>di</strong> M. leprae sono stati in<strong>di</strong>viduati oltre 1100 pseudogeni (geni<br />
con inserzioni, delezioni o comunque non co<strong>di</strong>ficanti per proteine) e questo<br />
numero è assolutamente incoerente con quanto trovato finora nel genoma<br />
non solo <strong>di</strong> altri micobatteri ma anche <strong>di</strong> altri batteri.<br />
Si ritiene che M. leprae abbia subito durante l’evoluzione un processo <strong>di</strong><br />
deca<strong>di</strong>mento genico che ha determinato l’inattivazione della maggior parte<br />
del corredo genico.<br />
La lebbra raramente uccide il paziente, ma risulta essere fortemente<br />
invalidante per i danni prodotti agli arti e altri tessuti periferici. La lebbra è<br />
una infezione granulomatosa cronica e lentamente progressiva che<br />
coinvolge la pelle e i tessuti nervosi periferici. È stato infatti <strong>di</strong>mostrato<br />
come M. lepre presenti un particolare tropismo per i nervi periferici.<br />
78<br />
MYCOBACTERIUM LEPRAE<br />
L’infezione è generalmente limitata alle parte più fredde dell’organismo (pelle,<br />
naso, tratto respiratorio superiore). Generalmente gli organi interni quali cervello,<br />
fegato, milza, reni e ossa, non risultano essere coinvolti. Si è solito <strong>di</strong>stinguere due<br />
tipi <strong>di</strong> lebbra:<br />
lebbra lepromatosa. È caratterizzata da una scarsa risposta immunitaria dell’ospite<br />
che non è in grado <strong>di</strong> controllare la replicazione del bacillo. In questi casi l’analisi<br />
microscopica dei tessuti evidenzia la presenza <strong>di</strong> numerosissimi batteri AAR (forma<br />
multibacillare). È questa la forma altamente contagiosa <strong>di</strong> lebbra, fortemente invalidante e<br />
che richiede prolungati trattamenti terapeutici (> 2 anni).<br />
lebbra tubercoloide. È caratterizzata da una buona risposta immunitaria, dalla presenza<br />
<strong>di</strong> pochi batteri AAR nei tessuti, e da un modesto danno tissutale. Non è contagiosa e il<br />
trattamento si conclude normalmente entro 6 mesi <strong>di</strong> terapia.<br />
Possono comunque presentarsi forme <strong>di</strong> lebbra interme<strong>di</strong>e.<br />
La <strong>di</strong>agnosi si effettua generalmente su base clinica e può essere confermata dalla<br />
presenza nel reperto microscopico <strong>di</strong> bacilli acido-alcol resistenti.<br />
Il trattamento farmacologico si basa sull’utilizzo <strong>di</strong> dapsone, clofazimina e<br />
rifampicina, somministrati da soli od in combinazione a seconda del quadro clinico.<br />
79<br />
ALTRI <strong>MICOBATTERI</strong><br />
La maggior parte dei micobatteri sono batteri ambientali o saprofiti e possono essere<br />
isolati normalmente dal suolo o dall’acqua. Alcuni <strong>di</strong> questi micobatteri possono<br />
causare importanti patologie nell’ospite umano, in particolare nel soggetto<br />
immunocompromesso.<br />
Chiamati micobatteri atipici, opportunisti o anonimi, oggi si identificano quali Non-<br />
Tuberculous Mycobacteria (NTM) o Mycobacteria Other Than Tuberculosis<br />
(MOTT).<br />
Possono causare infezioni croniche a livello polmonare simili a quelli causate da M.<br />
tuberculosis nel soggetto adulto; linfoadeniti localizzate nei bambini; infezioni della<br />
cute e dei tessuti molli; infezioni <strong>di</strong>sseminate.<br />
Negli anni 80-90 del secolo scorso abbiamo assistito a un emergere <strong>di</strong> infezioni<br />
<strong>di</strong>sseminate in soggetti con AIDS. La riduzione del numero <strong>di</strong> linfociti T CD4<br />
circolanti determinava una incapacità dei macrofagi <strong>di</strong> attivarsi e <strong>di</strong> esercitare una effi<br />
cace azione antimicobatterica, che aveva come risultato la comparsa <strong>di</strong> infezioni<br />
<strong>di</strong>sseminate. Tra le specie più frequentemente associate a tali infezioni ritroviamo<br />
Mycobacterium avium intracellulare complex, sebbene molti altre specie siano<br />
state isolate. Negli ultimi anni, l’introduzione <strong>di</strong> più efficaci terapie anti-retrovirali ha<br />
reso molto meno frequenti questo tipo <strong>di</strong> infezioni.<br />
I MOTT hanno un genoma più grande rispetto ai micobatteri patogeni come M.<br />
tuberculosis, ma conservano la loro capacità <strong>di</strong> resistere e moltiplicarsi all’interno dei<br />
macrofagi e/o delle cellule dell’ospite come principale meccanismo <strong>di</strong> patogenesi.<br />
80<br />
20