La respirazione cellulare - Bgbunict.it
La respirazione cellulare - Bgbunict.it
La respirazione cellulare - Bgbunict.it
- No tags were found...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
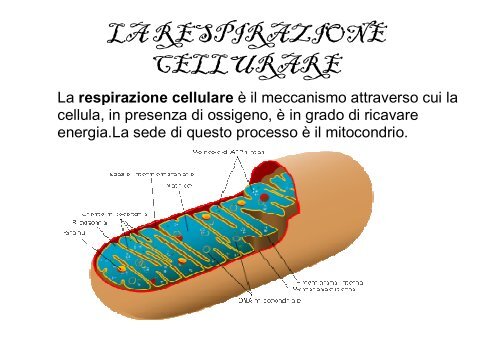
LA RESPIRAZIONECELLURARE<strong>La</strong> <strong>respirazione</strong> <strong>cellulare</strong> è il meccanismo attraverso cui lacellula, in presenza di ossigeno, è in grado di ricavareenergia.<strong>La</strong> sede di questo processo è il m<strong>it</strong>ocondrio.
I m<strong>it</strong>ocondri (dal greco”m<strong>it</strong>os”,filoe“condros”corpuscolo)generalmente defin<strong>it</strong>i”lacentrale elettrica della cellula”sono degli organuli endocellulari che presentano unaforma bastoncellare o a fagiolo con un diametro di 0,5µm ed una lunghezza di 1-2µm.Morfologicamente im<strong>it</strong>ocondri sono caratterizzati da una membrana esternae da una membrana interna.le due membranedelim<strong>it</strong>anodue compartimenti che sono chiamati camera esterna ematrice.<strong>La</strong> camera esterna è lo spazio compreso tra ledue membrane,la matrice è , invece,lo spazio delim<strong>it</strong>atodalla membrana interna.
<strong>La</strong> membrana interna presenta delle invaginazioni,chesi estendono nella matrice,denominate crestem<strong>it</strong>ocondriali.Le due membrane differiscono fra diloro per la composizione chimica,infatti lamembrana esterna e caratterizzata da un maggiorecontenuto di lipidi rispetto alle proteine mentre lamembrana interna risulta essere cost<strong>it</strong>u<strong>it</strong>amaggiormente da proteine ed inoltre ècaratterizzata dalla presenza di cardiolipina,unfosfolipide raro che d’altra parte è del tutto assentein quella esterna.
Nella matrice sono contenuti ribosomi e molecolecircolari di mtDNA che sono molto simili a quellidelle cellule procariotiche e la loro presenzapermette ai m<strong>it</strong>ocondri la sintesi di proteine cherendono questi organuli semi-autonomi rispetto allacellula stessa.Tra le sostanze che essi possonosintetizzare autonomamente sono comprese leproteine del comlplesso Fo-F1 ATPsintetasi
Fo è un complesso proteico che svolge la funzione dicanale di trans<strong>it</strong>o per protoni,F1 catalizza la reazione disintesi dell’ATP,che cost<strong>it</strong>uisce la moneta energetica,apartire da ADP+Pi.
Cosa avviene nel processodi <strong>respirazione</strong> <strong>cellulare</strong>?All’interno dei m<strong>it</strong>ocondri avvengono delle reazioniredox,che producono energia,nelle quali un composto(riducente) trasferisce elettroni ad un altro composto(ossidante).In queste reazioni gli elettroni si spostanoda composti che li legano a se ad alti livelli energeticia composti che li legano a livelli energetici sempre piùbassi fino ad arrivare all’accettore finale che èl’ossigeno il quale,con l’aggiunta di due protoniH+,formerà H2O.
Un ruolo molto importante che consiste nel trasportodegli elettroni fino all’accettore finale ,che abbiamodetto essere l’O2,lungo la catena respiratoria è svoltodai cofattori NAD+ e FAD,che veicolano gli elettroniriducendosi a NADH+H+ e FADH2.NAD(NICOTINAMMIDE ADENIN DINUCLEOTIDE) FAD(FLAVIN ADENIN DINUCLEOTIDE)
Le molecole che ,ossidandosi,consentiranno aim<strong>it</strong>ocondri di produrre ATP sono i carboidrati,i lipidi,leproteine e gli acidi nucleici.Poichè sono molecolerelativamente grandi prima di entrare nei m<strong>it</strong>ocondrisubiranno delle particolari modificazioni chedifferiscono a seconda della natura chimica.Icarboidrati vengono idrolizzati in monosaccaridi,leproteine in amminoacidi che successivamenteverranno deaminati(-NH2),I lipidi scissi in glicerolo eacidi grassi.Tali modificazioni prendono luogo nelc<strong>it</strong>oplasma,ed inoltre i monosaccaridi sono soggetti adun’ulteriore trasformazione che porta alla formazionedi piruvato( CH3-CO-COOH) e che prende il nome diglicolisi.
LA GLICOLISIEssa dunque consiste nelprocesso di ossidazione di un monosaccaride conformazione di due molecole di piruvato che si realizzain dieci tappe.
Reazione 1Nella 1°tappa il glucosio viene fosforilato in gluco sio 6-fosfato.la reazione è catalizzata dall’enzimaesochinasi con consumo di una molecoladi ATP.Nella 2°tappa si ha l’isomerizzazioneDel glucosio 6-P in fruttosio 6-P.Ad opera è l’enzimaFosfoglucoisomerasi.Reazione 2
Reazione 3Nel 3°step il fruttosio 6-P vieneulteriormente fosforilato.L’enzimacatalizzante è la fosfofruttochinasi.A tal punto la cellula si trova indifetto di 2 ATP,che sono state usateper formare una molecola instabile in modo da facil<strong>it</strong>are larottura del legame covalente,infatti la presenza nella molecola didue radicali fosforici legati al C1 e al C6,che sono all’esternodell’anello,fa si che gli elettroni vengano attratti dai due fosfati.Ciò indebolirà il legame tra gli atomi di C3 e C4,favorendo larottura della molecola e la formazione di due molecole a treatomi di carbonio:<strong>La</strong> (3PGAL)Gliceraldeide 3-fosfatoe il (DHAP)Diidrossiacetone fosfato.
Reazione 4<strong>La</strong> 4°fase della glicolisi ,catalizzata dall’enzima a ldolasi,consistenella scissione del fruttosio 1,6-bifosfato in gliceraldeide-3-P ediidrossiacetone fosfato,composti a tre atomi dicarbonio.Tuttavia soltanto la 3PGAL entra nella fasesuccessiva.
Reazione 5 e 6Man mano che la 3PGAL viene consumata cedendo 2 elettroni ee due protoni al NAD+ riducendolo a NADH+H+ formando 1,3difosfoglicerato ad opera della 3PGALdeidrogenanasi(REAZIONE 6) ,entra in gioco unenzima,la trioso fosfato isomerasi,che trasforma il DHAP in3PGAL.
Reazione 7 e 8Il 7°step consiste nella defosforilazione del 1-3 dif osfogliceratoIn 3-fosfoglicerato con guadagno di una molecola di ATP,l’enzimache catalizza la reazione è la fosfoglicerato chinasi.Successivamente il G3P è soggetto ad un riarrangiamentocatalizzato dalla fosfoglicerato mutasi con formazione di2-fosfoclicerato.
Reazione 9 e 10Nella penultima reazione il 2-fosfoglicerato viene disidratato afosfoenolpiruvato,reazione catalizzata dall’enzimaEnolasi,infine quest’ultimo composto viene defosforilato dallaPiruvato chinasi,con guadagno netto di un un ATP per ogn<strong>it</strong>rioso quindi in totale due; in enolpiruvato che dopo un ultimoriarrangiamento diventa acido piruvico.
Il resoconto energetico della glicolisi è:• 2 molecole di ATP e non 4 perché nelle prime fasi siha un dispendio energetico pari a 2 ATP• 2 NADH+H+• 2 molecole di H2OUna volta che si ha ottenuto il piruvato vi sono duepossibiltà d’impiego di quest’ultimo a seconda che lacellula si trovi in condizione di aerobiosi o anaerobiosi.Se la cellula è in anaerobiosi avviene un processodenominato FERMENTAZIONE,che consiste nelprocesso di riossidazione del NAD+ e del FAD.
<strong>La</strong> Fermentazione può essere <strong>La</strong>ttica o Alcolica.Nella fermentazione lattica il piruvato agisce daaccettore di elettroni e protoni legati al cofattoreNADH+,trasformandosi in acido lattico.Questo tipo difermentazione avviene anche in organismi chenormalmente si trovano in condizione aerobica masono in defic<strong>it</strong> d’ossigeno,es:mioc<strong>it</strong>a.
<strong>La</strong> Fermentazione Alcolica,come nel caso dei liev<strong>it</strong>iconsta di due tappe.Nella prima l’acido piruvico vienedecarbossilato dalla piruvato decarbossilasi inacetaldeide con conseguente produzione di CO2,nellaseconda l’acetaldeide viene deidrogenata ad alcoletilico con conseguente ossidazione delNAD+(l’enzima che catalizza la reazione è la AlcolDeidrogenasi).Sia la fermentazione lattica che quellaalcolica sono dei processi che non avvengono nelm<strong>it</strong>ocondrio ma nel c<strong>it</strong>oplasma.
IL percorso svolto dal piruvato in cellule in aerobiosi eben diverso da quello poc’anzi esposto,infatti il piruvatiper poter subire una completa ossidazione deveentrare nella matrice m<strong>it</strong>ocondriale attraversando ledue membrane.Nella matrice è presente il complessomultienzimatico della piruvato deidrogenasi,checontiene più copie di tre enzimi ad attiv<strong>it</strong>àcatal<strong>it</strong>ica:piruvato deidrogenasi,diidrolipoammideacetiltransferasi e diidrolipoammide deidrogenasi.
IL complesso multienzimatico della piruvatodeidrogenasi è responsabile della rapidatrasformazione del piruvato in gruppo acetile cheviene rapidemente legato al coenzima A(CoACoA), ),unamolecola nucleotidica,formando aceti-coenzima A.Sintesi acetil-CoA=CH3COCOOH+(NAD+)+CoA=>=>acetil-CoA+(NADH+H+)+CO2
Ciclo di Krebs
Nella matrice sono presenti gli enzimi che consentono la completaossidazione del gruppo acetile,derivato dal piruvato,inCO2,grazie ad una serie di reazioni che vengono indicatecomplessivamente come ciclo dell’acido c<strong>it</strong>rico.Il ciclo inizia conla cessione del gruppo acetile(CH3-CO-)da parte dell’acetilCoA all’acido ossalacetico(COO¯-CO-CH3-COO¯)che s<strong>it</strong>rasforma in c<strong>it</strong>rato.il 2°step,catalizzato dall’Acon tasi, consistenell’isomerizzazione del c<strong>it</strong>rato in isoc<strong>it</strong>rato,successivamentel’isoc<strong>it</strong>rato va incontro a decarbossilazione ossidativa(Isoc<strong>it</strong>ratodeidrogenasi) formando α-chetoglutarato,NADH ridotto e unamolecola ci CO2.<strong>La</strong> reazione successiva molto simile allaprecedente prevede la decarbossilazione ossidativa dell’αchetoglutarato(glutaratodeidrogenasi)formando nuovamenteCO2,NADH ridotto e un composto a cui viene aggiunto il CoAche prende il nome di succinil-CoA.(dominio catal<strong>it</strong>ico della diidrolipoammidesucciniltransferasi,parte del complessodella α-chetoglutarato deiidrogenasi)
Il ciclo continua e il succinato viene ossidato dallasuccinato deidrogenasi ,riduncedo 1 FAD a FADH2,esi forma acido fumarico.Nella penultima reazione il fumarato,idratato dalla fumarasi, formal’acido malico.Nell’ultima tappa ilmalato viene ossidato ad ossalacetatodalla malato deidrogenasi,producendo una molecola diNADH ridotto,e il ciclo si chiude.
In ogni ciclo dunque si avrà la liberazione di 2 molecoledi CO2 e la formazione di 3 molecole diNADH,FADH2,1 di ATP o GTP.Tenendo conto che igruppi acetile inser<strong>it</strong>i nel ciclo sono due per ognimolecola di glucosio,i prodotti vanno duplicati.Seconsideriamo ulteriormente che le 2 molecole dipiruvato ottenute dalla glicolisi,prima di entrare nelciclo di crebs,siano state trasformate in acetil-CoAformando 2 molecole di CO2 e NADH+H+,la reazionedi ossidazione completa dei prodotti della glicolisidiventa:2(CH3-CO-COO¯)+8(NAD+)+2FAD+2ADP+2Pi6CO2+8NADH+(8H+)+2FADH2+2ATP
SISTEMI SHUTTLELe molecole di NADH formatesi nelc<strong>it</strong>oplasma,in segu<strong>it</strong>o alla glicolisi,non riescono a passare la membranainterna per cedere i loro elettroni allacatena di trasporto,quindi le cellule per recuperare l’energia deglielettroni conservata nelle molecole di NADH fanno ricorso aisistemi navetta.In alcune cellule i NADH in questione vengono ossidatia livello della membrana esterna del m<strong>it</strong>ocondriocedendo i propri e¯ ad una molecola di DHAP che s<strong>it</strong>rasforma in glicerolo-3-P.Quest’ultimo attraversa lamembrana interna e si ossida a DHAP riducendo unamolecola di FAD a FADH2.Il DHAP r<strong>it</strong>orna nel c<strong>it</strong>oplasma ed èpronto a ricominciare il ciclo.
Con questo tipo di sistema, pur essendo vantaggiosoper la cellula,si ha perd<strong>it</strong>a di energia in quanto nellamolecole di FADH2 gli elettrone si trovano ad unlivello energetico più basso rispetto a quello con cuisono legati nelle molecole di NADH.
In altri tipi di cellule,come cellule cardiache omuscolari,le molecole di NADH, provenienti dalc<strong>it</strong>oplasma,vendono ossidate nel compartimentointermembranario,in segu<strong>it</strong>o alla trasformazione di unmolecola di ossalacetato in malato; quest’ultimoattraversa la membrana interna e viene riossidato aossalacetato riducendo una molecola NAD+ a NADH.In questo sistema l’energia viene conservataintegralmente.
CATENA DI TRASPORTO DEGLI e¯Nella membrana interna dei m<strong>it</strong>ocondri vi sono 4complessi in grado in grado di trasferire all’ossigenogli elettroni trasportati dalle molecole di NADH.Complesso 1:NADH-CoenzimQ ossidoreduttasiComplesso 2:succinato-CoenzimaQ ossidorettutasiComplesso 3:CoenzimaQ-c<strong>it</strong>ocromo c ossidoreduttasiComplesso 4:C<strong>it</strong>ocromo c ossidasi
Ogni complesso è cost<strong>it</strong>u<strong>it</strong>o da:• Enzima principale, che consente il trasferimento degli e¯.• Gruppi prostetici associati a proteine, che accettono ecedono gli e¯.• Proteine strutturali,che nei complessi 1,3 e 4 consentono laformazione del gradiente protonico nello spaziointermembranario.Inoltre vi sono due trasportatori mobili che trasferisconogli elletroni da un complesso all’altro.Il 1°è l’Ubichinone,molecola organica non proteicail 2°è il c<strong>it</strong>ocromo c, una proteina molto piccola a cui èassociato un gruppo prostetico.
L’Ubichinone o Coenzima Q è formato da una strutturaad anello detta chinone e da una lunga catenaapolare.L’ubichinone pare essere s<strong>it</strong>uata nella parteapolare della membrana interna e, movendosiliberamente consentirebbe il trasferimento di e¯ e H+tra i vari trasportatori.Coenzima Q ossidato Coenzima Q forma semichinonicaCoenzimaQ ridotto
I gruppi Prostetici che associati alle proteine permettonoil trasferimento di elettrroni sono di 4 tipi:• C<strong>it</strong>ocromi(a,a3,b,c1),composti caratterizzati da unanello tetrapirrolico con al centro un atomo di ferro.Essi passano dallo stato ossidato allo stato ridotto inquanto l’atomo di Fe centrale,acquistando o cedendoun elettrone, passa da Fe2+ a Fe3+.
• FAD e FMN(flavin mononucleotide)• Centri ferro-zolfo,in cui atomi di Fee di S sono legati con legami covalenti.Il complesso formato dai centri Fe-Se dalle proteine associate cost<strong>it</strong>uisconoLe proteine ferro-zolfo che sono sono la classe d<strong>it</strong>rasportatori di elettroni m<strong>it</strong>ocondriale più numerosa.• Centri a rame,dove un atomo di rame,legato ed unresiduo di istidina, cisteina o metionina, permette iltrasferimento di elettroni,passando da uno stato ridottoCu+ ad uno stato ossidato Cu2+.
Fosforilazione ossidativaNel 1961 M<strong>it</strong>chell enunciò la teoriachemiosmotica che per la prima voltaMetteva in relazione la <strong>respirazione</strong> <strong>cellulare</strong>Con la sintesi di ATP,spiegandone il meccanismo.Sempre nello stesso anno Racker dimostro che,isolandole particelle F0 ed F1dell’ATPsintasi,in loro assenza laSintesi di ATP non avveniva,nonostante il trasporto dielettroni si verificasse normalmente.Egli inoltre verificòche senza trasporto di elettroni,non creandosi ilgradiente protonico,il complesso F0-F1 non sintetizzaATP;infatti l’uso si sostanze disaccoppianti,che impediscono laformazione del gradiente, provoca il rilascio dell’energia cedutadagli elettroni,durante il loro trasferimento lungo la catena diTrasporto, sotto forma di calore.
Secondo la teoria chemiosmotica di M<strong>it</strong>chell,nelle tappe deltrasferimento di elettroni in cui viene rilasciata energialibera,quest’ultima viene utilizzata per trasferire protoni dalla matriceallo spazio intermembranario.IL complesso 1 libera energiasufficiente per spingere nella camera esterna 4 protoni,mentre icomplessi 3 e 4 consentono la spinta di 2 protoni.Ancora non è benchiaro il meccanismo che permette ai complessi 1,3 e 4 di trasferire iprotoni ,ma l’ipotesi più accred<strong>it</strong>ata è quella della modificazioneconformazionale proposta da Boyer,secondo la quale quando untrasportatore di elettroni si riduce,induce un cambiamentoconformazionale in una delle molecole proteiche associate alcomplesso.Tale cambiamento attiva sul versante della matrice un s<strong>it</strong>odi legame ad alta affin<strong>it</strong>à per un protone;quando il trasportatore saràossidato,il s<strong>it</strong>o di legame del protone si modificherà volgendosi versoil compartimento intermembrana dove il protone sarà rilasciato insegu<strong>it</strong>o alla diminu<strong>it</strong>a affin<strong>it</strong>à.Il r<strong>it</strong>orno dei protoni nella matriceavviene attraverso la particella F0,ciò provoca il riequilibrio delpotenziale di membrana e la cessione di energia al sistema;taleenergia verrà utilizzata da F1 per sintetizzare ATP.
Per concludere,la quant<strong>it</strong>à energetica che una cellula può ricavaredall’ossidazione di una molecola di glucosio si può calcolaretenendo conto che ogni molecola di NADH porta alla sintesi di2,5 molecole di ATP mentre una molecola di FADH2 forma 1,5molecole ATP.ATP da NADH della matriceATP da FADH2 della matrice8x2,5=202x1,5=3ATP da ciclo di Krebs 2ATP da glicolisi 2ATP da NADHglicolisi(shuttle DHAP)2x1,5=3Tot = 30o ATP da NADHglicolisi(shuttle a.malico)2x2,5=5Tot = 32






![Glucidi-Lipidi-010210 [modalità compatibilità] - Bgbunict.it](https://img.yumpu.com/41100335/1/190x134/glucidi-lipidi-010210-modalita-compatibilita-bgbunictit.jpg?quality=85)