Bekijk hoofdstuk 1 - Educatheek.nl
Bekijk hoofdstuk 1 - Educatheek.nl
Bekijk hoofdstuk 1 - Educatheek.nl
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
2. Warmteleer 45<br />
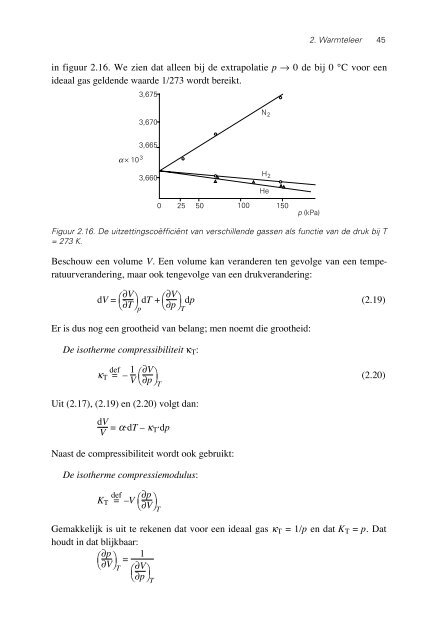
in figuur 2.16. We zien dat alleen bij de extrapolatie p → 0 de bij 0 °C voor een<br />
ideaal gas geldende waarde 1/273 wordt bereikt.<br />
α × 10 3<br />
3,675<br />
3,670<br />
3,665<br />
3,660<br />
N 2<br />
H 2<br />
He<br />
0 25 50 100 150<br />
p (kPa)<br />
Figuur 2.16. De uitzettingscoëfficiënt van verschillende gassen als functie van de druk bij T<br />
= 273 K.<br />
Beschouw een volume V. Een volume kan veranderen ten gevolge van een temperatuurverandering,<br />
maar ook tengevolge van een drukverandering:<br />
dV = ⎛∂V⎞<br />
⎝ ⎠<br />
dT + ⎛∂V⎞<br />
dp (2.19)<br />
⎝ ⎠<br />
∂T p<br />
∂p T<br />
Er is dus nog een grootheid van belang; men noemt die grootheid:<br />
De isotherme compressibiliteit κT:<br />
κT =<br />
def – 1<br />
V ⎝ ⎛∂V⎞<br />
⎠<br />
∂p T<br />
Uit (2.17), (2.19) en (2.20) volgt dan:<br />
dV<br />
V<br />
= α·dT – κT·dp<br />
Naast de compressibiliteit wordt ook gebruikt:<br />
De isotherme compressiemodulus:<br />
KT =<br />
def –V ⎛∂p⎞<br />
⎝ ⎠<br />
∂V T<br />
(2.20)<br />
Gemakkelijk is uit te rekenen dat voor een ideaal gas κT = 1/p en dat KT = p. Dat<br />
houdt in dat blijkbaar:<br />
⎛∂p⎞<br />
⎝∂V⎠<br />
=<br />
T<br />
1<br />
⎛∂V⎞<br />
⎝ ⎠<br />
∂p T