ANEXO II - áreas 018 a 035 - Universidade Federal do Acre
ANEXO II - áreas 018 a 035 - Universidade Federal do Acre
ANEXO II - áreas 018 a 035 - Universidade Federal do Acre
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
curvas, de mo<strong>do</strong> geral, ao se aumentar a temperatura? c) A função que dá a distribuição P (ou densidade de<br />
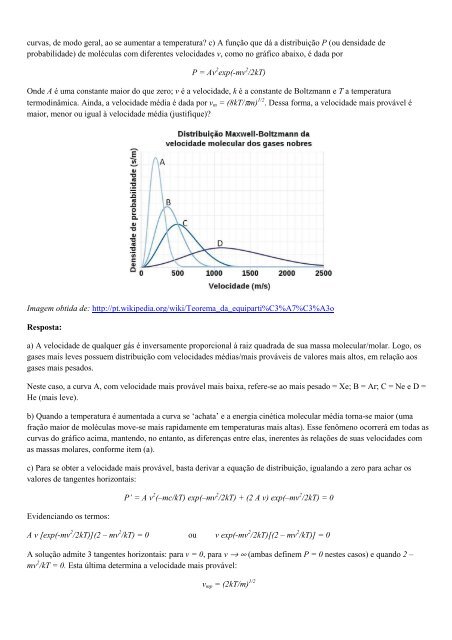
probabilidade) de moléculas com diferentes velocidades v, como no gráfico abaixo, é dada por<br />
P = Av 2 exp(-mv 2 /2kT)<br />
Onde A é uma constante maior <strong>do</strong> que zero; v é a velocidade, k é a constante de Boltzmann e T a temperatura<br />
termodinâmica. Ainda, a velocidade média é dada por vm = (8kT/πm) 1/2 . Dessa forma, a velocidade mais provável é<br />
maior, menor ou igual à velocidade média (justifique)?<br />
Imagem obtida de: http://pt.wikipedia.org/wiki/Teorema_da_equiparti%C3%A7%C3%A3o<br />
Resposta:<br />
a) A velocidade de qualquer gás é inversamente proporcional à raiz quadrada de sua massa molecular/molar. Logo, os<br />
gases mais leves possuem distribuição com velocidades médias/mais prováveis de valores mais altos, em relação aos<br />
gases mais pesa<strong>do</strong>s.<br />
Neste caso, a curva A, com velocidade mais provável mais baixa, refere-se ao mais pesa<strong>do</strong> = Xe; B = Ar; C = Ne e D =<br />
He (mais leve).<br />
b) Quan<strong>do</strong> a temperatura é aumentada a curva se ‘achata’ e a energia cinética molecular média torna-se maior (uma<br />
fração maior de moléculas move-se mais rapidamente em temperaturas mais altas). Esse fenômeno ocorrerá em todas as<br />
curvas <strong>do</strong> gráfico acima, manten<strong>do</strong>, no entanto, as diferenças entre elas, inerentes às relações de suas velocidades com<br />
as massas molares, conforme item (a).<br />
c) Para se obter a velocidade mais provável, basta derivar a equação de distribuição, igualan<strong>do</strong> a zero para achar os<br />
valores de tangentes horizontais:<br />
Evidencian<strong>do</strong> os termos:<br />
P’ = A v 2 (–mc/kT) exp(–mv 2 /2kT) + (2 A v) exp(–mv 2 /2kT) = 0<br />
A v [exp(-mv 2 /2kT)](2 – mv 2 /kT) = 0 ou v exp(-mv 2 /2kT)[(2 – mv 2 /kT)] = 0<br />
A solução admite 3 tangentes horizontais: para v = 0, para v → ∞ (ambas definem P = 0 nestes casos) e quan<strong>do</strong> 2 –<br />
mv 2 /kT = 0. Esta última determina a velocidade mais provável:<br />
vmp = (2kT/m) 1/2