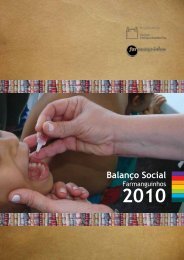
US$ 3,00R$ 6,00US$ 2,00US$ 1,00R$ 4,00R$ 2,0051995 1996 1997 1999 2000 2001 2002 2003 2004 2005A mesma proporcionalida<strong>de</strong> é vista quando contrastamos o número acumuladoVenda da Biobrás AnimalHumanaAnimalHumana<strong>de</strong> suspeita <strong>de</strong>à NovoRAMNordiskcom as dosesUS $distribuídasUS $(Gráfico 4).R$Foram disponibilizadasem torno <strong>de</strong> 85 milhões <strong>de</strong> doses no período <strong>de</strong> nove meses e restaramR$apenas <strong>de</strong>z contatos classificados como suspeita <strong>de</strong> RAM.Gráfico 4:Atendimentos acumulados feitos pelo FAC em relação aonúmero <strong>de</strong> doses acumuladas expedidas no período <strong>de</strong>grafico 4nov/07 a ago/200890.000.00080.000.00070.000.00060.000.00050.000.00040.000.00030.000.00020.000.00010.000.0001110987654321US $ 10,0US $ 9,0US $ 8,0US $ 7,0US $ 6,0US $ 5,0US $ 4,0US $ 3,0US $ 2,0US $ 1,00Nov Dez Jan Fev Mar Abr Mai Jun Jul Ago2007 2008Total Insulina expedida(doses acumuladas)Suspeita RAMFonte: FAC <strong>de</strong> <strong>Farmanguinhos</strong>Vendà No8.3 Inspeções da AnvisaApós a primeira inspeção à fábrica do Indar na Ucrânia, realizada em janeiro <strong>de</strong>2007, foi concedido o certificado <strong>de</strong> Boas Práticas <strong>de</strong> Fabricação (BPF) ao institutoe o registro do produto a <strong>Farmanguinhos</strong>, em março <strong>de</strong> 2007, sem nenhumaexigência a se cumprir. Em seguida, <strong>Farmanguinhos</strong> abriu a primeira carta <strong>de</strong> créditopara a compra <strong>de</strong> 3,5 milhões <strong>de</strong> frascos <strong>de</strong> <strong>insulina</strong>, dos quais 2,4 milhões jáforam distribuídos à população entre novembro/2007 a agosto/2008.Em junho <strong>de</strong> 2008, a agência reguladora voltou a inspecionar a unida<strong>de</strong> ucraniana,e, ao contrário do ocorrido na primeira visita, houve problemas <strong>de</strong> comunicaçãoentre os técnicos do Indar e os inspetores da agência, que enten<strong>de</strong>ram que24 PRODUÇÃO PÚBLICA DE INSULINA
parte do processo produtivo do produto importado pelo Brasil era feita na fábricarecentemente inaugurada na cida<strong>de</strong> <strong>de</strong> L’viv e não na fábrica <strong>de</strong> Kiev, foco <strong>de</strong>inspeção, ferindo uma norma da agência, a RDC 315/05. Questionou-se tambéma capacida<strong>de</strong> <strong>de</strong> produção da planta <strong>de</strong> Kiev. Ainda que o diretor do Indar tenha,em exposição pessoal e por documentos, comprovado que a origem do produtoexportado ao Brasil era Kiev, os argumentos não foram aceitos pela Agência.Antes da inspeção <strong>Farmanguinhos</strong> transmitira a Anvisa o pedido do fabricante <strong>de</strong>incluir na inspeção a visita ao local <strong>de</strong> fabrico <strong>de</strong> L’viv, mas a Agência recomendouque ela fosse realizada em uma segunda ocasião por não po<strong>de</strong>r esten<strong>de</strong>r aviagem <strong>de</strong> seus inspetores por mais alguns dias.A inspeção em andamento foi cancelada com a volta dos inspetores ao Brasil ese iniciou intensa troca <strong>de</strong> informações e realização <strong>de</strong> reuniões entre a Agência,o Indar e <strong>Farmanguinhos</strong> para esclarecer o ocorrido. Por precaução, em agosto<strong>de</strong> 2008 a Anvisa suspen<strong>de</strong>u as importações e a distribuição <strong>de</strong> um milhão <strong>de</strong>frascos <strong>de</strong> <strong>insulina</strong> recebidos nas últimas importações, exigindo testes <strong>de</strong> qualida<strong>de</strong>que comprovassem que a qualida<strong>de</strong> do produto não se alterara <strong>de</strong>s<strong>de</strong> aprimeira inspeção. Prontamente <strong>Farmanguinhos</strong> encaminhou testes <strong>de</strong> qualida<strong>de</strong>já realizados em alguns lotes do produto e provi<strong>de</strong>nciou a execução <strong>de</strong> testes <strong>de</strong>qualida<strong>de</strong>, incluindo teste <strong>de</strong> potência biológica em camundongos, <strong>de</strong> 34 lotesarmazenados. <strong>Farmanguinhos</strong> contestou a <strong>de</strong>cisão da agência <strong>de</strong> suspen<strong>de</strong>r asdistribuições, pelas consequências que essa medida traria a milhares <strong>de</strong> brasileirosjá adaptados ao uso do produto, <strong>de</strong> altíssima qualida<strong>de</strong>, como <strong>de</strong>monstravamos testes realizados e os dados <strong>de</strong> farmacovigilância. É <strong>de</strong> se registrar a ação <strong>de</strong>concorrentes – milhares <strong>de</strong> mensagens eletrônicas foram encaminhadas a diabéticospedindo que <strong>de</strong>nunciassem problemas com o produto – mas, ainda assimrestou o registro <strong>de</strong> apenas três reações do tipo alérgico, notificados <strong>de</strong>pois daaplicação <strong>de</strong> 2,5 milhões <strong>de</strong> frascos, ou seja, 85 milhões <strong>de</strong> aplicações, sendo queum milhão dos mesmos supostamente proveio <strong>de</strong> etapas <strong>de</strong> produção realizadaem L’viv. <strong>Farmanguinhos</strong> requisitou a realização, com maior brevida<strong>de</strong> possível,<strong>de</strong> nova inspeção ao Indar focando os pontos <strong>de</strong> <strong>de</strong>FACordo levantados. A Anvisamanteve a restrição à distribuição do produto ucraniano e agendou para o final<strong>de</strong> setembro a visita à fábrica ucraniana.Para minimizar os <strong>de</strong>sentendimentos vistos na última inspeção, <strong>Farmanguinhos</strong>encaminhou, no início <strong>de</strong> setembro, uma missão <strong>de</strong> técnicos especialistas eminspeção <strong>de</strong> produto biológico à Ucrânia, a qual contou inclusive com o auxílio <strong>de</strong>Biomanguinhos, numa missão <strong>de</strong> pré-inspeção. O objetivo principal era levantartodas as não-conformida<strong>de</strong>s apontadas pela Anvisa que levaram ao diagnóstico<strong>de</strong> que parte do processo <strong>de</strong> produção da <strong>insulina</strong> tinha passagem pela fábrica<strong>de</strong> L’viv e auditá-las. Como resultado, a pré-inspeção comprovou a dificulda<strong>de</strong> norastreamento documental do dossiê <strong>de</strong> produção, principalmente no cálculo daprodutivida<strong>de</strong> nas diferentes etapas do processo produtivo. Em alguns pontos25