Том 2 â2 - ÐбÑеÑÑво ÐиоÑÐµÑ Ð½Ð¾Ð»Ð¾Ð³Ð¾Ð² РоÑÑии им. Ю.Ð. ÐвÑинникова
Том 2 â2 - ÐбÑеÑÑво ÐиоÑÐµÑ Ð½Ð¾Ð»Ð¾Ð³Ð¾Ð² РоÑÑии им. Ю.Ð. ÐвÑинникова
Том 2 â2 - ÐбÑеÑÑво ÐиоÑÐµÑ Ð½Ð¾Ð»Ð¾Ð³Ð¾Ð² РоÑÑии им. Ю.Ð. ÐвÑинникова
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
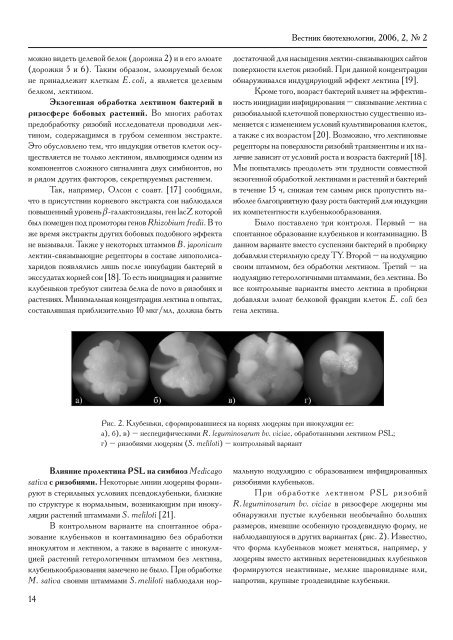
Вестник биотехнологии, 2006, 2, № 2можно видеть целевой белок (дорожка 2) и в его элюате(дорожки 5 и 6). Таким образом, элюируемый белокне принадлежит клеткам E. coli, а является целевымбелком, лектином.Экзогенная обработка лектином бактерий вризосфере бобовых растений. Во многих работахпредобработку ризобий исследователи проводили лектином,содержащимся в грубом семенном экстракте.Это обусловлено тем, что индукция ответов клеток осуществляетсяне только лектином, являющимся одним изкомпонентов сложного сигналинга двух симбионтов, нои рядом других факторов, секретируемых растением.Так, например, Олсон с соавт. [17] сообщили,что в присутствии корневого экстракта сои наблюдалсяповышенный уровень -галактозидазы, ген lacZ которойбыл помещен под промоторы генов Rhizobium fredii. В тоже время экстракты других бобовых подобного эффектане вызывали. Также у некоторых штаммов B. japonicumлектин-связывающие рецепторы в составе липополисахаридовпоявлялись лишь после инкубации бактерий вэкссудатах корней сои [18]. То есть инициация и развитиеклубеньков требуют синтеза белка de novo в ризобиях ирастениях. Минимальная концентрация лектина в опытах,составлявшая приблизительно 10 мкг/мл, должна бытьдостаточной для насыщения лектин-связывающих сайтовповерхности клеток ризобий. При данной концентрацииобнаруживался индуцирующий эффект лектина [19].Кроме того, возраст бактерий влияет на эффективностьинициации инфицирования – связывание лектина сризобиальной клеточной поверхностью существенно изменяетсяс изменением условий культивирования клеток,а также с их возрастом [20]. Возможно, что лектиновыерецепторы на поверхности ризобий транзиентны и их наличиезависит от условий роста и возраста бактерий [18].Мы попытались преодолеть эти трудности совместнойэкзогенной обработкой лектинами и растений и бактерийв течение 15 ч, снижая тем самым риск пропустить наиболееблагоприятную фазу роста бактерий для индукцииих компетентности клубенькообразования.Было поставлено три контроля. Первый – наспонтанное образование клубеньков и контаминацию. Вданном варианте вместо суспензии бактерий в пробиркудобавляли стерильную среду TY. Второй – на нодуляциюсвоим штаммом, без обработки лектином. Третий – нанодуляцию гетерологичными штаммами, без лектина. Вовсе контрольные варианты вместо лектина в пробиркидобавляли элюат белковой фракции клеток E. coli безгена лектина.Рис. 2. Клубеньки, сформировавшиеся на корнях люцерны при инокуляции ее:а), б), в) – неспецифическими R. leguminosarum bv. viciae, обработанными лектином PSL;г) – ризобиями люцерны (S. meliloti) – контрольный вариантВлияние пролектина PSL на симбиоз Medicagosativa с ризобиями. Некоторые линии люцерны формируютв стерильных условиях псевдоклубеньки, близкиепо структуре к нормальным, возникающим при инокуляциирастений штаммами S. meliloti [21].В контрольном варианте на спонтанное образованиеклубеньков и контаминацию без обработкиинокулятом и лектином, а также в варианте с инокуляциейрастений гетерологичным штаммом без лектина,клубенькообразования замечено не было. При обработкеM. sativa своими штаммами S. meliloti наблюдали нормальнуюнодуляцию с образованием инфицированныхризобиями клубеньков.При обработке лектином PSL ризобийR. leguminosarum bv. viciae в ризосфере люцерны мыобнаружили пустые клубеньки необычайно большихразмеров, имевшие особенную гроздевидную форму, ненаблюдавшуюся в других вариантах (рис. 2). Известно,что форма клубеньков может меняться, например, улюцерны вместо активных веретеновидных клубеньковформируются неактивные, мелкие шаровидные или,напротив, крупные гроздевидные клубеньки.14