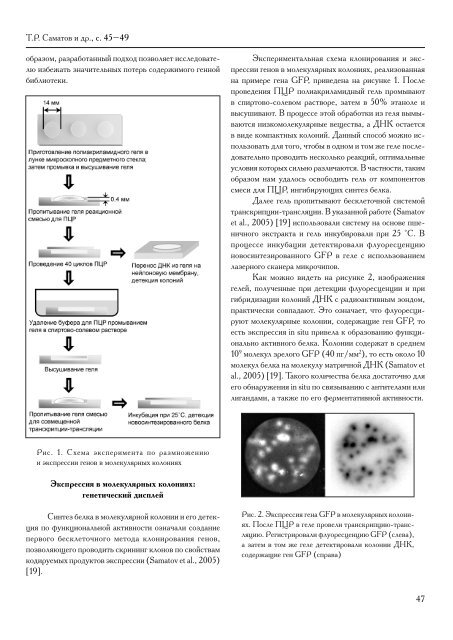
Т.Р. Саматов и др., с. 45–49образом, разработанный подход позволяет исследователюизбежать значительных потерь содержимого геннойбиблиотеки.Экспериментальная схема клонирования и экспрессиигенов в молекулярных колониях, реализованнаяна примере гена GFP, приведена на рисунке 1. Послепроведения ПЦР полиакриламидный гель промываютв спиртово-солевом растворе, затем в 50% этаноле ивысушивают. В процессе этой обработки из геля вымываютсянизкомолекулярные вещества, а ДНК остаетсяв виде компактных колоний. Данный способ можно использоватьдля того, чтобы в одном и том же геле последовательнопроводить несколько реакций, оптимальныеусловия которых сильно различаются. В частности, такимобразом нам удалось освободить гель от компонентовсмеси для ПЦР, ингибирующих синтез белка.Далее гель пропитывают бесклеточной системойтранскрипции-трансляции. В указанной работе (Samatovet al., 2005) [19] использовали систему на основе пшеничногоэкстракта и гель инкубировали при 25 °С. Впроцессе инкубации детектировали флуоресценциюновосинтезированного GFP в геле с использованиемлазерного сканера микрочипов.Как можно видеть на рисунке 2, изображениягелей, полученные при детекции флуоресценции и пригибридизации колоний ДНК с радиоактивным зондом,практически совпадают. Это означает, что флуоресцируютмолекулярные колонии, содержащие ген GFP, тоесть экспрессия in situ привела к образованию функциональноактивного белка. Колонии содержат в среднем10 9 молекул зрелого GFP (40 пг/мм 2 ), то есть около 10молекул белка на молекулу матричной ДНК (Samatov etal., 2005) [19]. Такого количества белка достаточно дляего обнаружения in situ по связыванию с антителами илилигандами, а также по его ферментативной активности.Рис. 1. Схема эксперимента по размножениюи экспрессии генов в молекулярных колонияхЭкспрессия в молекулярных колониях:генетический дисплейСинтез белка в молекулярной колонии и его детекцияпо функциональной активности означали созданиепервого бесклеточного метода клонирования генов,позволяющего проводить скрининг клонов по свойствамкодируемых продуктов экспрессии (Samatov et al., 2005)[19].Рис. 2. Экспрессия гена GFP в молекулярных колониях.После ПЦР в геле провели транскрипцию-трансляцию.Регистрировали флуоресценцию GFP (слева),а затем в том же геле детектировали колонии ДНК,содержащие ген GFP (справа)47
Вестник биотехнологии, 2006, 2, № 248Разработанный метод позволяет осуществлятьбыстрый функциональный скрининг большого числаклонов одновременно. Благодаря отсутствию клеточныхстенок, мембран, капель водно-масляной эмульсии и т.д.имеется прямой доступ к новосинтезированным белкам,что облегчает и ускоряет тестирование их функции. Крометого, исследователь имеет возможность вводить в гельпосле экспрессии различные реагенты и, таким образом,тестировать специфическую активность клонов в условиях,отличных от условий транскрипции-трансляции.Полученные результаты позволяют рассматриватьразработанный метод как новую разновидность генетическогодисплея, обладающую рядом существенныхпреимуществ перед используемыми в настоящее времяподходами. В частности, физическая связь фенотипа игенотипа осуществляется за счет того, что ген и соответствующийему белковый продукт находятся в однойи той же молекулярной колонии. Это позволяет обойтисьбез модификаций белка, обеспечивающих ковалентнуюсвязь с собственной матрицей либо образование с нейнековалентного комплекса, как у большинства бесклеточныхгенетических дисплеев. Таким образом, нативнаяструктура белкового продукта клонов не нарушается.Известно, что бесклеточные системы синтеза белкатранслируют только каждую десятую молекулу мРНК,внесенную в реакционную смесь (Pavlov & Ehrenberg,1996) [16]. Это означает, что в результате экспрессиибиблиотеки, в которой последовательности могут бытьпредставлены всего в одном экземпляре, часть клоновнеизбежно останется вне поля зрения исследователя.В то же время предлагаемый нами подход обеспечиваетразмножение каждой молекулы библиотеки в видемолекулярной колонии, которая содержит до 100 миллионовкопий исходной матрицы. Следовательно, дажепри малоэффективном вовлечении матриц в трансляциюэкспрессирован будет каждый клон.Более того, в результате экспрессии в молекулярнойколонии оказывается до 10 9 молекул белковогопродукта данного клона. Таким образом, белок имеетвозможность формировать олиго- или даже мультимерныекомплексы, если этого требует проявление егофункциональной активности.В заключение хотелось бы отметить, что в определенномсмысле молекулярные колонии можно рассматриватькак некие клетки, лишенные оболочки. Онипредставляют собой отдельные компартменты, где происходятбиохимические процессы. Их геном представленмногими копиями одного гена, который они реплицируюти экспрессируют. Подобно живым организмам, они добываютиз окружающей среды энергию и материал дляпроизводства своих компонентов.Работа выполнена при финансовой поддержкепрограммы Президиума Российской академии наук«Молекулярная и клеточная биология».Литература1. Четверин А.Б. и Четверина Е.В. Способ клонированиянуклеиновых кислот. Патент РФ № 2 114 175 – 1998.2. Четверина Е.В., Кравченко А.В., Фалалеева М.В.,Четверин А.Б. Экспресс-гибридизация молекулярныхколоний с флуоресцентными зондами (в печати – «Биоорган.химия»).3. Brenner S., Williams S.R., Vermaas E.H., Storck T., MoonK., McCollum C., Mao J.-I., Luo S., Kirchner J.J., EletrS., DuBridge R.B., Burcham T. and Albrecht G. In vitrocloning of complex mixtures of DNA on microbeads: physicalseparation of differentially expressed cDNAs // Proc. NatlAcad. Sci. USA. – 2000. – Vol. 97. – P. 1665–1670.4. Chetverin A.B. and Kramer F.R. Oligonucleotide arrays:new concepts and possibilities // Bio/Technology. – 1994.– Vol. 12. – P. 1093–1100.5. Chetverina H.V. and Chetverin A.B. Cloning of RNAmolecules in vitro // Nucleic Acids Res. – 1993. – Vol.21. – P. 2349–2053.6. Chetverina H.V., Samatov T.R., Ugarov V.I. and ChetverinA.B. Molecular colony diagnostics: detection and quantitationof viral nucleic acids by in-gel PCR // BioTechniques.– 2002. – Vol. 33. – P. 150–157.7. Dressman D., Yan H., Traverso G., Kinzler K.W. andVogelstein B. Transforming single DNA molecules intofluorescent magnetic particles for detection and enumeration ofgenetic variations // Proc. Natl Acad. Sci. USA. – 2003.– Vol. 100. – P. 8817–8822.8. De Figueiredo P., Roberts R.L. and Nester E.W. DARTs:A DNA-based in vitro polypeptide display technology //Proteomics. – 2004. –Vol. 4. – P. 3128–3140.9. Hanes J. and Pluckthun A. In vitro selection and evolution offunctional proteins by using ribosome display // Proc. NatlAcad. Sci. USA. – 1997. – Vol. 94. – P. 4937–4942.10. Lukyanov K.A., Matz M.V., Bogdanova E.A., GurskayaN.G. and Lukyanov S.A. Molecule by molecule PCRamplification of complex DNA mixtures for direct sequencing:an approach to in vitro cloning // Nucleic Acids Res. – 1996.– Vol. 24. – P. 2194–2195.11. Mattheakis L.C., Bhatt R.R. and Dower W.J. An in vitropolysome display system for identifying ligands from very largepeptide libraries // Proc. Natl Acad. Sci. USA. – 1994.– Vol. 91. – P. 9022–9026.