Br Br
Br Br
Br Br
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
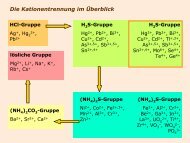
<strong>Br</strong>om - Vorkommen<br />
<strong>Br</strong>om kommt nur gebunden in Form von <strong>Br</strong>omiden vor,<br />
beispielsweise als Silberbromid Ag<strong>Br</strong>.<br />
Ein anderes wichtiges Vorkommen des <strong>Br</strong>oms ist im<br />
Meerwasser (1 m 3 Meerwasser enthält rund 68 g <strong>Br</strong>omid), in<br />
Solequellen und in Salzseen.<br />
Von <strong>Br</strong>om gibt es zwei natürliche Isotope<br />
81<br />
35<br />
<strong>Br</strong><br />
79<br />
35<br />
<strong>Br</strong><br />
50.69 % 49.31 %
2 K<strong>Br</strong> + Cl 2<br />
Darstellung<br />
<strong>Br</strong>om kann aus seinen Verbindungen durch Chlor freigesetzt<br />
werden:<br />
Cl 2 + 2 e –<br />
2 <strong>Br</strong> –<br />
2 Cl –<br />
<strong>Br</strong> 2 + 2 e –<br />
2 KCl + <strong>Br</strong> 2<br />
E 0 = 1.3583 V<br />
E 0 = 1.065 V
Darstellung<br />
Heißentbromung bei <strong>Br</strong>omidgehalten von 0.2 – 3.5 kg/m 3 .<br />
Die Oxidation erfolgt bei Temperaturen zwischen 90 und<br />
100°C. Das entstandende <strong>Br</strong>om wird mit Dampf<br />
ausgetrieben (steaming out).<br />
Kaltentbromung bei geringen <strong>Br</strong>omgehalten.<br />
Die Oxidation erfolgt bei Normaltemperaturen, zur<br />
Entbromung wird Luft verwendet (blowing out).<br />
Im Labor:<br />
2 K<strong>Br</strong> + H2SO4 4 H<strong>Br</strong> + MnO2 2 H<strong>Br</strong> + K 2SO 4<br />
Mn<strong>Br</strong> 2 + 2 H 2O + <strong>Br</strong> 2
Physikalische Eigenschaften<br />
Neben Quecksilber ist <strong>Br</strong>om das einzige unter<br />
Normalbedingungen flüssige Element.<br />
Dichte 3.14 g · cm –3 (20°C)<br />
Sdp. 58.78 °C<br />
Smp. – 7.25 °C<br />
Mit abnehmender Temperatur hellt sich die Farbe auf.<br />
Temperatur nimmt ab<br />
T = – 253 °C<br />
(20 K)
<strong>Br</strong>om löst sich gut in Wasser:<br />
Physikalische Eigenschaften<br />
Bei einer Temperatur von 25 °C lösen sich 0.2141 mol <strong>Br</strong>om<br />
in einem Liter Wasser. Diese Lösung ist etwa 0.2 molar und<br />
wird als <strong>Br</strong>omwasser bezeichnet.<br />
Mit unpolaren Lösungsmitteln wie Schwefelkohlenstoff,<br />
CS 2 , oder Tetrachlorkohlenstoff, CCl 4 , mischt sich <strong>Br</strong>om<br />
unbegrenzt.
Chemische Eigenschaften<br />
Die chemischen Eigenschaften von <strong>Br</strong>om gleichen denen<br />
des Chlors, wobei <strong>Br</strong>om im allgemeinen nicht ganz so heftig<br />
reagiert.<br />
Jedoch tritt mit Metallen oftmals eine energische Reaktion<br />
ein.<br />
<strong>Br</strong> 2 + 2 K 2 K<strong>Br</strong><br />
Gegen feuchtes <strong>Br</strong>om sind nur Platin und Tantal beständig.<br />
Gegen trockenes <strong>Br</strong>om sind auch andere Metalle, wie<br />
beispielsweise Blei, Silber aber nicht dagegen Eisen<br />
beständig.
Chemische Eigenschaften<br />
<strong>Br</strong>om entzieht vielen Wasserstoffverbindungen den<br />
Wasserstoff:<br />
H 2S + <strong>Br</strong> 2<br />
2 H<strong>Br</strong> + 1 / 8 S 8
<strong>Br</strong>omwasserstoff, H<strong>Br</strong><br />
Die Darstellung von <strong>Br</strong>omwasserstoff kann nicht so wie die<br />
des Chlorwasserstoffs oder des Fluorwasserstoffs erfolgen,<br />
da die Schwefelsäure das gebildete H<strong>Br</strong> teilweise bis zum<br />
<strong>Br</strong>om oxidiert:<br />
2 K<strong>Br</strong> + H 2SO 4<br />
2 H<strong>Br</strong> + H 2SO 4<br />
K 2SO 4 + 2 H<strong>Br</strong><br />
<strong>Br</strong> 2 + SO 2 + 2 H 2O<br />
Zur Darstellung müssen daher verdünnte Schwefelsäure<br />
oder nicht-oxidierende Säuren verwendet werden:<br />
3 K<strong>Br</strong> + H 3PO 4<br />
K 3PO 4 + 3 H<strong>Br</strong>
<strong>Br</strong>omwasserstoff, H<strong>Br</strong><br />
Im Labor wird zumeist Wasser als Protonenquelle und ein<br />
leichtzersetzliches <strong>Br</strong>omidsalz verwendet:<br />
P<strong>Br</strong> 3 + 3 H 2O H 3PO 3 + 3 H<strong>Br</strong><br />
Phosphortribromid wird direkt aus den Elementen<br />
hergestellt:<br />
2 P + 3 <strong>Br</strong> 2<br />
2 P<strong>Br</strong> 3
Physikalische Eigenschaften<br />
Farbloses Gas, kann durch Abkühlung zu einer farblosen<br />
Flüssigkeit verdichtet werden, weitere Abkühlung führt zu<br />
farblosen Kristallen.<br />
Smp. – 86.82 °C, d = 2.603 g · cm –3 (– 84°C),<br />
Sdp. – 66.73 °C<br />
<strong>Br</strong>omwasserstoff ist sehr gut löslich in Wasser:<br />
1 Liter Wasser löst bei einer Temperatur von 0 °C 612 Liter<br />
(~ 25 mol) <strong>Br</strong>omwasserstoffgas.
Chemische Eigenschaften<br />
Wässrige Lösungen reagieren sauer - <strong>Br</strong>omwasserstoffsäure.<br />
Chlor setzt aus einer wässrigen Lösung von <strong>Br</strong>omwasserstoff<br />
rotbraune <strong>Br</strong>omdämpfe frei:<br />
2 H<strong>Br</strong> + Cl 2<br />
2 HCl + <strong>Br</strong> 2<br />
H<strong>Br</strong> ist ein stärkeres Reduktionsmittel als HCl und Chlor<br />
ist ein stärkeres Oxidationsmittel als <strong>Br</strong>om.<br />
Die Salze des <strong>Br</strong>omwasserstoffs, die <strong>Br</strong>omide, sind zumeist<br />
gut löslich in Wasser.<br />
Schwerlöslich sind Silberbromid, Ag<strong>Br</strong>,<br />
Quecksilber(I)bromid, Hg 2 <strong>Br</strong> 2 sowie Bleibromid, Pb<strong>Br</strong> 2 .
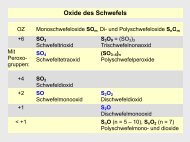
Sauerstoffsäuren des <strong>Br</strong>oms<br />
Von <strong>Br</strong>om gibt es vier Sauerstoffsäuren:<br />
• die Hypobromige Säure HO<strong>Br</strong><br />
• die <strong>Br</strong>omige Säure H<strong>Br</strong>O 2<br />
• die <strong>Br</strong>omsäure H<strong>Br</strong>O 3<br />
• die Perbromsäure H<strong>Br</strong>O 4
Die Hypobromige Säure, H<strong>Br</strong>O<br />
Die hypobromige Säure ist eine schwächere Säure als die<br />
hypochlorige Säure. Ihre Salze, die Hypobromite, lassen<br />
sich durch Schütteln von <strong>Br</strong>omwasser mit Quecksilberoxid<br />
darstellen:<br />
2 <strong>Br</strong> 2 + 3 HgO + H 2 O Hg<strong>Br</strong> 2 · 2 HgO + 2 HO<strong>Br</strong><br />
Auch durch Umsetzung von <strong>Br</strong>om mit Alkalilaugen bei einer<br />
Temperatur von 0 °C werden Hypobromite erhalten:<br />
<strong>Br</strong> 2 + 2 NaOH Na<strong>Br</strong> + NaO<strong>Br</strong> + H 2 O
Die Hypobromite<br />
Wässrige Lösungen von Hypobromiten besitzen eine<br />
ausgeprägte Bleich- und Oxidationswirkung.<br />
Hypobromite können durch Kristallisation aus Na<strong>Br</strong>/NaO<strong>Br</strong>-<br />
Lösungen erhalten werden. Sie sind gelbgefärbt und<br />
besitzen einen aromatischen Geruch.<br />
Bei Temperaturen oberhalb von 0 °C disproportionieren sie<br />
in wässriger Lösungen quantitativ zu <strong>Br</strong>omid und <strong>Br</strong>omat:<br />
3 <strong>Br</strong>O –<br />
2 <strong>Br</strong> – –<br />
+ <strong>Br</strong>O3
Die <strong>Br</strong>omige Säure, H<strong>Br</strong>O 2<br />
Die Salze der bromigen Säure, die <strong>Br</strong>omite entstehen als<br />
Zwischenprodukt bei der Oxidation von Hypobromiten<br />
oder <strong>Br</strong>om mit Hypochloriten<br />
<strong>Br</strong>O – + ClO –<br />
– –<br />
<strong>Br</strong>O2 + Cl<br />
oder durch Disproportionierung von Hypobromit in<br />
alkalischer Lösung:<br />
2 <strong>Br</strong>O –<br />
– –<br />
<strong>Br</strong>O2 + <strong>Br</strong>
Die <strong>Br</strong>omite<br />
Umgekehrt lässt sich in trockener Reaktion bei 190 – 225 °C<br />
durch Komproportionierung von <strong>Br</strong>omat und <strong>Br</strong>omid das<br />
<strong>Br</strong>omit erhalten:<br />
– –<br />
2 <strong>Br</strong>O3 + <strong>Br</strong><br />
–<br />
3 <strong>Br</strong>O2 <strong>Br</strong>omite sind gelb gefärbt und nur in alkalischer Lösung<br />
beständig. In saurer Lösung erfolgt ihre Zersetzung.
Die <strong>Br</strong>omsäure, H<strong>Br</strong>O 3<br />
<strong>Br</strong>omsäure ist eine starke Säure. Ihre Darstellung kann<br />
durch Umsetzung von Bariumbromat mit verdünnter<br />
Schwefelsäure erfolgen:<br />
Ba(<strong>Br</strong>O 3) 2 + H 2SO 4<br />
Ab einem Gehalt von 50 % tritt Zersetzung ein:<br />
4 H<strong>Br</strong>O 3<br />
BaSO 4 + 2 H<strong>Br</strong>O 3<br />
2 <strong>Br</strong> 2 + 5 O 2 + 2 H 2O
Die <strong>Br</strong>omate<br />
Die Salze der <strong>Br</strong>omsäure, die <strong>Br</strong>omate, werden durch<br />
Disproportionierung von <strong>Br</strong>om in 50 – 80 °C heißen<br />
Laugen erhalten:<br />
<strong>Br</strong> 2 + 6 OH –<br />
Die Darstellung von <strong>Br</strong>omaten kann auch durch Oxidation<br />
von heißer alkalischer <strong>Br</strong>omidlösung mit Chlor oder<br />
Hypochlorit erfolgen:<br />
<strong>Br</strong> – + 3 Cl 2 + 6 OH –<br />
– –<br />
<strong>Br</strong>O3 + 5 <strong>Br</strong> + 3 H2O<br />
– –<br />
<strong>Br</strong>O3 + 6 Cl + 3 H2O
Eigenschaften der <strong>Br</strong>omsäure<br />
<strong>Br</strong>omsäure ist ein kräftiges Oxidationsmittel. Wässrige<br />
Lösungen von <strong>Br</strong>omaten werden für Redoxtitrationen<br />
verwendet.<br />
<strong>Br</strong>omatometrie<br />
Die quantitative Komproportionierung von <strong>Br</strong>omat und<br />
<strong>Br</strong>omid zu <strong>Br</strong>om wird bei der Herstellung von <strong>Br</strong>om-<br />
Lösungen für Redox-Titrationen genutzt.<br />
– – +<br />
<strong>Br</strong>O3 + 5 <strong>Br</strong> + 6 H<br />
<strong>Br</strong>omometrie<br />
3 <strong>Br</strong> 2 + 3 H 2O
Perbromsäure, H<strong>Br</strong>O 4<br />
Perbromate werden durch Oxidation von <strong>Br</strong>omaten mit sehr<br />
starken Oxidationsmitteln erhalten:<br />
– –<br />
<strong>Br</strong>O3 + F2 + H2O <strong>Br</strong>O4 + 2 HF<br />
Verdünnte Lösungen können bis zu einem Gehalt von 55 %<br />
(6 molar) aufkonzentriert werden, höhere Gehalte führen<br />
dagegen zu instabilen Mischungen.<br />
Verdünnte Perbromsäure ist ein träges Oxidationsmittel.<br />
Konzentriertere Lösungen sind dagegen reaktiv:<br />
• 3 molare Perbromsäure greift rostfreien Stahl an<br />
• 12 molare Perbromsäure explodiert bei Berührung mit<br />
Salpetersäure