5 Ionenverbindungen, Salze - hep.info
5 Ionenverbindungen, Salze - hep.info
5 Ionenverbindungen, Salze - hep.info
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
5 I o n e n v e r b i n d u n g e n , S a l z e<br />
Wegen ihrer lockeren Struktur besitzen kristallwasserhaltige <strong>Salze</strong> gewöhnlich<br />
kleinere Gitterenergien und lösen sich daher schneller, allerdings endotherm,<br />
weil keine Hydrationsenthalpie mehr frei wird.<br />
Das Auflösen eines <strong>Salze</strong>s in Wasser ist ein chemischer Vorgang. Feste <strong>Salze</strong>,<br />
wie auch destilliertes Wasser, zeigen keine elektrische Leitfähigkeit (Wasser nur in<br />
ganz geringem Ausmass). Eine Salzlösung hingegen leitet den elektrischen Strom.<br />
Damit sind die Kriterien auf Stoffebene, an denen man eine chemische Reaktion<br />
erkennt, erfüllt: Änderung der Stoffeigenschaften, Energieumsatz und Umkehrbarkeit<br />
(Abschnitt 4.1). Auf mikroskopischer Ebene findet eine Umgruppierung von<br />
Teilchen statt (Ionen im Ionengitter, Wassermoleküle; Wassermoleküle gebunden<br />
an Ionen) sowie eine Änderung der Aufenthaltswahrscheinlichkeit von Elektronen<br />
(stärkere Polarisierung der O H-Bindungen im H2O-Molekül durch die Ionenladungen).<br />
Interessant ist in diesem Zusammenhang, dass die Bindung der H2O-<br />
Moleküle an das Al 3+ -Ion z.B. stärker ist als die Bindungsenthalpie im H2O-Molekül<br />
selbst (767 kJ/mol für die H2O-Moleküle im Al 3+ -Komplex, 463 kJ/mol für die<br />
O H-Bindung).<br />
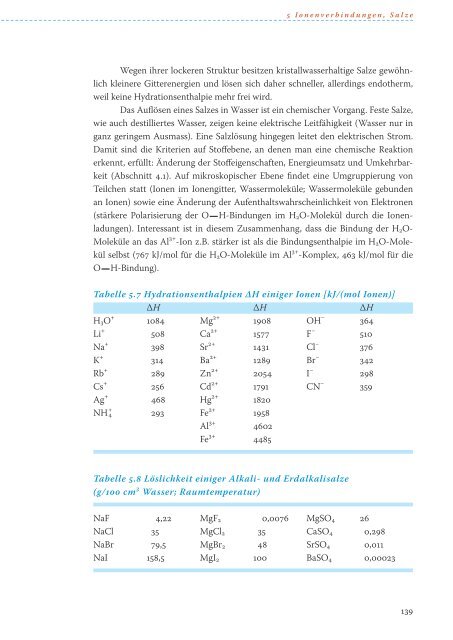
Tabelle 5.7 Hydrationsenthalpien ∆H einiger Ionen [kJ/(mol Ionen)]<br />
∆H ∆H ∆H<br />
H3O + 1084 Mg 2+ 1908 OH − 364<br />
Li + 508 Ca 2+ 1577 F − 510<br />
Na + 398 Sr 2+ 1431 Cl − 376<br />
K + 314 Ba 2+ 1289 Br − 342<br />
Rb + 289 Zn 2+ 2054 I − 298<br />
Cs + 256 Cd 2+ 1791 CN − 359<br />
Ag + 468 Hg 2+ 1820<br />
NH + 4 293 Fe 2+ 1958<br />
Al 3+ 4602<br />
Fe 3+ 4485<br />
Tabelle 5.8 Löslichkeit einiger Alkali- und Erdalkalisalze<br />
(g/100 cm 3 Wasser; Raumtemperatur)<br />
NaF 4,22 MgF2 0,0076 MgSO4 26<br />
NaCl 35 MgCl2 35 CaSO4 0,298<br />
NaBr 79,5 MgBr2 48 SrSO4 0,011<br />
NaI 158,5 MgI2 100 BaSO4 0,00023<br />
139