Theorie zum Histidase- Versuch
Theorie zum Histidase- Versuch
Theorie zum Histidase- Versuch
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
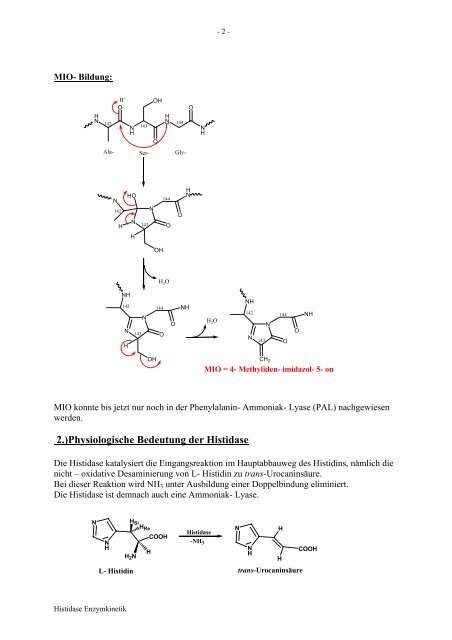
MIO- Bildung:<br />
H<br />
N<br />
142<br />
N<br />
O<br />
142<br />
H +<br />
H<br />
NH<br />
142<br />
<strong>Histidase</strong> Enzymkinetik<br />
N<br />
H<br />
N<br />
H<br />
HO<br />
N<br />
H<br />
143<br />
143<br />
143<br />
N<br />
N<br />
OH<br />
- 2 -<br />
MIO konnte bis jetzt nur noch in der Phenylalanin- Ammoniak- Lyase (PAL) nachgewiesen<br />
werden.<br />
2.)Physiologische Bedeutung der <strong>Histidase</strong><br />
OH<br />
OH<br />
H<br />
N<br />
144<br />
O<br />
H 2O<br />
144<br />
O<br />
O<br />
144<br />
O<br />
O<br />
H<br />
N<br />
NH<br />
N<br />
H<br />
H 2O<br />
Die <strong>Histidase</strong> katalysiert die Eingangsreaktion im Hauptabbauweg des Histidins, nämlich die<br />
nicht – oxidative Desaminierung von L- Histidin zu trans-Urocaninsäure.<br />
Bei dieser Reaktion wird NH3 unter Ausbildung einer Doppelbindung eliminiert.<br />
Die <strong>Histidase</strong> ist demnach auch eine Ammoniak- Lyase.<br />
N<br />
Ala- Ser- Gly-<br />
N<br />
H<br />
H SiHRe<br />
H 2N<br />
L- Histidin<br />
H<br />
O<br />
COOH<br />
<strong>Histidase</strong><br />
-NH 3<br />
NH<br />
142<br />
N<br />
143<br />
N<br />
CH 2<br />
144<br />
O<br />
O<br />
NH<br />
MIO = 4- Methyliden- imidazol- 5- on<br />
N<br />
N<br />
H<br />
H<br />
H<br />
trans-Urocaninsäure<br />
COOH