Supraleiter - IPHT Jena
Supraleiter - IPHT Jena
Supraleiter - IPHT Jena
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Die „permanenten Gase“<br />
„Permanente Gase“ (CO, O 2, N 2, H 2, He, …)<br />
ließen sich Mitte 19. Jhd. nicht verflüssigen<br />
1869 Thomas Andrews, kritische Temperatur für<br />
Gasverflüssigung<br />
1877 Paul Caillitet/ M. Raoul Pictet unabhängig<br />
(20 Tage später)<br />
Sauerstoff O 2, T S = - 182,2ºC (90,2 K)<br />
1882 van der Waals, Zustandsgleichung für reale Gase<br />
1883 Sigmund v. Wroblewski und Karol Olszewski<br />
Stickstoff N 2, T S = - 195,8ºC (77,4 K)<br />
1898 James Dewar (in Konkurrenz zu HKO)<br />
Wasserstoff H 2, T S = - 252,9ºC (20,3 K)<br />
1899 J. Dewar damals niedrigste Temperatur<br />
fester Wasserstoff T S = - 259,1ºC (14 K)<br />
Druck<br />
Flüssigkeit<br />
Koexistenz<br />
Flüssigkeit<br />
Dampf<br />
Dampf<br />
kritischer<br />
Punkt<br />
Volumen<br />
T > T K<br />
T K<br />
T < T K<br />
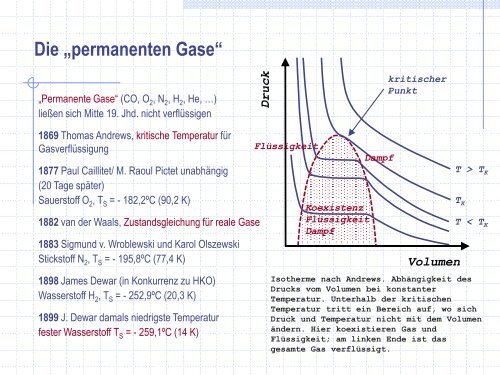
Isotherme nach Andrews. Abhängigkeit des<br />
Drucks vom Volumen bei konstanter<br />
Temperatur. Unterhalb der kritischen<br />
Temperatur tritt ein Bereich auf, wo sich<br />
Druck und Temperatur nicht mit dem Volumen<br />
ändern. Hier koexistieren Gas und<br />
Flüssigkeit; am linken Ende ist das<br />
gesamte Gas verflüssigt.